
2024年开年到现在,可能是无数股民最难忘的岁月。股海弄潮,引无数股民竞折腰。作为创新药“一哥”的恒瑞医药,它的的股价自然会引得大家的关注。截至2024年2月2日收盘,恒瑞的估值恰好到了最近五年的估值低位,距离2021年历史高点市值也缩水了近62.9%,达到了49.51倍的PE(滚动市盈率)。随着新一周的开盘,经过两个交易日的上涨,截止2024年2月6日收盘,恒瑞医药收获了单日9.63%的涨幅,市值来到了2613亿元。
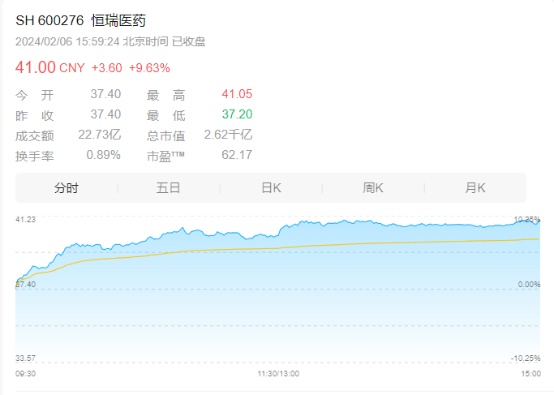
医药和白酒曾是A股机构投资者的心头肉,“医药配白酒,越喝越有”这句话也在坊间盛传。恒瑞医药凭借其在生物医药行业龙头地位,收获众多机构芳心,也成了多个基金重仓的对象。公司市值更是在2020年底突破6000亿元,历史涨幅(不含上市首日)一度超过220倍,被众多投资者称为“药中茅台”。自那以后,恒瑞医药股价便一跌再跌,截止目前,每股已经不足50元,市值跌破3000亿大关,接近腰斩。创新不易,未来可期。
14款自研新药+2款引进新药!恒瑞进入收获期
截止恒瑞医药已有14个自研新药获批上市,第一款引进的1类新药林普利塞于2022年11月获批上市,第二款引进创新药奥特康唑是公司从美国 Mycovia 公司引进的新型口服唑类抗真菌药物。(推荐阅读:阿得贝利单抗注射液:恒瑞医药国产PD-L1抑制剂展现实力,市场可期!)
从2011年至2024年2月的约14年时间里,恒瑞一共获得了国家药品监督管理局14款1类新药的上市批准,平均每年都有一款。截至2023年6月底,恒瑞医药正在进行临床试验的创新药项目超80个,管线潜力十足。在海外研发投入上,据2022年年报,恒瑞医药2022年海外研发投入共计12.72亿元,占总体研发投入的20.04%,同时恒瑞医药在美国、日本及欧洲均有研发中心。创新药出海是恒瑞摆脱内卷的必经之路。
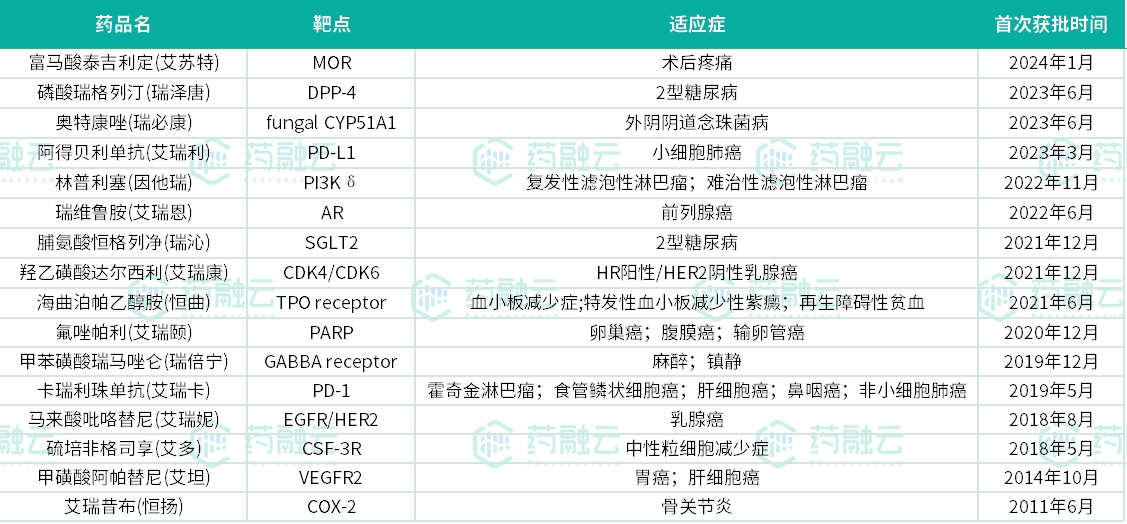
来源:药融云中国药品批文
具体的药物信息整理如下:
01富马酸泰吉利定注射
2024年1月获批,富马酸泰吉利定是一种阿片受体完全激动剂,对阿片受体μ亚型(MOR)具有相对的选择性,按照麻醉药品管理。研究数据显示,该药物不仅镇痛效果显著,起效速度快,能有效延缓术后疼痛反弹需补充镇痛的时间;并且在保证镇痛效果的同时,大幅降低了恶心、呕吐和呼吸抑制等常见不良反应的发生率,极大地提升了患者的治疗舒适度和安全性。截至获批时可查询的数据,富马酸泰吉利定注射液相关项目累计已投入研发费用超过1.6亿元。
02磷酸瑞格列汀片
2023年6月获批,磷酸瑞格列汀是恒瑞自主研发的一款 DPP-4 抑制剂,通过抑制 DPP-4 的活性达到降血糖的作用。截至获批时可查询的数据,磷酸瑞格列汀片相关项目累计已投入研发费用约 18,903 万元。
03阿得贝利单抗注射液
2023年3月获批,阿得贝利单抗(SHR-1316)是恒瑞医药研发的人源化抗PD-L1单克隆抗体,能特异性结合PD-L1分子,从而阻断导致肿瘤免疫耐受的PD-1/PD-L1通路,重新激活免疫系统的抗肿瘤活性,达到治疗肿瘤的目的。截至2024年1月,恒瑞最新公告显示,阿得贝利单抗注射液相关项目累计已投入研发费用约5.64亿元。
04脯氨酸恒格列净片
2021年12月获批,脯氨酸恒格列净是一种钠-葡萄糖协同转运蛋白 2(SGLT2)抑制剂,通过抑 制 SGLT2,减少肾小管滤过的葡萄糖的重吸收,从而增加尿糖排泄。截至获批时可查询的数据,脯氨酸恒格列净相关项目累计已投入研发费用约为 27,353 万元。
05 羟乙磺酸达尔西利片
2021年12月获批,羟乙磺酸达尔西利是恒瑞医药自主研发的化学药品 1 类新药,是一种口服、 高效、选择性的小分子 CDK4/6 抑制剂。截至获批时可查询的数据,羟乙磺酸达尔西利相关项目累计已投入研发费用约 36,359 万元。
06海曲泊帕乙醇胺片
2021年6月获批,海曲泊帕乙醇胺片是一种口服非肽类血小板生成素受体(TPO-R)激动剂,通过激活 TPO-R 介导的 STAT 和 MAPK 信号转导通路,促进血小板生成。截至获批时可查询的数据,海曲泊帕乙醇胺片相关项目累计已投入研发费用约为 18,389 万元。
07氟唑帕利胶囊
2020年12月获批,氟唑帕利为小分子PARP抑制剂,可抑制BRCA1/2功能异常细胞中的DNA修复过程,诱导细胞周期阻滞,进而抑制肿瘤细胞增殖。截至获批时可查询的数据,该产品累计已投入研发费用约为 29,492 万元。
08注射用甲苯磺酸瑞马唑仑
2019年12月获批,注射用甲苯磺酸瑞马唑仑是一种短效的 GABAa 受体激动剂,截至获批时可查询的数据,该研发项目上已投入研发费用约 7,135 万元人民币。
09注射用卡瑞利珠单抗
2019年5月获批,注射用卡瑞利珠单抗是人源化抗 PD-1 单克隆抗体,可与人PD-1受体结合并阻断 PD-1/PD-L1 通路,恢复机体的抗肿瘤免疫力,从而形成癌症免疫治疗基础。该产品项目投入研发费用约为 50,431 万元人民币。
10马来酸吡咯替尼片
2018年8月获批,马来酸吡咯替尼是不可逆性人表皮生长因子受体2(HER2)、表皮生长因子受体(EGFR)双靶点的酪氨酸激酶抑制剂,其作用机理为与细胞内HER2和EGFR激酶区的三磷酸腺苷(ATP)结合位点共价结合,阻止肿瘤细胞内HER2和EGFR的同质和异质二聚体形成,抑制其自身的磷酸化,阻断下游信号通路的激活,从而抑制肿瘤细胞生长。该产品的研发项目已投入研发费用约为 55,600 万元人民币。
11硫培非格司亭注射液
2018年5月获批,硫培非格司亭是恒瑞医药自主研发的生物创新药长效粒细胞集落刺激因子(G-CSF)。截至获批时可查询的数据,硫培非格司亭注射液研发项目上已投入研发费用约为 9,800 万元人民币。
12甲磺酸阿帕替尼片
2014年12月获批,阿帕替尼主要用于晚期胃癌标准化疗失败后的治疗,通过竞争性结合细胞内VEGFR-2的ATP结合位点,抑制酪氨酸激酶的生成从而抑制肿瘤组织新血管的生成。阿帕替尼从立项研发到获批上市前后历时10 年,见证了恒瑞自主创新转型的历程。
13艾瑞昔布片
2011年6月获批,艾瑞昔布是新一代非甾体抗炎类创新药,主要用于缓解骨关节炎的疼痛症状,这是恒瑞医药第一个获批上市的国家一类新药。
1.引进的PI3Kδ小分子抑制剂:林普利塞(因他瑞)
林普利塞是恒瑞医药引进的1类新药,由璎黎药业研发,是一种磷脂酰肌醇 3-激酶-δ(Phosphoinositide 3-kinase-δ,PI3Kδ)小分子抑制剂。2021 年 2 月,恒瑞医药与璎黎药业达成协议,璎黎药业授予恒瑞医药针对林普利塞在大中华地区的联合开发权益以及排他性独家商业化权益。
林普利塞于2022年11月正式获批上市,用于治疗既往接受过至少两种系统性治疗的复发或难治(R/R)滤泡性淋巴瘤(FL)成人患者。作为我国首个高选择性PI3Kδ抑制剂,林普利塞采用创新性的药物结构,使其选择性更高、特异性更强,有助于减少高血糖、高血压及腹泻等不良反应情况的发生。同时,林普利塞的给药方式为口服给药,给药频次为一日一次且不受餐食影响,更有助于提升患者依从性,便于临床长期治疗和有效管理。
2.引进的新型抗真菌药物:奥特康唑
奥特康唑(SHR8008)是恒瑞 License in 的一种新型口服四氮唑结构抗真菌药物,可高度特异性抑制真菌 CYP51 酶。2019 年,恒瑞以超 1 亿美元的研发付款和里程碑付款从 Mycovia 公司引进 SHR8008,获得其在中国(包括中国大陆、香港、澳门和台湾地区)的临床开发、注册、生产和市场销售的独家权益。
奥特康唑于2023年6月27日在国内获批,用于治疗重度外阴阴道假丝酵母菌病(VVC),该药为恒瑞合作引进产品中第二个上市的创新药。奥特康唑的上市,将为VVC患者提供新的治疗选择,同时这也是恒瑞医药布局抗感染治疗领域迎来的首个上市1类创新药产品。
总结
作为国内创新药企的标杆,恒瑞医药已有 16个创新药上市,其中13个已经进入国家医保。截至2023年上半年,恒瑞的营收达到111.68亿元,创新药收入还不到一半,含税收入为49.62亿元。随着医保支付压力的加大,创新药在国内市场呈现的是无差别内卷的状态,出海成了扩大市场的必经之路。可喜的是,目前已经有多款国产创新药成功出海。期待恒瑞医药能够保持在国内的研发冲劲,带领国产创新药冲向国际。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论