
实时掌握每月全球范围的新药研发情况,尽在药融云《全球在研新药与靶点月报》。据药融云10月月报数据统计,2023年10月共有179个化药1类新药受理号获CDE承办(含补充申请35个),其中国产127个,进口15个,从申请类型来看,包括临床申请135个,上市申请6个,涉及87个品种,90家企业。
10月共有95个1类治疗用生物制品受理号获CDE承办(含补充申请19个),其中国产63个,进口13个,从申请类型来看,包括临床申请75个,上市申请1个,涉及79个品种,75家企业。中药方面,有1个1类中药受理号获CDE承办,从申请类型来看,全部临床申请涉及1个品种,1家企业。
2023年10月国内获批临床新药一览表
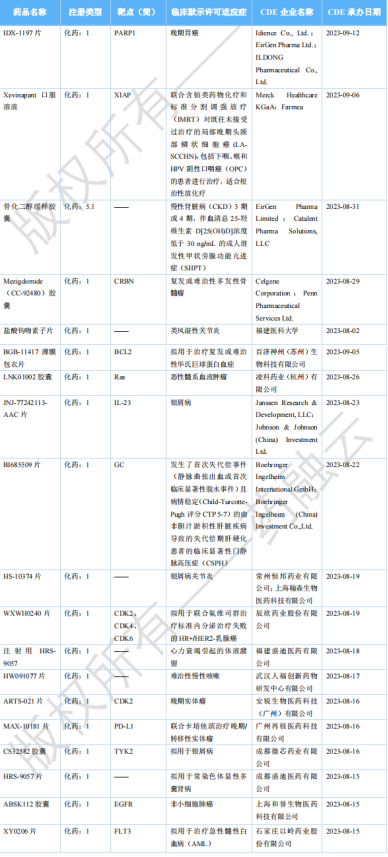
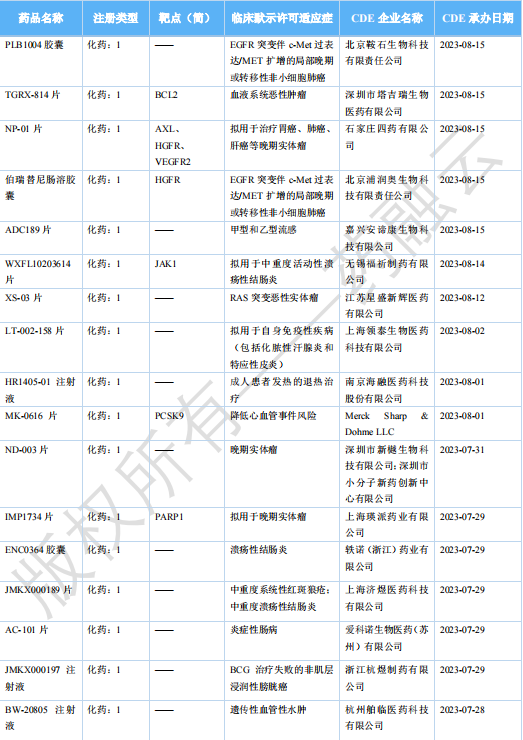
图片来源:药融云《全球在研新药与靶点月报》
10月,共有142款新药获批临床(共计231个受理号),其中包括68款化药,72款生物制品,2款中药;本月有7款新药获批上市。
其中,10月获批上市的7款新药分别是:
1. 庞贝病全新特效药注射用艾夫糖苷酶α在中国获批
10月13日,NMPA发布药品批准证明文件送达信息显示赛诺菲的新药注射用艾夫糖苷酶α首次获批上市。公开资料显示,艾夫糖苷酶α是一种高效酶替代疗法(ERT),可以靶向6-磷酸甘露糖(M6P)受体,从而改善GAA向肌肉细胞的递送,使得多余的糖原得以分解,减少对患者肌肉细胞的损伤。
药融云中国药品审评数据库显示,艾夫糖苷酶α于2021年9月首次获批临床,2022年7月申报上市并在当年8月被纳入优先审评,直至2023年下半年获得NMPA批准进口上市。审评时间轴显示,艾夫糖苷酶α从药审中心承办到获批上市总耗时419天。此前,艾夫糖苷酶α于2021年8月获得美国FDA批准上市,并获得FDA授予突破性疗法认定,目前已在欧盟、日本、加拿大等多个国家和地区获批。
注射用艾夫糖苷酶α批准进口-审评时间轴(部分)

图片来源:药融云中国药品审评数据库
2. 斑秃1类新药甲苯磺酸利特昔替尼国内获批
10月19日,国家药品监督管理局通过优先审评程序批准辉瑞公司申报的1类创新药甲苯磺酸利特昔替尼胶囊(商品名:乐复诺)上市,用于12岁及以上青少年和成人重度斑秃患者。公开资料显示,甲苯磺酸利特昔替尼是一款创新JAK3/TEC激酶家族双通道抑制剂。乐复诺是国内首款获批用于治疗青少年重度斑秃患者的药物。
根据药融云数据统计,2022年9月,特昔替尼胶囊在中国提交上市申请,并于同年11月被国家药监局纳入优先审评审批程序,至今历时一年左右正式获批上市。目前,特昔替尼胶囊已在美国、日本、挪威等多国上市。
3. 全球首款口服TYK2变构抑制剂颂狄多(氘可来昔替尼片)中国获批
10月24日,国家药品监督管理局(NMPA)批准百时美施贵宝公司申报的1类创新药氘可来昔替尼片(商品名:颂狄多)上市,用于适合系统治疗或光疗的成年中重度斑块状银屑病患者。
银屑病是一种常见的慢性、系统性、炎症性、免疫介导疾病,严重损害患者的身心健康与生活质量。在中国,银屑病患病率约为0.47%,患者人数超650万,其中近六成患者病情已发展至中度或重度。
氘可来昔替尼片(国药准字HJ20230120)基本信息
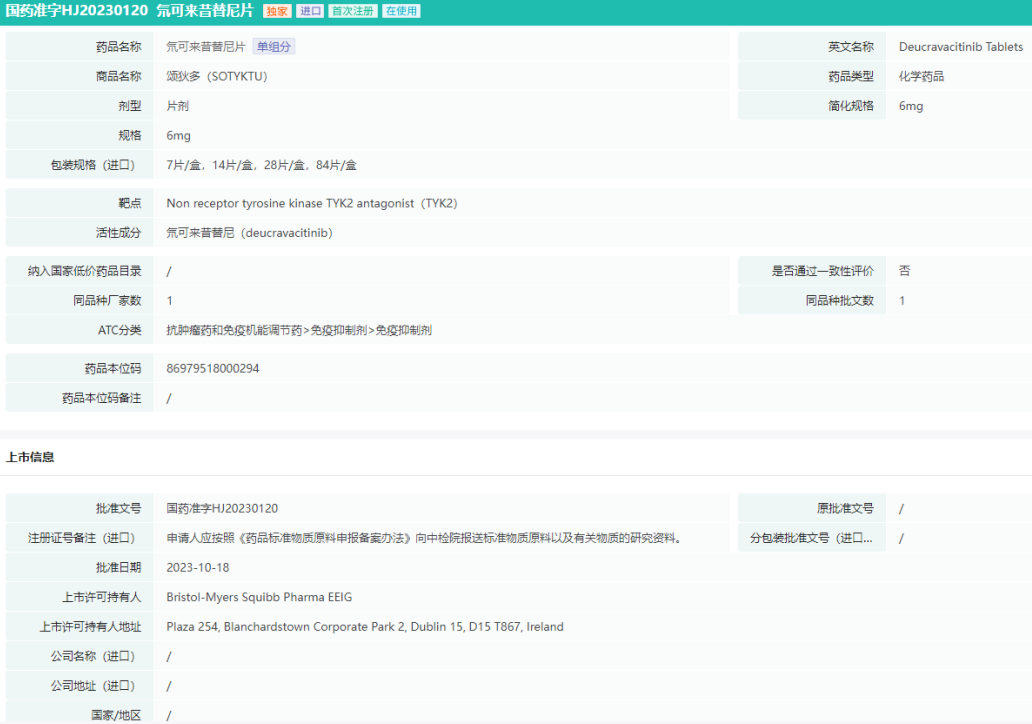
图片来源:药融云中国药品批文数据库
从疾病类型上看,斑块状银屑病是最常见的疾病类型,约占银屑病的80%-90%,其特征是界限清楚的圆形或椭圆形斑块,表面覆有银白色鳞屑,会引起皮肤干燥、瘙痒、疼痛等不适。
颂狄多是目前全球唯一获批的TYK2变构抑制剂,通过独特的“变构抑制”机制高选择性靶向TYK2,从而抑制白介素(IL)-23、IL-12和I型干扰素(IFN)这些参与银屑病发病机制的关键细胞因子的信号传导,精准靶向发挥治疗作用的同时带来良好安全性。每日一次口服,给药便捷,将为中国银屑病患者带来口服靶向治疗全新方案。
4. 健民药业1.1类小儿紫贝止咳糖浆获批上市
10月24日,健民药业的小儿紫贝止咳糖浆获得国家药品监督管理局批准上市。公开资料显示,该药品疏散风热、宣肺止咳,用于小儿急性支气管炎风热犯肺证的咳嗽,伴咳痰、汗出、咽痛、口渴,舌苔薄黄,脉浮数。
小儿急性支气管炎风热犯肺证咳嗽,是小儿常见的一种呼吸系统疾病,约占儿科门诊人数的70%至80%,约占儿科门诊呼吸道患者的24%至35%。经积极治疗,患儿多于短期内恢复,若迁延不愈或反复发作可演变成慢性支气管炎,难以治愈。该药品的上市为急性支气管炎的咳嗽患儿提供了又一种治疗选择。
5. 青峰药业奥兰替胃康片获批上市
10月24日,青峰药业的奥兰替胃康片获得国家药品监督管理局批准上市,用于治疗胃肠运动障碍型功能性消化不良。
功能性消化不良(FD)是临床常见的功能性胃肠疾病,其发病率高,且呈逐年增高的趋势。我国健康体检者(15-75岁)中,FD患病率为23.5%,平均每5人就有超过1人存在FD。FD病情容易反复,严重影响患者的生活质量,明显加重患者经济负担。
奥兰替胃康片专利信息查询
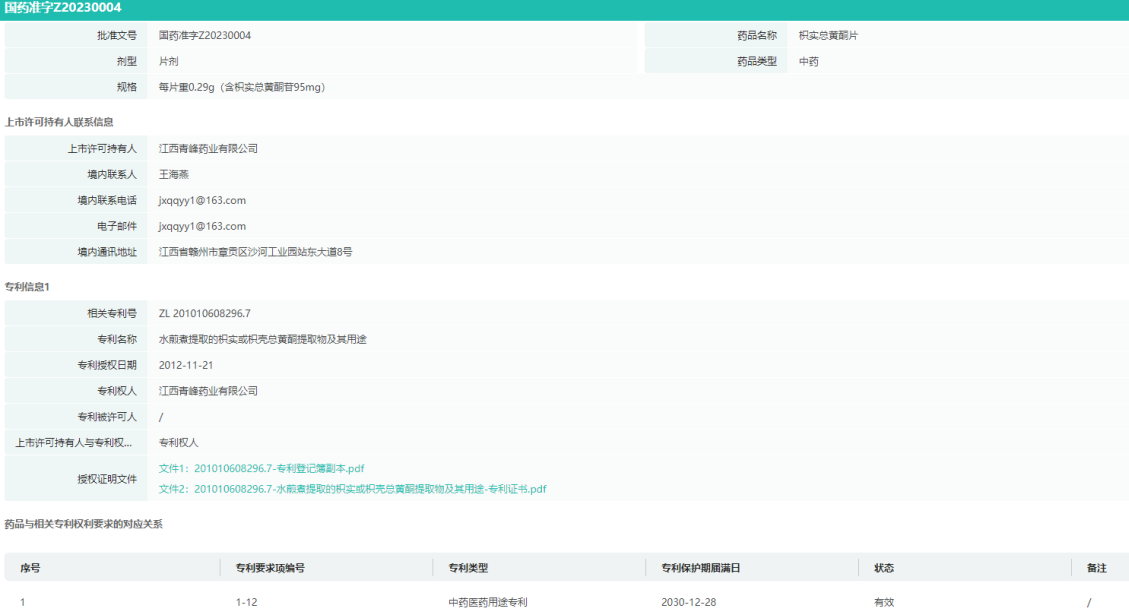
图片来源:药融云中国上市药品专利数据库
奥兰替胃康片是从江西道地药材枳实中提取的枳实总黄酮苷提取物制成的口服制剂,在治疗肝胃不和型的功能性消化不良中效果良好,可以明显减轻患者的早饱症状,同时无明显不良作用。优于西医治疗方法对功能性消化不良的治疗。
6. 石家庄以岭药业芪黄明目胶囊获批上市
10月24日,以岭药业的芪黄明目胶囊获得国家药品监督管理局批准上市,用于2型糖尿病引起的中度非增殖性糖尿病视网膜病变。
糖尿病性视网膜病变(DR)是糖尿病导致的视网膜微血管损害所引起的一系列典型病变,是一种影响视力甚至致盲的慢性进行性疾病。其中继发于糖尿病的黄斑水肿(DME)是DR中最需要治疗的部分。
在我国DR在糖尿病患者人群中的患病率为24.7%-37.5%。与美国、英国、澳大利亚、加拿大等基本相当。根据我国人口基数和糖尿病总患病人数推算,我国DR的患病人数约有1690-2120万人,DME患者约占其中的一半,但由于DME影响视力,对工作和生活影响极大,因此临床需求更为急迫。芪黄明目胶囊可以有效降低毛细血管通透性、减轻视网膜及黄斑水肿和出血,同时还有利于稳定患者血糖,遏制住单纯性病变发展成为增值性病变。
以岭药业药品审评年度趋势
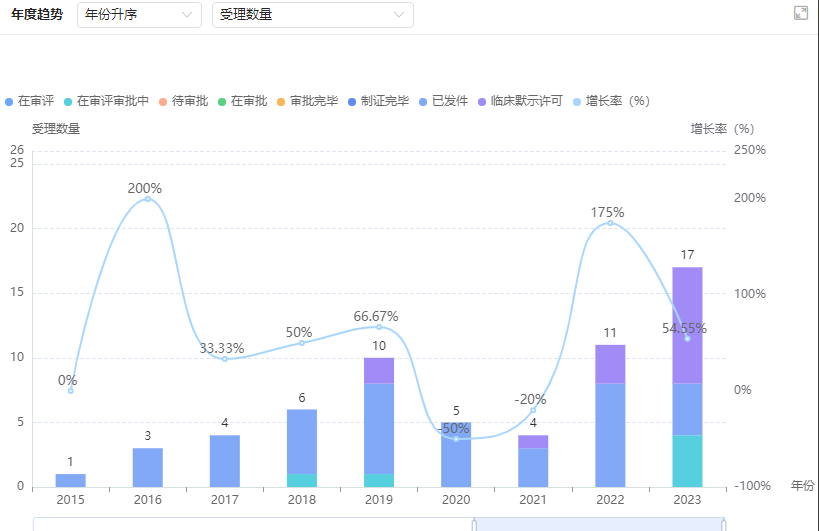
图片来源:药融云中国药品审评数据库
7. IL-1受体拮抗剂在中国获批,治疗家族性地中海热
10月31日,苏庇医药(SwedishOrphanBiovitrum,简称Sobi)IL-1受体拮抗剂安纳白介素注射液已正式获批,用于治疗成人、青少年、儿童和8个月及以上婴幼儿患者的自身炎症性周期性发热综合征(治疗家族性地中海热)。
安纳白介素是一种白细胞介素1(IL-1)受体拮抗剂,它能通过与多种组织和器官中表达的IL-1的1型受体结合,阻断IL-1的生物活性。此前,该药已经在海外获批治疗冷吡啉相关周期性综合征(CAPS)、类风湿关节炎(RA)、白介素-1受体拮抗剂缺乏症(DIRA)、COVID-19、家族性地中海热(FMF)等适应症。
<END>
药融咨询团队定期监控每月中国医药市场内发生的重大事件,帮助更多药企解决重点新药动向收集的难题,助您实时了解国内外企业在新药研发领域重要进展,快速跟踪行业发展的脉络,获取核心的新药情报信息。想要领取完整报告内容,关注“药融云”公众号,后台回复“报告”关键词进行领取。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论