
近日,阿斯利康开发的“first-in-class”AKT抑制剂Truqap(capivasertib)上市,与 Faslodex (fulvestrant) 联合使用,用于治疗激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的晚期或转移性乳腺癌成年患者。
在HR+/HER2-晚期乳腺癌中,以AKT信号通路为靶点的抗肿瘤治疗成为近几年的研究热点,并在post-CDK4/6抑制剂治疗领域中发挥着重要作用。Capivasertib掀起HR+/HER2-晚期乳腺癌治疗新浪潮,为CDK4/6抑制剂经治患者提供强有力的全新治疗选择,这也意味着AKT通路在经历了40多年的艰难探索后终于迎来曙光。
药融云数据库显示,在2023年6月,FDA已授予Capivasertib+fulvestrant的新药申请(NDA)优先审评资格,不到半年的时间,FDA正式批准意味着Capivasertib为HR+/HER2-晚期乳腺癌治疗临床实践带来了全新的突破,且作为全球首个获批的AKT通路抑制剂,具有重要的里程碑意义。
Capivasertib获批信息查询
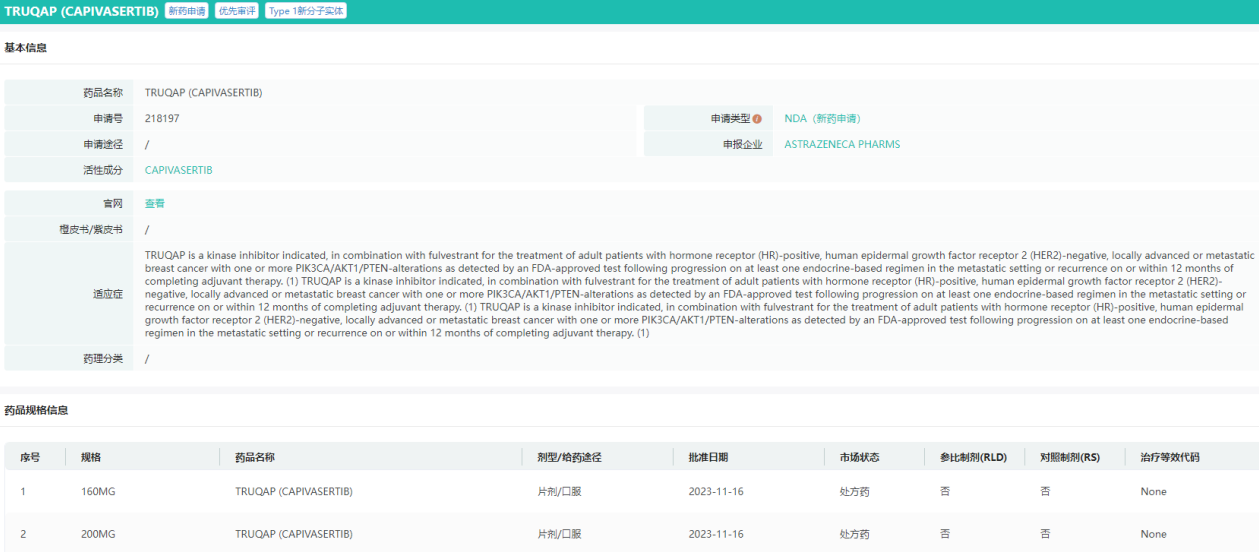
图片来源:药融云美国FDA批准药品数据库
阿斯利康肿瘤业务部执行副总裁Dave Fredrickson表示:“美国对Truqap的快速批准加强了PI3K/AKT途径在HR阳性乳腺癌中的重要作用,以及在诊断时对患者进行测试的迫切需要,因为高达50%的患者患有具有这些变化的肿瘤。作为一流的药物,这一批准为美国患有这种特定类型疾病的患者提供了一个关键的新选择,我们期待将Truqap带给全球许多乳腺癌患者,使他们受益。”
Capivasertib或成为HR+/HER2-晚期乳腺癌二线内分泌靶向治疗金标准
HR+/HER2-乳腺癌约占所有乳腺癌的70%,CDK4/6抑制剂联合内分泌治疗是不合并内脏危象HR+/HER2-晚期乳腺癌的标准一线选择,但CDK4/6抑制剂治疗进展后尚无标准推荐。近年来,靶向AKT通路的抗肿瘤治疗已成为探索post-CDK4/6抑制剂治疗策略的热点方向。
Capivasertib是针对AKT通路的强效选择性抑制剂,在III期CAPItello-291研究中Capivasertib+fulvestrant针对HR+/HER2-晚期乳腺癌疗效优异,整体健康状况和生活质量均表现良好,并且总体安全性良好,相较于现有PI3K抑制剂及mTOR抑制剂常见的高血糖、口腔炎等不良反应,Capivasertib的不良反应发生率均较低。
Capivasertib全球临床试验信息查询(部分)

图片来源:药融云全球临床试验数据库
Capivasertib是目前HR+/HER2-乳腺癌领域靶向联合内分泌治疗方案中唯一在大型III期研究纳入大量CDK4/6抑制剂经治人群且取得PFS显著获益的创新药物,极具临床应用前景。
药融云数据库显示,2023年10月10日,中国国家药品监督管理局药品审评中心(CDE)受理了阿斯利康(AstraZeneca)递交的1类新药Capivasertib片的新药上市申请。期待该药物在国内早日获批,能够惠及更多乳腺癌患者,给广大患者带来新希望。
HR阳性乳腺癌
乳腺癌是最常见的癌症,也是全球癌症相关死亡的主要原因之一。HR阳性乳腺癌(表达雌激素或孕激素受体,或两者兼有)是最常见的亚型,超过65%的肿瘤被认为是HR阳性和HER2低或HER2阴性。
2020年,超过200万患者被诊断患有乳腺癌,全球有近685000人死亡。在中国,2020年乳腺癌新发41.6万例,在女性群体中发病率已超越肺癌,登顶首位。
HR阳性乳腺癌(表达雌激素或孕激素受体,或两者都表达)是乳腺癌最常见的亚型,超过65%的肿瘤被认为是HR阳性和HER2低或HER2阴性。总的来说,基因突变PIK3CA、AKT1和变异在PTEN经常发生,影响到50%的晚期HR阳性乳腺癌患者。
全球乳腺癌药物研发TOP10企业
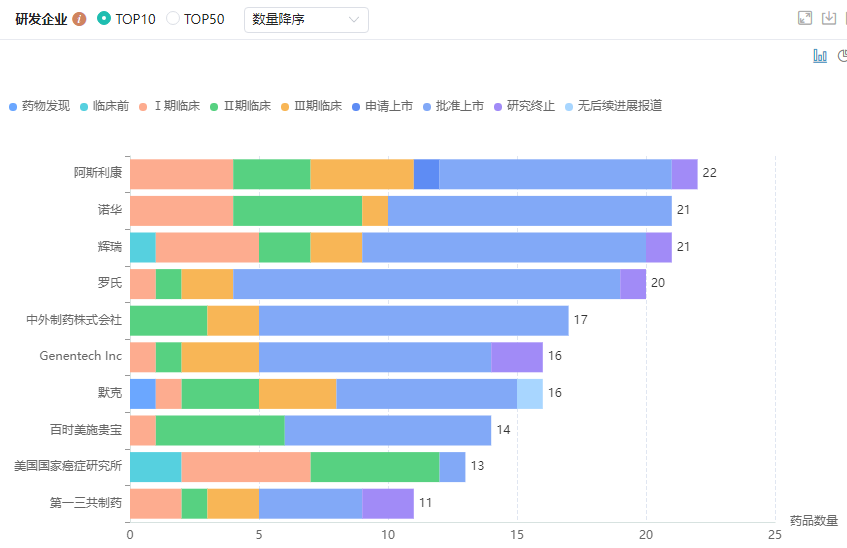
图片来源:药融云全球药物研发数据库
HR阳性乳腺癌细胞的生长通常由雌激素受体(er)驱动, 和针对ER驱动的疾病的内分泌疗法被广泛用作高级设置中的一线治疗,并且经常与CDK4/6抑制剂配对。然而,许多晚期患者对CDK4/6抑制剂和目前的内分泌疗法产生了耐药性。一旦发生这种情况,化疗是目前的有限的治疗选择,治疗存活率很低,预计30%的患者在诊断后能活过5年。
优化内分泌治疗和克服耐药性,使患者能够继续从这些治疗中受益,以及为那些不太可能受益的人确定新的治疗方法,是乳腺癌研究的积极关注领域。
关于Truqap和Faslodex
Truqap(capivasertib)是所有三种AKT亚型(AKT1/2/3)的第一种有效的三磷酸腺苷(ATP)竞争性抑制剂。Truqap目前正在接受治疗多种乳腺癌亚型和其他肿瘤类型的III期试验评估,可以作为单一疗法,也可以与现有疗法联合使用。正在进行的临床研究计划集中于依赖于通过PI3K/AKT途径发出信号的肿瘤,以及在该途径中含有生物标志物改变的肿瘤。
Faslodex上市时间轴
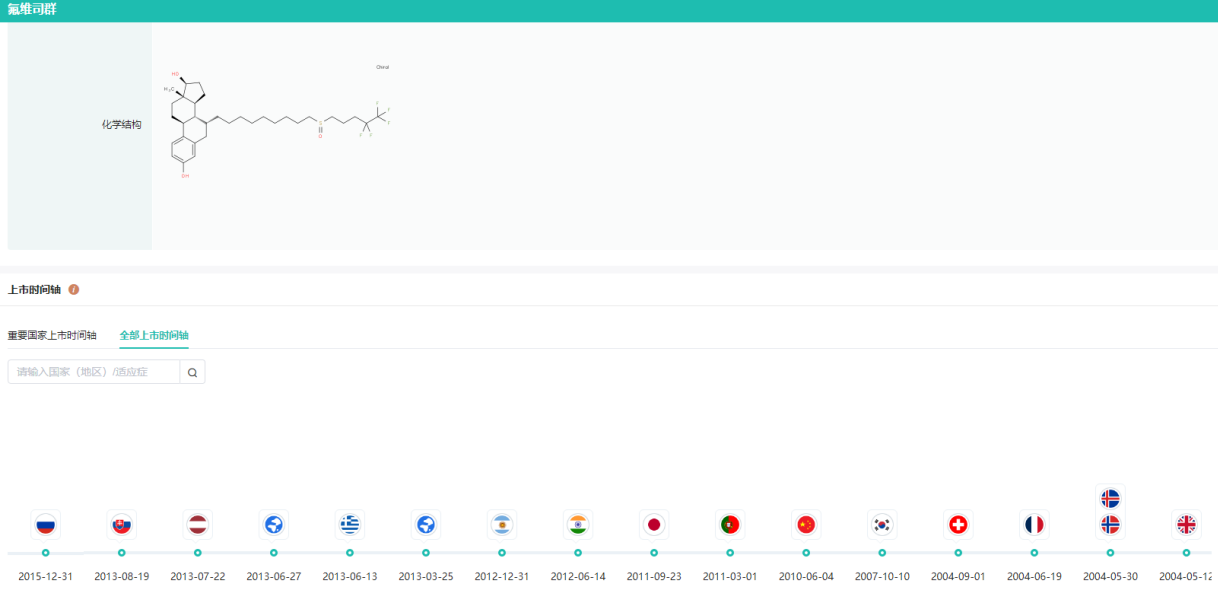
图片来源:药融云全球药物研发数据库
Faslodex(氟维司群)是一种内分泌疗法,适用于治疗雌激素受体阳性、局部晚期或转移性乳腺癌的绝经后妇女,这些妇女以前未接受内分泌疗法治疗,或在辅助抗雌激素治疗期间或之后出现疾病复发,或在抗雌激素治疗期间出现疾病进展。
Faslodex由阿斯利康发现和开发,于2002年首次获得美国食品和药物管理局(FDA)批准,作为治疗激素受体阳性(HR+)转移性乳腺癌的单一疗法。该药物还被批准作为与CDK4/6抑制剂palbociclib的联合疗法,用于治疗HR+和人表皮生长因子受体2阴性(HER2-)晚期或转移性乳腺癌患者,这些患者以前接受过内分泌药物治疗。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论