随着各类国内医药企业不断升级、转型、创立;资本不断涌入这个生物医药大健康市场;相信在若干年后,中国新芽/新药也会在全球制药市场上展露头角。随着时间推进,候选药物临床失败、上市公司股市大跌:或将成为国产新药常态。
稍微提及下今年的案例。太多失败案例只是未公开,其实已经非常多,对新药创制应该多多敬畏:
01 康乃德生物医药有限公司
近日报告了在中重度特应性皮炎(AD)成人患者中皮下注射(SC)CBP-201的国际多中心二期研究(NCT04444752)的积极顶线结果。
该研究结果显示,CBP-201达到了主要有效性终点,显著改善了从基线到第16周的湿疹面积和严重程度指数(EASI)评分的下降百分比,所有三个CBP-201治疗组(300mg 每2周一次,150mg 每2周一次或者300mg 每4周一次(Q4W))在第16周都显著优于安慰剂组,具统计学意义。对于EASI的次要终点,所有三个CBP-201治疗组,在第16周达到EASI评分较基线降低至少50%或75%的患者比例(分别称作 EASI-50和EASI-75),都显著优于安慰剂组,具统计学意义。
在其它关键次要有效性指标中,也显示出CBP-201的300mg Q2W组较安慰剂组有统计学意义的显著性改善,包括:在第16周达到研究者总体评估(IGA)为0或1分(皮损完全清除或基本清除)并且较基线改善≥2分的受试者比例,周平均峰值瘙痒数字评估量表(PP-NRS)评分从基线到第16周的变化,以及其它有效性终点。同时,研究还观察到CBP-201有良好的安全性特征,治疗中出现的不良事件(TEAE)、严重不良事件(SAE)和导致研究药物中断的TEAE的发生率, 在CBP-201治疗组和安慰剂组相似。而且,接受CBP-201的患者中,报告的注射部位反应的发生率(1.8%)和结膜炎的发生率(3.5%)都很低。
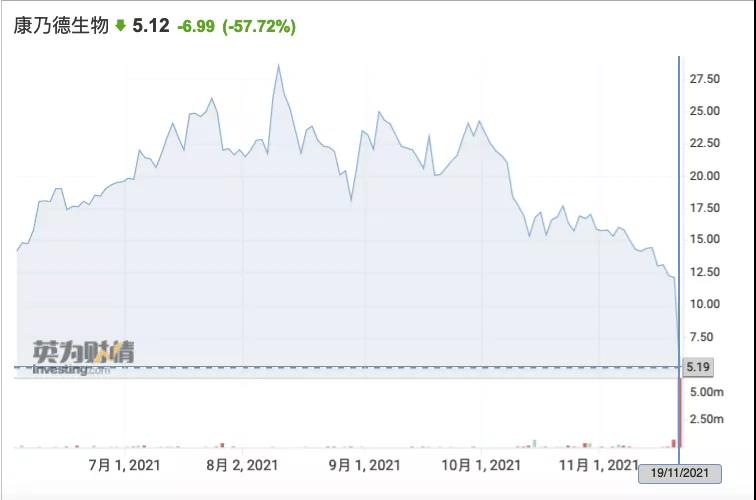
公司所认为的积极数据-消息一经发布后,该公司股价几乎腰斩。公司披露数据不完全/不充分,与强者Dupixent竞争,需展示优势数据;无法给予投资者信心。
02 2021年4月9日,康弘公司公告:
2018年5月启动关于“一项多中心、双盲、随机、剂量范围试验,评估康柏西普眼用注射液治疗新生血管性年龄相关性黄斑变性患者的疗效和安全性”临床试验项目(以下简称“PANDA试验”)。2020年9月25日,PANDA试验完成全部受试者的第36周主要终点访视。
2020年初以来,全球突发公共卫生事件、外部环境变化等不利因素对临床研究造成了极大的困难和影响。虽然公司为此追加了大量人力、财力,保留和保护受试患者以减少不利影响,努力使PANDA试验能按时推进。但公司无法在揭盲前获悉各组受试者的获益情况,实际影响更难以评估。现在已经揭盲的阶段性分析表明,全球公共卫生事件对本研究的影响大大超过公司的预期,包括各国不断出台的各种管控措施等因素使得大量受试者脱落、失访、超窗,完全符合PANDA试验给药方案的病例已逐步降低到不足入组病例的40%。特别是国际航运和出行限制的阻碍,使得需要全程冷链配送的试验药品的质量控制以及需要去医院现场临床监查和稽查,都变得格外艰难。此外,高达68个试验中心,有一半以上的受试者视力在注射后较基线变化等于甚至低于零,这与试验药物既往的临床研究以及真实世界大量的使用经验有很大差异。
2021年4月9日,PANDA试验科学指导委员会召开专题会议,基于上述环境下产生的数据进行了中期评议。委员会认为本试验在全球公共卫生事件期间,大量受试者偏离试验规定的给药方案;康柏西普在试验中表现出了良好的安全性;在亚裔人群的亚组分析中,1mg康柏西普每三个月注射一次的剂量组疗效表现可能优于整体。同时,对于试验药物和冷链供应可能受到的影响深表关切,建议开展后续的调查研究。但委员会认为PANDA试验未能达到预期目标,建议公司停止PANDA试验。
公司认为临床试验是一个复杂的系统工程,试验结果受影响的因素较多。尤其突发的全球公共卫生事件对临床试验的影响,目前尚没有任何通行的评估和矫正方法。其对PANDA试验的重大影响在目前的认知条件下更无法被充分评估。但是,综合考虑全球公共卫生事件尚在蔓延的复杂国际局势和不确定的外部环境等诸多风险,继续推进PANDA试验已经无法获得具有注册价值的结果。特别是考虑到受试患者的临床获益,和保护广大投资者利益,公司经过慎重研究,决定尊重科学指导委员会的专业评估及建议,停止全球PANDA试验。
对PANDA试验的分析和调查仍在进行中,公司会认真分析试验数据和各项线索背后的原因,并继续与各国监管机构沟通。公司将在确保有相应有效措施后,再行审慎推进后续相关工作。
总 结
此前在2017年6月,《Nature Reviews Drug Discovery》发表了一篇名为“Chinese biopharma starts feeding the global pipeline”的综述。笔者也期待中国新药未来能成为全球产品线中的主力军,虽然这需要很长时间;让我们一起见证。

参考:
NMPA/CDE;
药融云数据,www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露;
Chinese biopharma starts feeding the global pipeline,https://www.nature.com/articles/nrd.2017.94;
等等。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论