引言:在食品药品工业中,必须控制微生物的污染以及残留。医药(中药、化学药、生物药品)、食品生产中要对生产环境进行微生物控制与消杀,在终端产品也要进行微生物检测控制,所以在生产前研究以及生产过程以及使用中需要大量的微生物学验证实验数据积累,本篇文章详细介绍实验用菌种传代、接种使用与经验总结。
一、菌种获取方式
- 1.ATCC:美国模式培养物集存库(全类)→全权代理机构(资质)
- 2.CMCC:中国医学细菌保藏管理中心(医药学)→中检院
- 3.CTCC:中国微生物菌种保藏管理中心(食品)→中检院
二、相关解释信息
1.标准菌珠:是指由标准源头提供的冷冻干燥菌(中国药品生物制品检定所医学微生物菌种保藏管理中心),也就是0代菌珠。
2.储备(传代)菌种:是指用标准菌种制备的采用特定保存方法长期固定保存的菌种,用于传代及制备工作用菌种,也就是复苏后的1代培养物。
3.工作用菌珠:是指用标准菌种或传代用菌种接种至普通琼脂斜面培养后,作为日常工作使用的菌种,一般多用第1代传代后菌种作为日常使用菌种,也就是由储备菌株转种传代而来。
三、菌种与培养基及相关信息
1.阳性菌对照室:菌种复苏传代应有单独的洁净操作间,并有独立的空气净化系统,这是菌种传代必须的硬件系统。
2.控制菌相关信息如下:
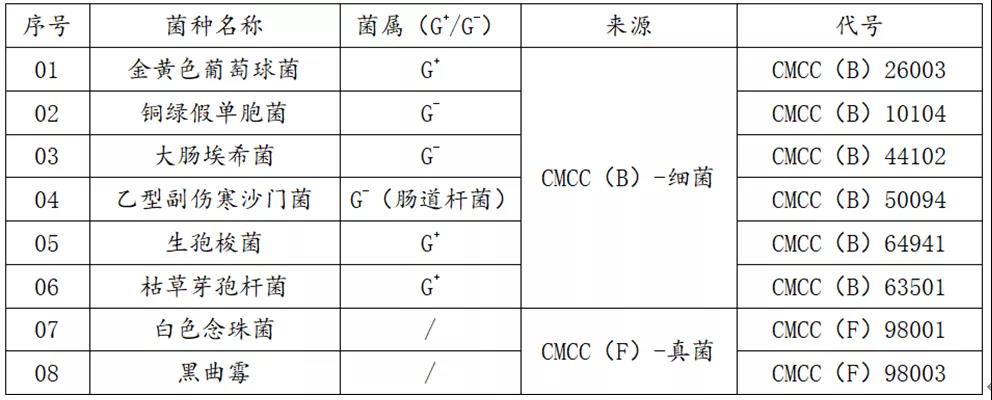
3.冷冻菌种一旦解冻转种制备工作菌株后,不得重新冷冻和再次使用;
4.工作菌株的传代次数应严格控制,不得超过5代(从菌种收藏机构获得的标准菌株为第0代),以防止过度的传代增加表型变化的风险。1代是指将活的培养物接种到微生物生长的新鲜培养基中培养,任何亚培养的形式均被认为是转种或传代一次。必要时,实验室应对工作菌株的特性和纯度进行确认;
5.微生物实验室必须建立和保存其所有菌种的进出、收集、贮藏、保存、确认试验以及销毁的记录(有了程序,就应该有配套的记录),应有文件化的程序管理菌种(从标准菌株到工作菌株),该程序包括:标准菌种的申购记录;从标准菌株传代工作菌株操作SOP及传代接种记录;菌种必须定期转种传代,并做纯度、特性等实验室所需关键诊断指标的确认并记录;每支菌种都应适当标注,注明其名称、标准号、接种日期、所传代数;菌种生长的培养基和培养条件;菌种保存的位置和条件;
6.将第3代传代菌种作为工作菌种用;
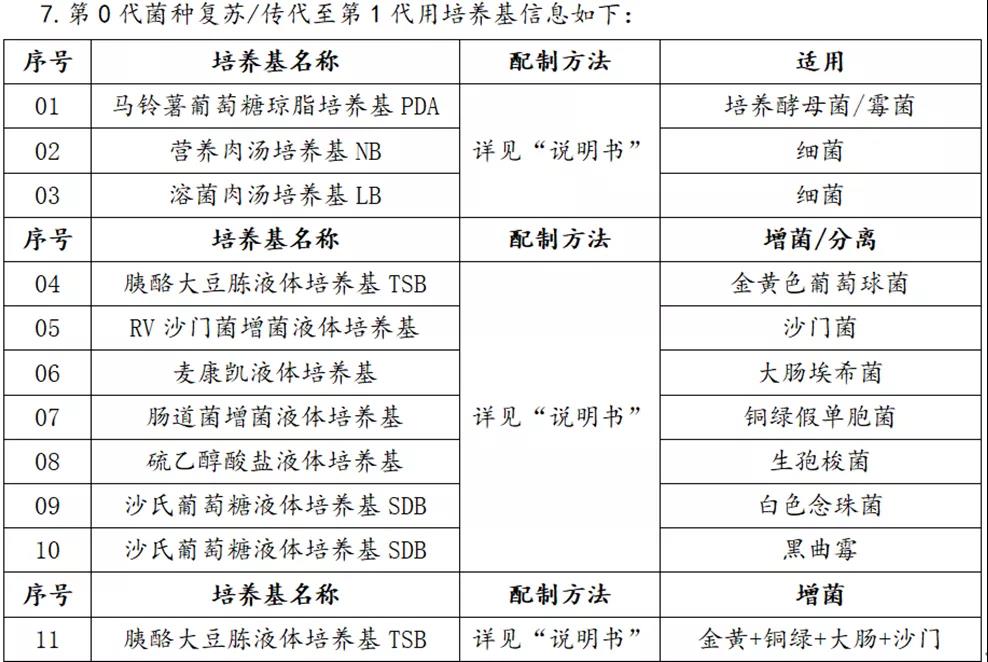
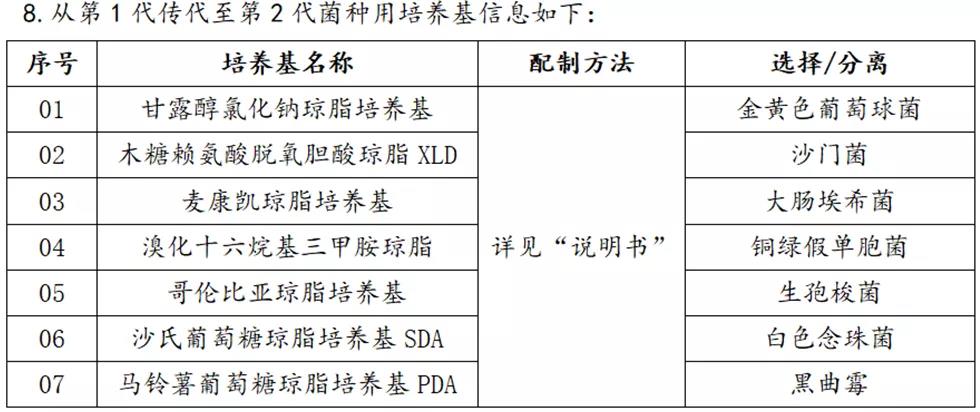
9.培养基应进行冷藏保存,且应在有效期内使用;购买回来的0代菌种应进行冷冻(-20℃),且购买回来的菌种严格按照说明书进行相关保存或处理。
四、实验耗材
生化恒温培养箱、试管、接种环、高压灭菌锅、干燥箱、酒精灯、生物安全柜、双碟、砂轮、第1代菌种(中检所)、棉布、75%酒精棉、电子光学显微镜
五、复苏/传代操作步骤
1)准备工作
1.培养基配制与灭活准备:
①配制:详见各培养基“使用说明书”(5种);
②将配制好的各相应培养基分装到50mL试管中,每管10-15mL,每种培养分装2管;
③各培养基配制好后,均应进行灭活处理(121℃高压灭活15min)满足无菌要求,制成液体/或斜面培养基备用。
2.器具灭活准备:将试管、接种环、吸管进行高温灭活。
3.将购买回来的第0代菌种(冻干)取出放置专用干燥器中进行复温到常温(30min)。
4.将复温的冻干菌种、灭菌后的器具/吸管/双碟、灭活后培养基通过传递窗转移至阳性对照室的生物安全柜中(可在传递窗中进行紫外再灭菌15min)。
2)菌种复苏与传代(第1代)操作
1.用砂轮将冻干粉菌种(第0代)安瓿颈部标点处挫5遍刻痕,用75%酒精棉将安瓿管外壁进行擦拭消毒、晾干,转移至灭菌的双碟内,点燃酒精灯,将菌粉轻弹至安瓿瓶瓶底部,用干燥的无菌纱布包住安瓿瓶,将安瓿瓶刻痕处转移至火焰旁0.5-1cm处,快速将其掰开并迅速移开,再次转移至灭菌双碟内。
2.取1支灭活的1mL无热源吸头,在火焰旁(同上)吸取相应营养肉汤(2010版)/或菌种相应液体培养基(2015/2020版)或1%无菌蛋白胨0.5-0.8mL,速速加到菌种安瓿瓶中,用吸管头或旋涡混合器进行搅拌,将冻干菌粉进行搅动使溶解制成菌悬液,并速速将菌悬液接种至相应液体培养基内,每种2管。
3.安瓿瓶先置于酒精灯进行加热灭活,再将上述吸管、棉布、安瓿瓶置于消毒液种进行灭活,最后用专用器具通过传递窗转出置于高压灭菌锅中,进行高压灭菌灭活。
4.将上述相应的培养基置于30-35℃培养18-24小时,20-25℃培养18-24小时,次日进行观察是否有菌生长,观察试管是否变浑浊(浑浊程度代表菌种生长繁殖好坏)。
5.浑浊生长良好-得到第1代菌种。
6.将第1代菌种进行包裹(双层牛皮纸+专用盒子/袋)处理后,置于专用冷冻(超低温冰箱)中,进行保存备用;“铜绿假单胞菌”室温保存。
3)传代接种(第2代)操作
1.用灭菌后的接种环蘸取第1代菌悬液,分别接种至各自培养基斜面上,进行“Z”型划线操作,每种2管。
2.具体接种操作:点燃酒精灯,左手握住菌种斜面,将管口靠近火焰旁,右手拿接种棒,将接种棒移至火焰上层进行烧红30-60秒,然后将接种棒金属部分同样在火焰上进行灼烧,往返重复灼烧3-5次,右手用无名指、小指以及手掌部将硅胶塞夹住,左手将试管管口移至火焰上旋转灼烧,右手再将硅胶塞轻轻拔开,将接种环伸入试管内先在试管管口壁靠2下进行降温冷却,稍微冷却后再移动至菌落苔上,刮取少量菌苔,随即取出接种棒,并将菌种试管口移至火焰旁进行烧3-5秒并塞上硅胶塞;左手将菌种试管放下,再用左手取相关培养基斜面1支,右手用无名指、小指以及手掌部将硅胶塞夹住,左手将试管管口移至火焰上旋转灼烧,右手再将硅胶塞轻轻拔开,将接种环伸入试管内至培养基斜面底部,由底向上,将接种环轻贴培养基斜面的表面进行曲折移动划线(“Z”型),使菌划线接种到斜面培养基表面上;取出接种棒并将培养基试管在火焰旁进行塞上硅胶塞,最后将接种过菌的接种棒在火焰上进行灼烧灭菌。
2.将上述相应的培养基置于30-35℃培养18-24小时,20-25℃培养18-24小时,次日进行观察是否有菌生长,观察斜面培养基是否有菌落(菌落应生长良好-纯度/典型菌落);如果生长不是很好,可继续培养至72小时。
3.将培养生长好的培养基取出,对每种菌种进行纯度和特性鉴定和确认,仔细观察菌落形态,查看有无杂菌,涂片,革兰氏染色镜检,如呈典型菌落后,可制成甘油冷冻管(第2代)或直接传代接种(第3代),第3代就可以直接用于日常工作检查用菌种;如发现杂菌或菌落菌型部典型,可进行平板分离单菌落。
4.生长良好-得到第2代菌种。
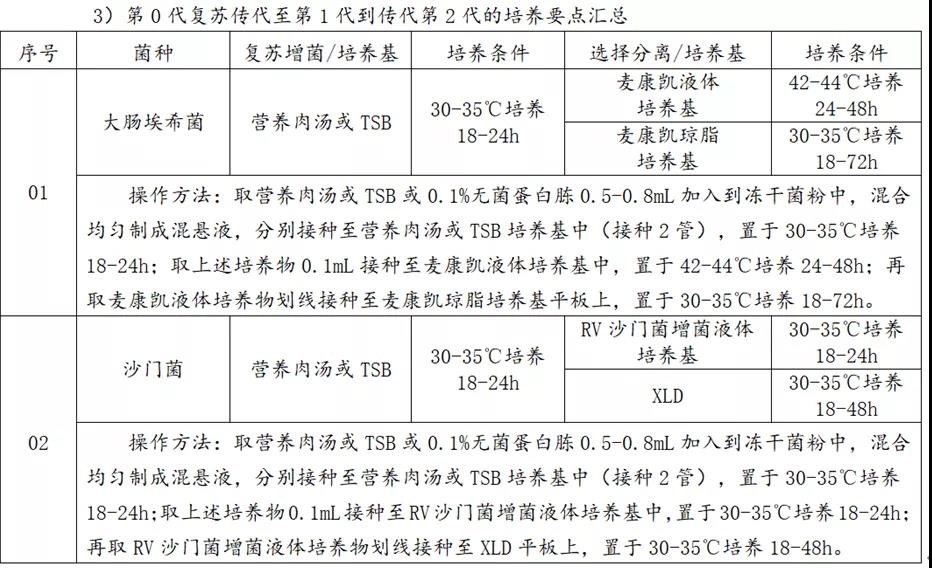
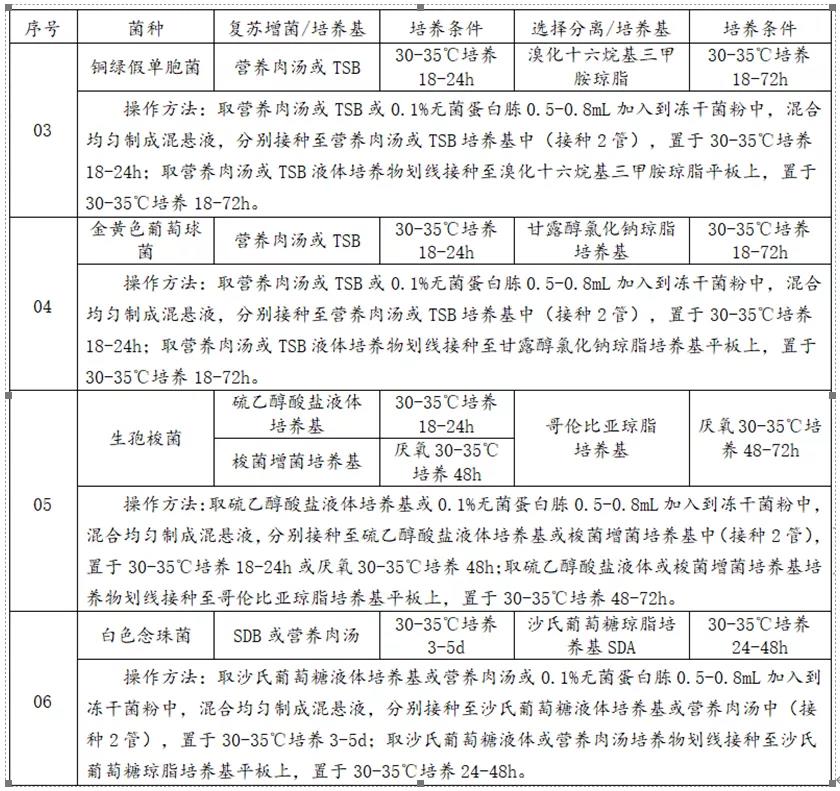
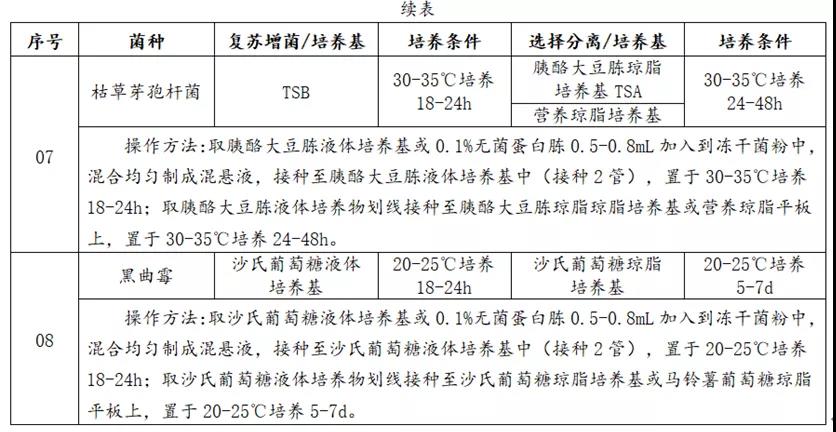
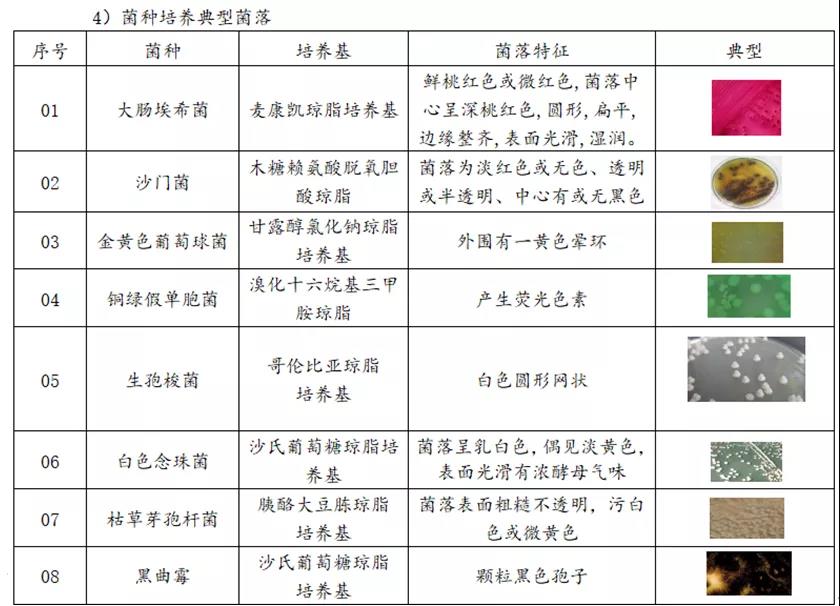
备注:TSB-胰酪大豆胨液体培养基,XLD-木糖赖氨酸脱氧胆酸琼脂,SDB-沙氏葡萄糖液体培养基,TSA-胰酪大豆胨琼脂培养基。
5)第2代菌种鉴定(镜检)操作
1.溶液制备:
①草酸铵结晶紫染色液:结晶紫2g,用95%乙醇溶解制成20mL溶液+草酸铵0.8g,用蒸馏水溶解制成80mL溶液;混合均匀,静置48h后使用。
②碘液:取碘化钾2g先用少量水溶解,再加入1g碘使之溶解,最后加水制成300mL。
③番红染色液:取(番红2.5g,用95%乙醇溶解制成100mL)10mL与80mL蒸馏水混合均匀,即得。
2.制片:在干净载玻片(用75%酒精浸泡)上滴上1滴蒸馏水,用干净灭菌的接种环挑取少许第1代或第2代新鲜培养物,置于载玻片上水滴中,用接种环与水磨合混合制成混悬液并涂片成直径大约1cm的薄层(保证菌液不要过多)。
3.干燥固定:将制作好的涂片置于酒精灯上方3-5cm高处,进行移动式微加热使水分蒸发,切记不要靠近火焰或加热时间过长,将标本烤枯变质(能自然晾干最好);再次将载玻片靠近酒精灯,标本向上,在酒精灯外焰尽快的来回通过3-5次,约2-5秒钟,并间断将载玻片进行降温(湿抹布),加热温度不要超过60℃,标本固定后放置冷却至室温。
4.染色处理:①滴加1滴草酸铵结晶紫染色液进行静置染色1分钟,用蒸馏水冲洗轻轻冲洗至无颜色为止;②再加碘液静置染色1分钟,用蒸馏水冲洗轻轻冲洗至无颜色为止并用吸水纸吸干;③将标本载玻片倾斜,滴加95%乙醇进行脱色(脱色洗至流下的液体中无紫色为止),然后水洗;④滴加番红染色液1-2滴,静置染色30分钟,水洗,用吸水纸吸干或烘干。
5.将处理好的标本载玻片置于显微镜的载物台上,进行对光、调焦镜检:
5.1低倍镜观察:光线调弱,进行发现目标确定部位;
5.2高倍镜观察:光线调强,使用细调焦旋钮调节物镜,将目标物调到清晰;
5.3油镜观察:亮度调到最大,光圈完全打开,盖玻片上滴加1滴香柏油,降低镜筒并从侧面仔细观察,直到油镜浸入香柏油并贴近玻片标本,然后用目镜观察并用细调焦旋钮抬升镜筒,调到清晰标本。
6)传代接种(第3代)操作-工作用菌种(制备菌悬液)
1.用灭菌后的接种环蘸取第2代菌种,分别接种至各自培养基斜面上,进行“Z”型划线操作,每种2管,其中1管用于接种第4代,另1管用于检查用。
2.具体接种操作:详见上述方法。
3.制备与培养:
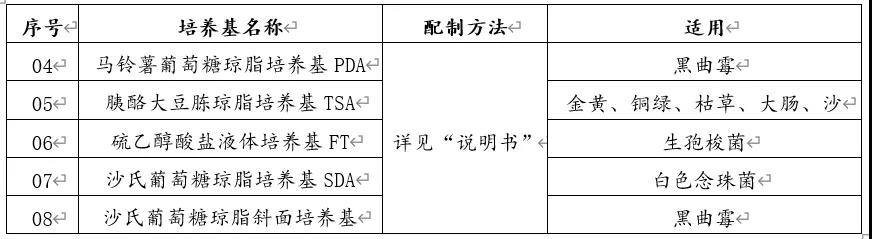
六、菌种销毁与灭活
先用消毒液进行灭菌,再用高压灭菌锅进行灭菌灭活,并进行相应记录。
总结:整个操作过程中要注意个人防护,要做到随时进行消杀处理。
<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论