我们在做药物的分析检测时,有时候发现样品的检测结果不重复,特别是有关物质检测中杂质的检出量较大时,现象更明显,杂质忽大忽小,没规律,在排除误差(如仪器误差、人为误差、方法误差)外,还有一个原因,就是样品本身不稳定,杂质升高或者降解了。出现样品不稳定的原因有很多种(我在这里说的不稳定,是指在样品的正常的检测过程中的不稳定,不包括影响因素和强制降解的杂质,因为影响因素和强制降解是在非正常的条件下进行的试验,不属于正常检测样品的范畴),如何在复杂的种种不稳定因素中快速找到“靶点”并进行解决,现进行如下解析。
一、寻找不稳定的因素
样品不稳定,某些情况下是对某特定因素不稳定,当我们接到一个新的项目的时候,在前期文献的调研过程中,能发现一些端倪。譬如,从样品的说明书中找线索。如果药品说明书上的贮藏条件显示“遮光,密封保存”表明本品对光比较敏感;说明书上显示“本品在冷处2~8度贮藏”表明本品对温度比较敏感,不耐高温;说明书上显示“本品需密封保存”表明本品对湿度比较敏感。有时候还可以从各国药典的检测方法中找线索,如“称取本品,置棕色量瓶中……”,暗示本品对光比较敏感,又譬如“取本品,置冰水中超声”,暗示本品对温度比较敏感,在常温或者高温下不稳定,“取本品,研磨后立即检测”,暗示本品可能有引湿性,当初次接触到这些信息的时候,脑海中对本品大致有个宏观的了解,在开发方法的时候,就会有针对性的进行研究。
二、确定不稳定因素
由于样品对某个特定因素的不稳定,可能引申出在实际的样品的检测的过程中,样品本身的不稳定,这就提到我们前面说的样品的检测结果不重复,忽大忽小,没规律,如何快速判断样品是否稳定,大家一般想到的是做溶液的稳定性,按照常规操作,配制一份样品,于不同的时间点进针,然后各个时间点所得的数据和0小时进行对比,通过检测样品的变化率来判断样品是否稳定。在这里需要特别强调的是,仅通过测供试品的稳定性是不够的,还需要测加标(100%加标和50%加标)溶液的稳定性,我们以甲钴胺的溶液稳定性进行对比研究。
供试品溶液的配制:取甲钴胺原料约20mg,精密称定,置100ml量瓶中,加溶剂适量超声使溶解,并用溶剂稀释至刻度。分别于不同的时间点进样检测,测得结果见下表:
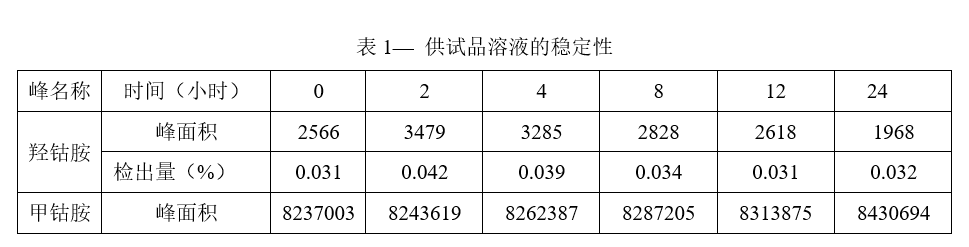
单纯从以上结果来看,甲钴胺及降解杂质羟钴胺的检出量的变化在±0.01%范围内波动,认为溶液在24小时内是比较稳定的,但是这个数据能证明本品比较稳定吗?看另个例子。
100%加标供试品溶液的配制:取甲钴胺原料约20mg,精密称定,置100ml量瓶中,加溶剂适量超声使溶解,加杂质贮备液1ml(取羟钴胺杂质约1mg置10ml量瓶中,用溶剂稀释至刻度),用溶剂稀释至刻度。测得结果见下表:
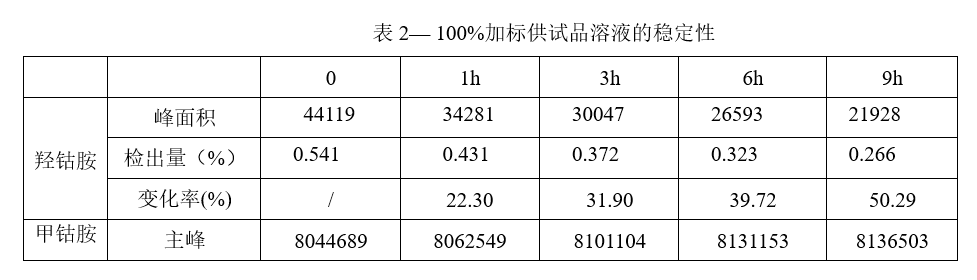
从这个例子,可以得出完全相反的结论,甲钴胺在1小时时,峰面积的变化率超过20%,已经不稳定。为什么同是做稳定性,得出相反的结论呢?主要的原因是供试品溶液中甲钴胺的杂质检出量比价小,在杂质很小的检出量的情况下,杂质量变化非常小,给人一种假象。但是如果考察100%加标溶液或者50%加标溶液的稳定性的话,样品的稳定性能很直观表现出来,更能反映出样品的稳定的情况。因此,我们在考察样品的稳定性的时候,不仅需要考察样品的稳定性,还一定要考察100%加标供试品溶液或者50%加标溶液的稳定性。
三、解决不稳定因素
确定样品溶液不稳定了,就要去解决问题,我一般从以下4个方面入手。
1.降低进样室温度
原因很简单,降低进样室的稳定,能够减缓样品的稳定性。举例如下:
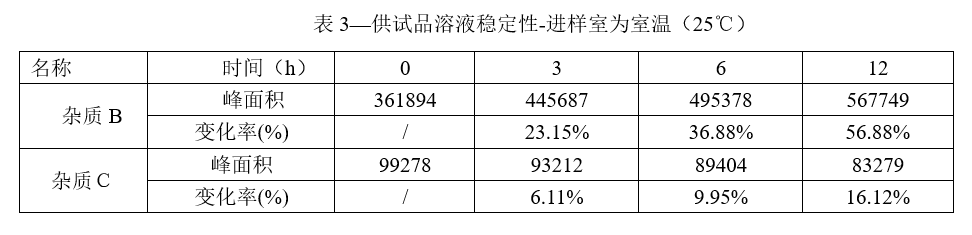
从以上数据上看出,在室温(进样室稳定25℃)条件下,在3小时下,供试品溶液中杂质B峰面积变化率为23.15%,至12小时时,杂质B变化率快速增长为56.88%,证明本品在常温条件下极不稳定。因此,将进样室的温度调整为4℃,进一步考察本品溶液中的稳定性。
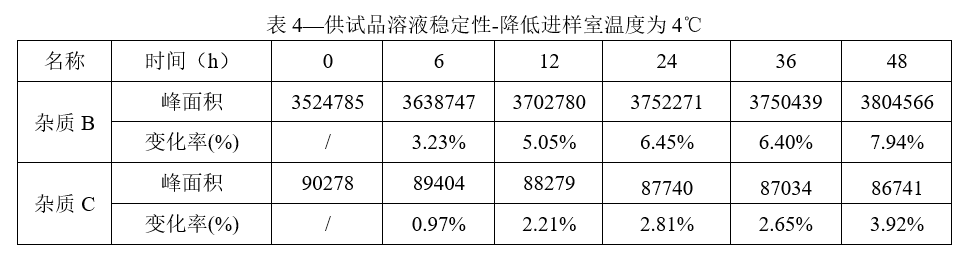
从以上数据上看出,降低进样室稳度为4℃,放置48h内,杂质B峰面积的最大变化率为7.94%,小于20%,认为供试品溶液在4℃进样室放置47小时是比较稳定的,这样能保证在检测周期内,样品是稳定的。
需要在这里说明的是,只是延缓了样品的稳定性,在检测周期内样品是稳定的,不能阻止杂质的降解。
2.优化溶剂
盐酸莫西沙星氯化钠滴眼液的有关物质的测定,配置后的溶液在室温条件下不稳定,降低进样室的稳定,效果也不很理想,为了提高工作效率,溶剂中增加稳定剂。
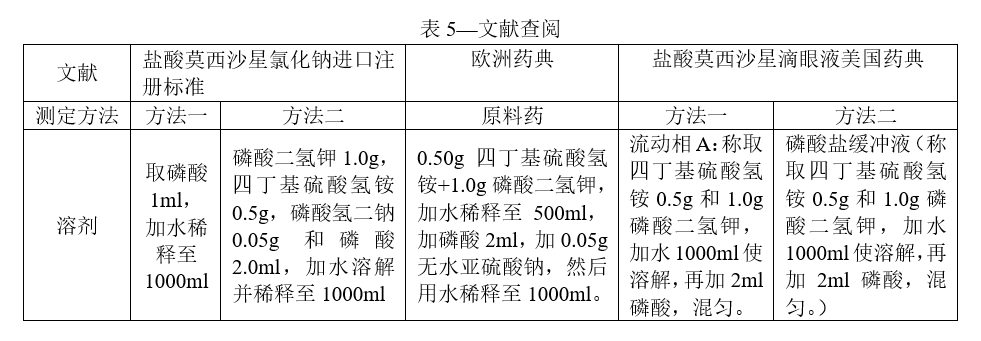
通过查找各种文献,发现欧洲药典原料药检测方法中,溶剂中增加了无水亚硫酸钠,无水亚硫酸钠的作用是保护对氧敏感的杂质,实际上起到一个保护的作用,因此,我们可以借鉴原料的溶剂的方法,在制剂的溶剂中增加无水亚硫酸钠,其他组分保持不变。最起码能在24小时,在整个的检测周期内,保证样品是稳定的。
3.优化配置方式
我们在做软膏制剂的时候,由于基质的存在样品往往比较黏稠,这样导致样品不易溶解,当样品
不稳定的时候,给分析检测带来一定的难度,我们可以借鉴其他软膏的溶解方式,譬如, 降低溶液浓度,相当于减少基质的称样量,减缓基质的干扰,对于对温度比较敏感的制剂,可以在超声仪中加入冰块,冰浴超声,虽然降低温度,很大可能会导致溶解的速度更慢,但是由于保证了较低的温度,会增加对温度敏感的杂质的稳定性。
4.改变环境
对于对光照比较敏感的样品,常规的方法是用棕色瓶配置样品,将配置好多样品溶液至于避光的进样室放置,或者装上有遮光效果的窗帘,或者将分析室的白炽灯换为比较柔和的红灯。
5.临用新制
就是现配现进。当样品本身比较特殊,各个杂质在溶剂中不稳定,以上种种措施均无效的时候,往往采用这种方法。需要说明的是临用新制的劳动成本太高,从仪器的使用和人员配置和工作效率来讲,成本也大,到了万不得已的情况下,选此下策。在写这篇文章之前,我特意翻了一下中国药典2020年版,好家伙,品种还真不少,如马来酸氟伏沙明及片、贝诺酯及片、去羟肌苷及制剂,头孢他啶……等等,有几十个品种之多,我相信随着科技的发展,随着技术的进步,人类一定有能力突破这道大难关。
相关阅读:
聊聊“对照品与供试品溶液稳定性考察”这回事!
药物分析中极性物质的保留方案(3种液相色谱法)
参考文献
[1]2020年版《中国药典》二部
<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论