
BFS(Blow/Fill/Sesl)机器是由德国工程师Gerhard Hansen发明的,技术及其设备的运用始于20世纪60年代德国Rommelag(罗姆莱格)公司。后来,在美国和意大利等相继推出这一技术设备产品。我国BFS技术设备在研制开发和应用方面有近20年的历史,吹灌封技术是一种常见的包装密封技术,通常被用于食品,药品和化妆品等行业的包装中……

图1为BFS完成吹灌封一体化的大致流程图
一、BFS在医药行业中的应用
无菌制剂是指采用无菌操作方法制备不含任何活的微生物繁殖体和芽孢或采用物理化学方法杀灭所有活的微生物繁殖体和芽孢的一类药物制剂。药融云数据库显示,在制药行业,目前BFS技术主要用于终端灭菌和非终端灭菌无菌液体制剂的生产,如滴眼液、吸入剂、小容量注射剂、大容量注射剂、口服制剂等……
BFS技术是指通过一体化设备将塑料粒料加热挤出,在同一设备内完成容器的吹塑成型,药品灌装及容器封口且能提供无菌保障的自动化生产技术。其生产线集制瓶、灌装、封口三个工艺步骤于一体,也叫做“三合一”技术,是无菌制剂灌装线的一种,可用于无菌液体制剂和无菌半固体制剂的生产。BFS技术在制药领域可满足0.1ml-1500ml容量的无菌生产,具有在线清洁(CIP)和在线灭菌(SIP)功能。[CIP(Clean in place):在不拆卸设备或元件的密闭条件下,用一定浓度的清洗液对被清洗的表面进行强力作用,从而使物料接触的表面得到清洗的方法,SIP(Sterilization in place):在密闭的条件下不拆卸设备和任何元件,用一定温度和浓度的杀菌物质或蒸汽热水,对物料接触的表面进行杀菌,从而达到预期杀菌效果的一种方法]。上世纪80年代末期,BFS开始引进中国,目前国内在大容量注射剂生产,小容量无菌液体制剂生产等方面,已积累丰富的应用经验。
在选择BFS之前有些问题是需要我们考虑的,什么样的医药产品适合使用BFS?应该注意那些问题?无可厚非,BFS是目前为止无菌保障水平最高的无菌生产工艺,其常用的塑料粒子为聚烯烃,该材料的化学性质比较稳定大多数产品在包材相容性这块问题不大。(不同厂家质量参差不齐需多厂家筛选评估其包材质量)。对于眼科和呼吸类的产品,用于BFS生产的大多数为单剂量,可挤压性和灵活性对临床给药很重要,对于该类型的医药产品低密度聚乙烯(LDPE)的使用占主导地位。对内包装的要求偏向于储存功能的产品来说,强的耐化学性和强的屏障功能(水蒸气渗透性和气体渗透性)就显的格外重要。聚烯烃虽有良好的水蒸气阻隔性,但其气体渗透性有所不足,倘若产品对氧气或其它气体高度敏感,是满足不了其需求的,需要额外的屏障加以保护(通常使用二次箔包裹),BFS虽说是一种无菌灌装技术,但在注射液产品中《化学药品注射剂灭菌和无菌工艺研究及验证指导原则(试行)》明确规定按照灭菌决策树执行,这就要求如果产品能用过度杀灭法,包装材料就需要使用PP(聚丙烯)材质。对于医药产品在BFS中的应用,要综合考虑产品的理化性质及其设备本身的属性加以判断。
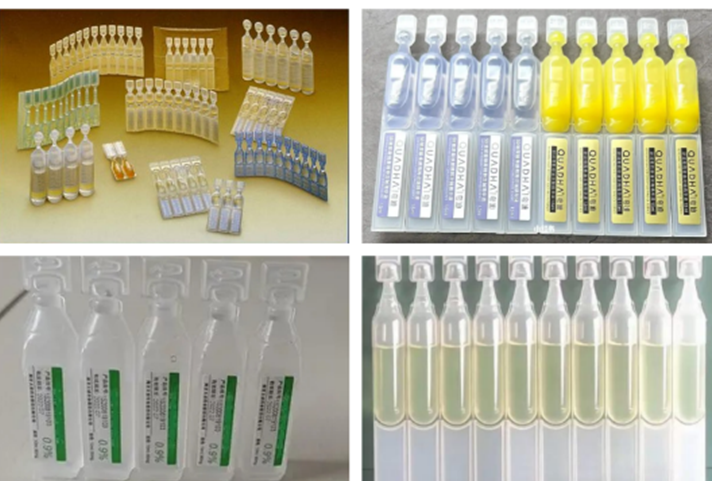
图2为用BFS仪器生产的部分产品
二、BFS无菌灌装工艺的大致流程
吹灌封技术可以在受控环境下在一台单机上完成成型、灌装并封口。整个工艺过程在无菌层流空气的保护下完成,工艺过程中,药液暴露于生产环境中的时间很短暂,减少了人为干预,从而降低了微生物污染和外来颗粒物带来的风险。用于生产非最终灭菌产品的吹灌封设备自身应装有A级空气风淋装置,人员着装应当符合A/B级洁净区的式样,该设备至少应当安装在C级洁净区环境下。在静态条件下,此环境中的悬浮粒子和微生物均应达到标准,在动态条件下,此环境中的微生物应达到标准。用于生产最终灭菌产品的吹灌封设备至少应当安装在D级洁净区。
BFS在生产操作过程中不需要过多的人为干预,是先进的无菌技术之一,其设备分为开放式型胚和封闭式型胚两种类型。开放式型胚采用的是传统的生产方式,其通过旋转模具方式将熔化的塑料粒子注入磨具内,在型胚的挤出工位,挤出机挤出型胚,熔融的塑料粒子被除菌过滤的气体(称为支撑气体,气体通常通过挤出头吹出)吹入塑料型胚的内部减少了其塌陷的风险,当仪器识别到型胚的长度合适时,主模具合模夹持着型胚,容器主体的形成是通过模具真空成型的,容器主体形成的同时,型胚被切断。此时,模具快速移至到灌装工位,芯轴向下进入到容器内部,待灌装产品被注入到容器内后,芯轴向上离开模具,最后由模具上部(密封磨具)对其进行封口处理合膜成型,灌装及封口的容器脱模,成品完成。封闭式型胚与开放式型胚的主要区别在于BFS循环之间有无型胚的切割,其吹制-灌装-密封的步骤相同,封闭式型胚已最低程度降低了人为干预和环境带来的污染风险。
常用于吹灌封生产的塑料粒子材质有LDEP(低密度聚乙烯),HDPE(高密度聚乙烯)和PP(聚丙烯)不同厂家的塑料粒子质量差异很大,选择合格的塑料粒子很关键,塑料粒子的选择包括但不限于下面几点要求:①阻隔性能②加工工艺特性③与包装产品的相容④灭菌耐受性等……综上可知,吹灌封技术主要的工艺步骤大致可分为:①挤出成型②灌装③密封和模具打开,开放式型胚和封闭式型胚在部分操作步骤会有些许不同,研发人员及药品生产企业需要结合需要生产产品的属性合理的去选择相应的模具。
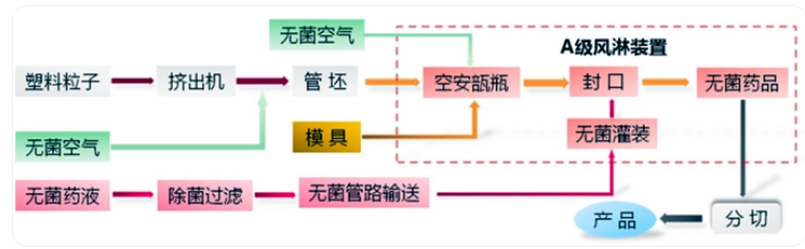
图3为BFS生产工艺流程图
三、BFS无菌灌装工艺的优势
①BFS设备在无菌状态下自制容器无需对容器进行清洗和灭菌,节约工艺用水和能源。
②采用模块化设计,占地面积小,生产过程能耗少,BFS无菌灌装工艺的综合生产成本并不比传统无菌灌装工艺高,但产品质量和综合经济效益要大大的高于传统的无菌灌装工艺。
③BFS设备可在计算机程序控制下自动完成在线清洁和在线灭菌,并且结果具有重现性且安全可靠。
④BFS设备可实现无菌灌装,不需要高温灭菌,产品质量稳定,只要更换不同的模具就可适用多种形式无菌产品的灌装和多种无菌容器的生产。可根据客户的需求设计不同的包装头部结构,以方便临床使用。
⑤相比于其它无菌灌装线玻璃包装的产品来讲,用于玻璃包装的产品需要更高的材料运输成本且需配备更加完善的运输体系(至少两层包装,以防止玻璃的破裂,从而增加了运输成本及人员成本),用于安瓿瓶包装的注射剂在熔融灌封时安瓿瓶中易产生负压,会导致在临床用药时空气中的悬浮粒子等推入瓶中进而污染药液。
四、总结
作为药品研发机构要充分的认识了解在研产品,结合本身的一个实际情况合理的去评估在研项目的风险点,衔接好药品,包装和生产线这三道防线。结合参比制剂及药厂包装生产线自身的情况合理的决策立项的一个问题。在这里需要提醒一点的是倘若参比制剂为美国,研发人员对包材的选用方面就要留意下,因为美国大多注射液不会采用玻璃安瓿(可能原因是熔融灌封时瓶内会形成负压,临床用药折断瓶口会有引进玻璃碎屑的风险存在)。这也就提醒研发人员有可能玻璃包材从相容性这块考虑也是合适的,需要我们期前做些研究去验证该想法,也不至于因为药企没有BFS的生产线就否定了该项目的立项,站在公司的角度考虑这点是得不偿失的。
BFS设备自带A级风淋装置为吹塑,灌装和封口区域提供A级洁净空气保护,确保输液生产过程在无菌条件下生产,杜绝微生物污染。与传统输液生产工艺比较,吹灌封设备在同一模块内连续完成容器的吹塑,药品灌装及容器封口三个工序,同时采用独立的空气净化系统,保证产品暴露区域无菌,从而达到有效控制污染与人为干扰,提高药品生产的安全性,是未来溶液制剂工艺发展的必然方向,无论对企业的制造水平,还是行业进一步发展都有重大意义。美国,日本和欧盟也有相当完善的法规体系用来指导设备的选型,安装和操作,同时也间接证明了BFS也是未来无菌灌装工艺生产无菌产品的一种发展趋势。
文章一开始简要介绍了BFS整个发展历程和在医药行业领域的运用,使读者对BFS有了初步的认识,随后从工艺流程方面和其相对于传统无菌生产工艺的优势方面做了详细介绍,以便研发人员对BFS有更加清晰的认识。最后,结合自己的研发浅谈了下相关产品在立项时的关注点,分析了BFS未来在医药行业的发展趋势,旨在为医药研发人员对BFS有一个合理,正确且清晰的认识。
路虽远行则将至,事虽难做则必成!
参考文献
【1】《采用吹灌封(BFS)技术生产无菌产品通用技术要求》
【2】《吹灌封(BFS)技术的无菌药品包装系统质量控制指导原则》
【3】吹灌封(BFS)一体机结构形式及无菌保障
【4】吹、灌、封(三合一)设备及其无菌灌装工艺探讨
【5】化学药品注射剂灭菌和无菌工艺研究及验证指导原则(试行)
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论