
在过去二十多年,生物制剂在治疗各种I&I(炎症和免疫学)适应症方面变得越来越普遍,目前仍然是核心治疗方法,据统计,生物制剂占I&I产品收入的近90%。Dupixent(度普利尤单抗)是针对自免疾病获批疗法中比较成功的一个例子,由再生元开发,赛诺菲与其合作共同销售,自2017年获批用于治疗AD(特应性皮炎)以来,已获批用于多个适应症,预计2031年销售额将达到210亿美元的峰值。Apogee Therapeutics的APG777是与Dupixent具有同类型适应症的研发产品,目前正在针对特应性皮炎和哮喘进行研发,虽然刚完成临床试验1期研究,但是作为Apogee Therapeutics进展最快的一条产品管线,可谓承载着公司全部的寄托,无惧披风斩棘的Apogee Therapeutics居然还是个“毛头小司”。
从药融云数据库获悉,Apogee Therapeutics(以下简称Apogee)由Paragon Therapeutics推出,Paragon Therapeutics致力于开发用于免疫和炎症性疾病的生物制剂,旗下有Apogee Therapeutics、Spyre Therapeutics和Oruka Therapeutics三家子公司。Apogee Therapeutics是一家推进用于治疗AD(特应性皮炎)、COPD(慢性阻塞性肺病)以及相关的I&I(炎症和免疫学)适应症的差异化生物制剂的的生物技术公司。公司的抗体项目旨在通过靶向完善的作用机制并结合先进的抗体工程来优化半衰期和其他特性,从而克服现有疗法的局限性。
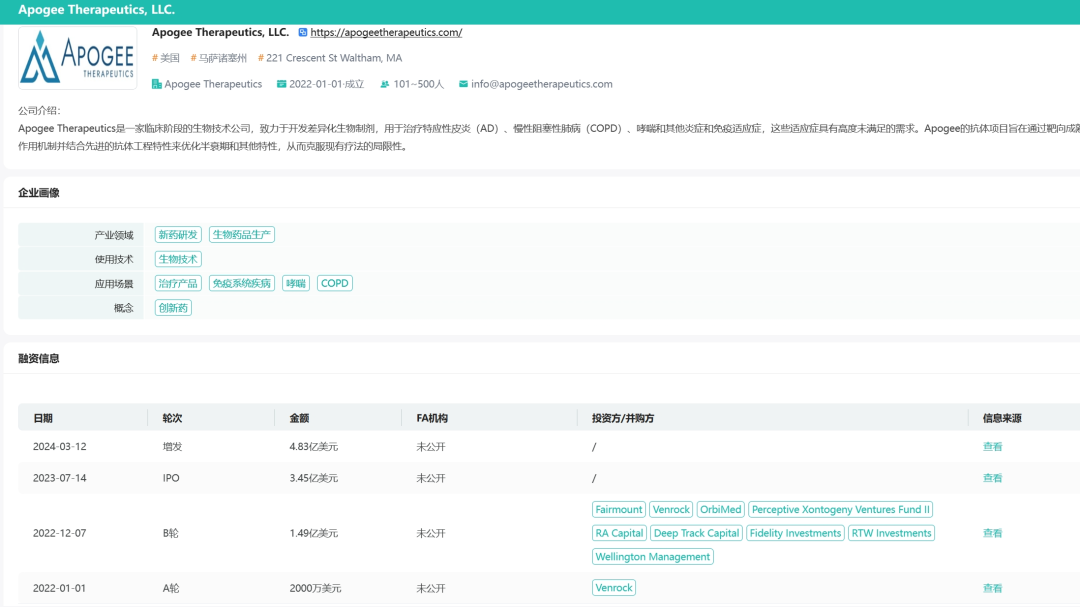
药融云数据库:融资信息
Apogee由Fairmount Funds和Venrock Healthcare Capital Partners于2022年创立,创立当年筹集了1.69亿美元的融资,其中包括由Deep Track Capital和RTW Investments领投的1.49亿美元的超额认购B轮融资。2023年7月,Apogee在成立的18个月通过IPO上市,公司也从此次发行中获得总收益约3.45亿美元。2024年3月12日,距离上次IPO不足一年,Apogee再次宣布大规模公开募股,此次筹集资金4.83亿美元。虽然公司目前的产品管线均处于临床研究以及开发阶段,但是在资本寒冬下,如此规模的筹资似乎在诉说其不可忽视的潜力。截至2024年4月16日,Apogee市值29.09亿美元。
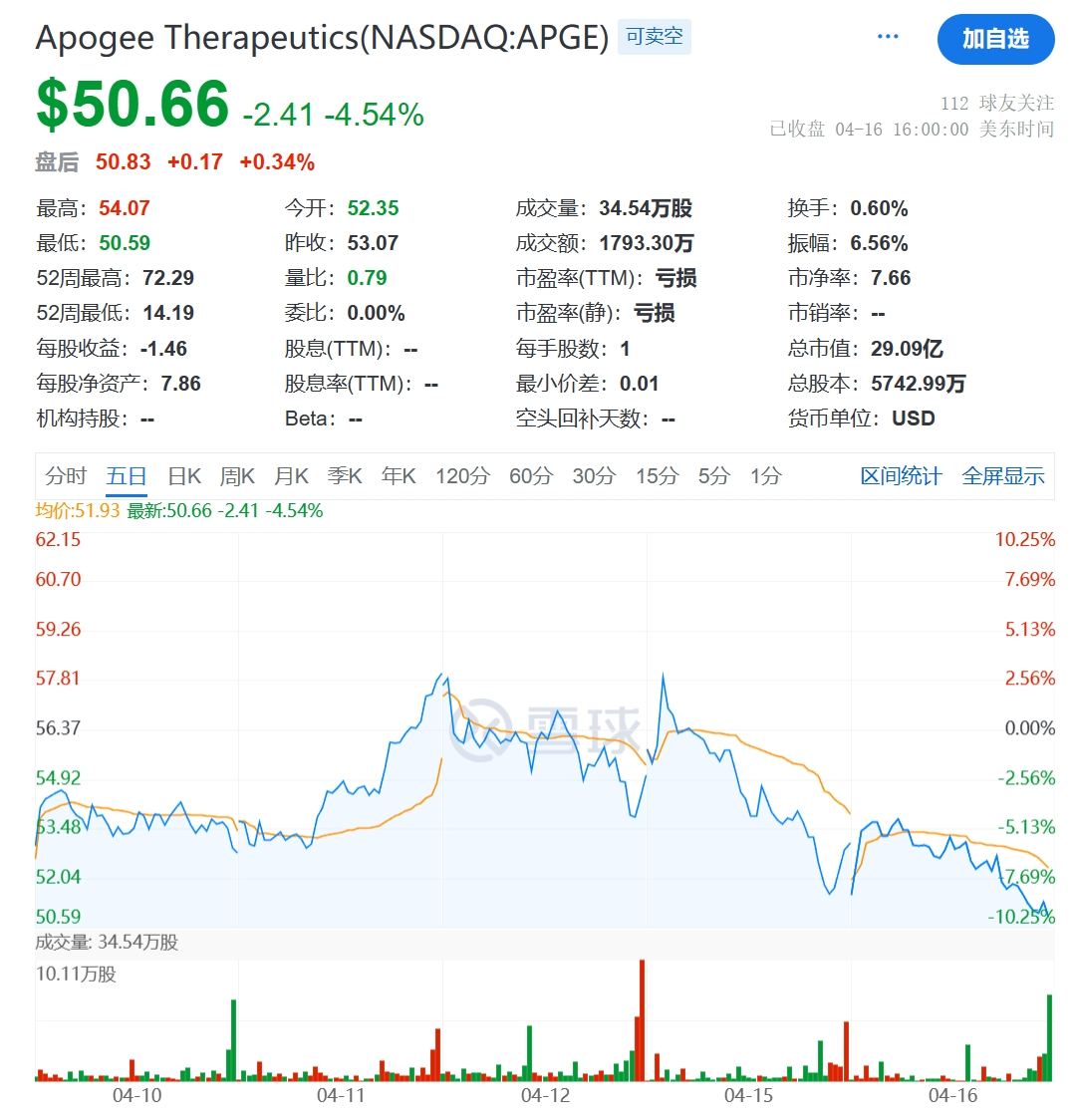
公司市值(截图)
一、研发管线
Apogee有四条研发管线,其中只有APG777和APG808已进入临床,目前针对的适应症有特应性皮炎、哮喘和慢性阻塞性肺病。以下是各管线具体进展情况:
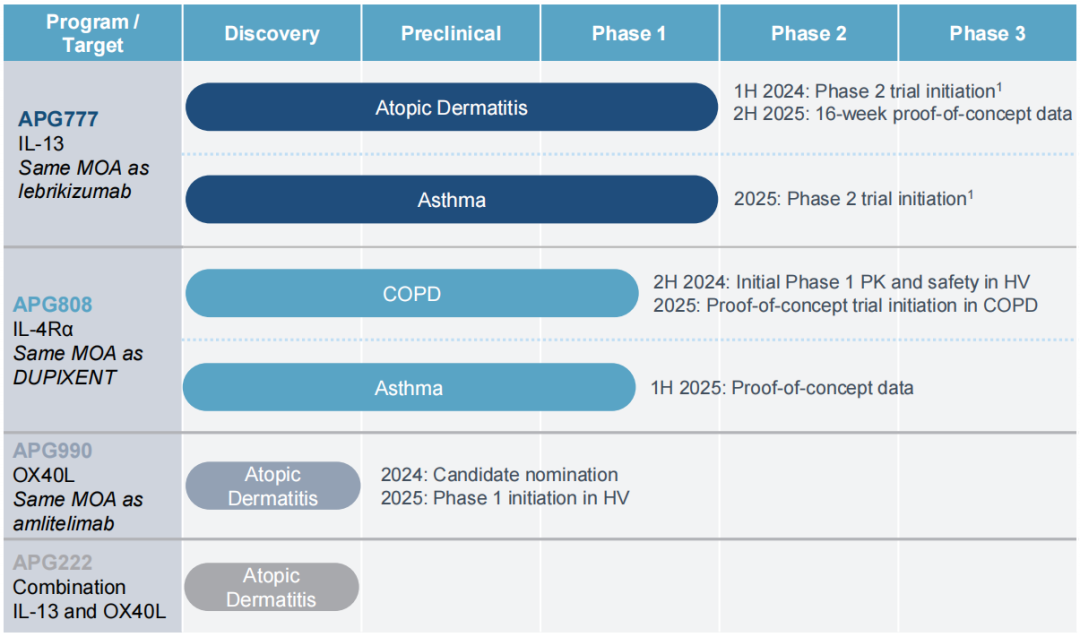
1.APG777
APG777是一种靶向IL-13的新型皮下延长半衰期单克隆抗体,可用于治疗特应性皮炎(AD)。
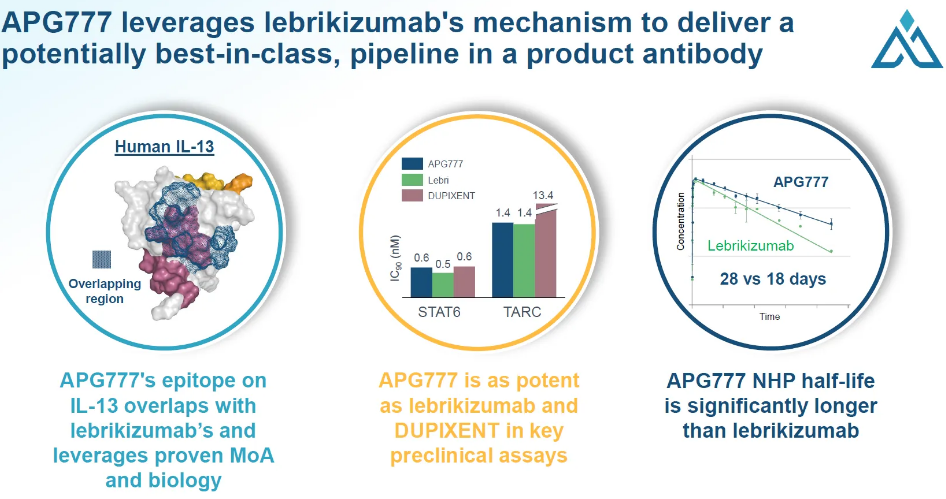
IL-13作为治疗AD(特应性皮炎)的公认靶点,在人体免疫反应中起重要作用,通常在特应性皮炎疾病进程中过量产生,导致皮肤屏障减弱,使细菌和病原体更容易进入皮肤,并加剧炎症反应,从而导致瘙痒、皮肤发红和进一步损伤。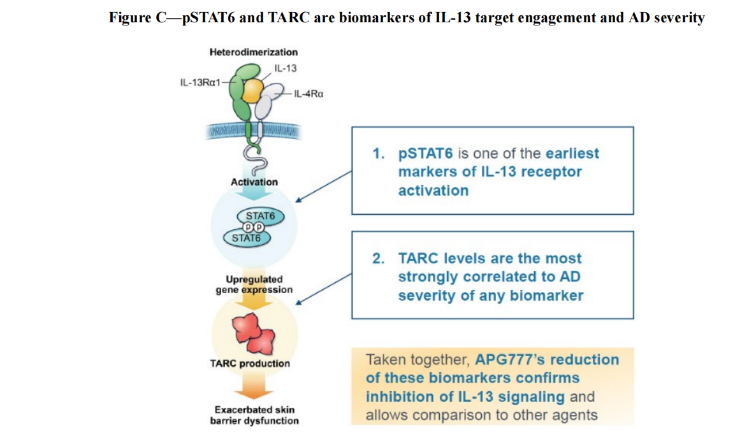
图:pSTAT6和TARC作为IL-13参与和AD严重程度的生物标志物
2024年3月5日,Apogee公布了APG777的首次人体研究的中期临床试验1期数据。临床试验1期研究是一项首次人体、随机、双盲、安慰剂对照研究,旨在评估APG777在健康志愿者中的安全性和药代动力学。药代动力学数据显示,测试剂量的半衰期约为75天,药效学数据显示对关键AD生物标志物pSTAT6和TARC的深度和持续抑制3个月。目前批准的特应性皮炎和其他免疫学适应症疗法通常需要每两到四周注射一次,这可能导致治疗依从性差和长期疾病控制。数据表明,APG777与目前批准的生物疗法相比,诱导暴露量增加,维持给药频率明显降低,有可能改善临床反应,这对AD和其他炎症性疾病患者来说是一个潜在的重大进步。积极中期结果之后,Apogee计划将APG777推进到一项为期16周的随机、安慰剂对照、中度至重度AD患者的临床试验2期研究中。临床试验2期研究预计将于2024年上半年启动,A部分的16周顶线数据预计将于2025年下半年公布。
根据初步临床数据,Apogee可能会在2025年启动针对哮喘的临床试验2期研究,并计划进一步评估开发APG777用于其他I&I适应症的机会,包括斑秃、慢性鼻窦炎伴鼻息肉、慢性自发性荨麻疹、嗜酸性粒细胞性食管炎和结节性痒疹。
2.APG808
APG808是一种新型的皮下注射延长半衰期的单克隆抗体,其靶向IL-4Rα,可用于慢性阻塞性肺病(COPD)、哮喘和其他炎症和免疫适应症的潜在治疗。与第一代单克隆抗体Dupixent相比,APG808对IL-4Rα具有相似的结合和飞摩尔亲和力,并且在测量IL-13/IL-4通路下游功能抑制(pSTAT6诱导、TF-1增殖的抑制和TARC分泌的抑制)的三个体外试验中表现出与Dupixent相似的抑制作用。

2024年3月25日,Apogee宣布开始在APG808的首次临床试验中对健康志愿者进行给药。APG808的临床试验1期研究为双盲、安慰剂对照、首次人体、单次剂量递增的健康志愿者试验,旨在评估APG808的安全性、耐受性和药代动力学。预计在2024年下半年获得中期安全性和药代动力学数据。在等待临床试验1期数据的同时,Apogee计划在2025年上半年启动一项潜在的针对哮喘的临床试验1b期研究,并于2025年启动针对中度至重度COPD患者的随机、安慰剂对照临床试验2期研究。
3.其他开发管线
APG990是一种针对OX40L的皮下延长半衰期单抗,通过阻断与OX40的相互作用并重新平衡AD中的细胞免疫反应。APG222通过OX40L和IL-13的双重抑制来解决多个免疫信号干预点。Apogee预计在2024年提名APG990为候选药物,并于2025年在健康志愿者中启动临床试验1期研究。
二、财务状况
Apogee截至2023年12月31日年度的研发费用为6840万美元,2022年成立至2022年12月31日期间为2780万美元,研发费用的增加主要是由于Apogee的APG777和APG808项目的进一步发展及其产品线的推进,以及与研发团队增长相关的人员成本增加,包括基于股权的薪酬费用。2023年度的一般和行政费用为2460万美元,2022年成立至2022年12月31日期间为290万美元。一般与行政费用的增加主要是由于人事成本的增加,包括股权薪酬以及法律和专业服务,所有这些都是Apogee扩大业务以支持其业务增长和作为上市公司运营成本的结果。2023年度净亏损为8400万美元,2022年成立至2022年12月31日期间净亏损为3980万美元,净亏损增加主要是由于研发和一般与行政运营费用的增加,部分被利息收入的增加所抵消。
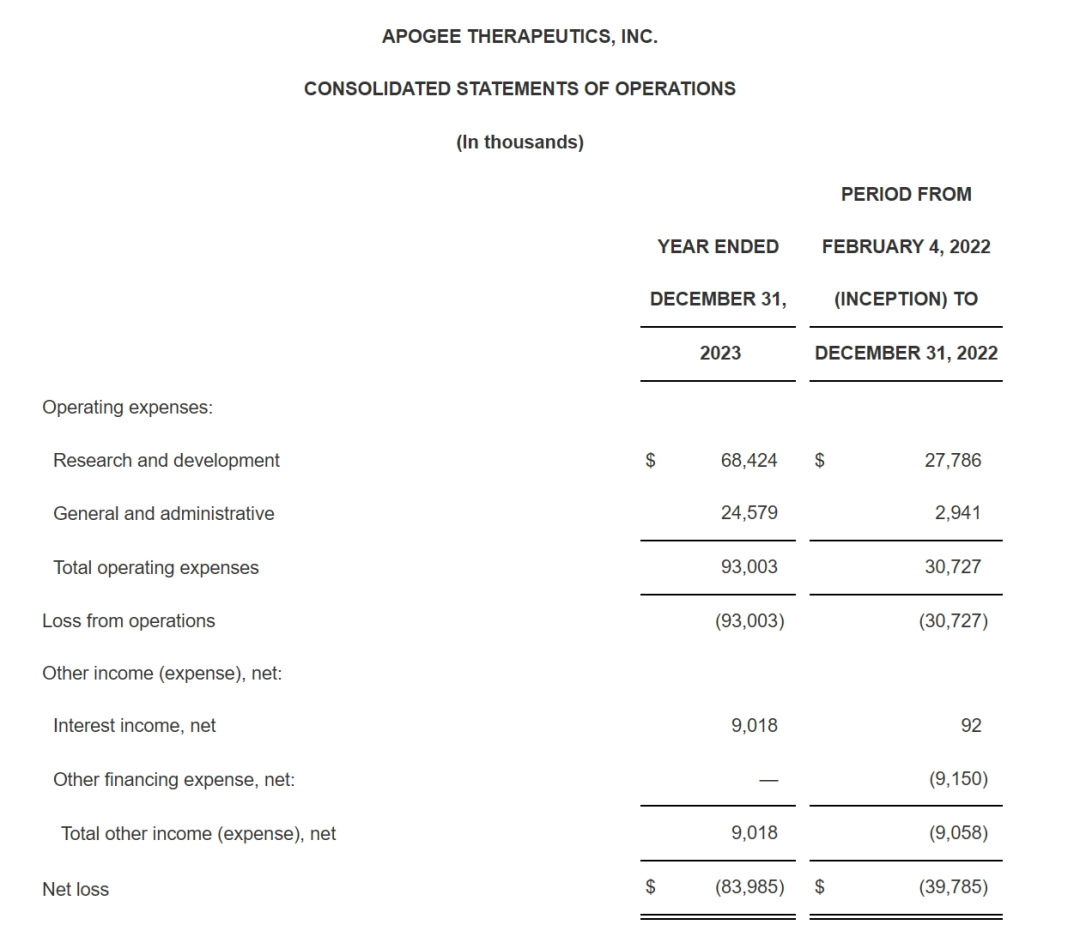
截至2023年12月31日,现金、现金等价物和有价证券为3.955亿美元。根据目前的运营计划,Apogee预计其现有的现金、现金等价物和有价证券将使公司能够为其2026年第四季度的运营费用提供资金。
文案发出前,市值31.42亿美元。

参考:
NMPA/CDE
药融云数据,www.pharnexcloud.com
FDA/EMA/PMDA;
相关公司公开披露(除标注外,正文图片均来自企业官网);
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论