
5月6日,中国生物制药(HK.01177)下属企业正大天晴自主研发的全球首个CDK2/4/6抑制剂库莫西利胶囊(赛坦欣®)获得国家药品监督管理局(NMPA)批准,联合氟维司群用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌患者的初始治疗。这是库莫西利胶囊获批上市的第2个适应症,为中国HR阳性晚期乳腺癌患者一线治疗提供全新的治疗方案。

截图来源:NMPA官网
去年12月,库莫西利已获批联合氟维司群用于既往内分泌治疗后出现疾病进展的HR+/HER2-乳腺癌适应症,在临床中预估已惠及上千名乳腺癌患者。
本次新增适应症的获批主要基于CULMINATE-2临床研究,显示库莫西利联合氟维司群对比安慰剂联合氟维司群可显著延长无进展生存期,并且长期用药安全性良好。
一、高效低毒,晚期乳腺癌患者迎一线治疗新选择
乳腺癌是全球及中国女性群体中的“第一大癌种”,据国际癌症研究机构统计,全球每年新发乳腺癌近百万例,中国每年新发近40万例。其中,HR+/HER2-乳腺癌是最常见的亚型,约占全部乳腺癌的65%-70%[1]。《中国临床肿瘤学会(CSCO)乳腺癌指南(2026年版)》和《中国抗癌协会乳腺癌诊治指南与规范(2026年版)》等指南均将CDK4/6抑制剂联合内分泌治疗作为HR+/HER2-晚期乳腺癌一线治疗方案[2,3],但随之而来的CDK4/6抑制剂耐药和骨髓抑制成为临床亟待解决的问题。
库莫西利作为全球首款CDK2/4/6抑制剂,从机制上可以更全面地抑制细胞周期信号通路,为克服耐药提供新思路。库莫西利在传统CDK4/6抑制剂的基础上,对CDK2具有强效的抑制作用,三重阻断CDK信号通路有助于延缓临床上CDK4/6抑制剂的耐药问题。此外,库莫西利在保持CDK4的高效抑制作用的同时,选择性降低对CDK6作用,相比传统CDK4/6抑制剂,这有助于降低严重骨髓抑制的发生风险[4]。基于机制上的创新,库莫西利为一线治疗延缓耐药,或二线治疗克服耐药,提供全新的更优疗效选择。
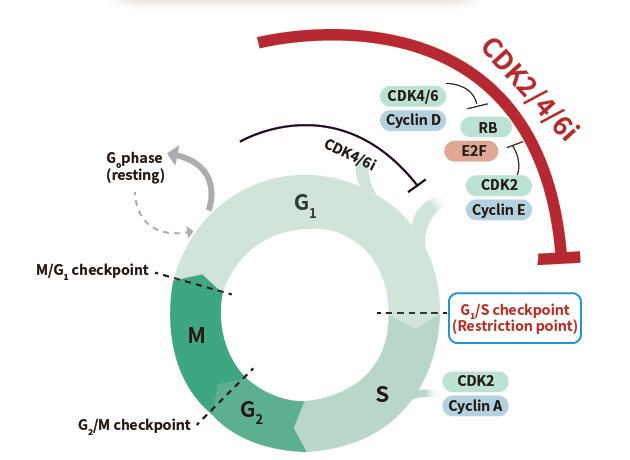
图1. 库莫西利作用机制: 全面抑制CDK2/4/6,阻断细胞周期进展,抑制肿瘤细胞增殖
本次新增适应症的获批主要基于CULMINATE-2临床研究结果。CULMINATE-2研究证实,库莫西利联合氟维司群一线治疗HR+/HER2-晚期乳腺癌,客观缓解率达59.3%,疾病进展或死亡风险降低44%;≥3级中性粒细胞减少发生率仅20.3%,因不良事件导致的治疗终止率仅3.5%,在内脏转移、绝经前人群中均表现出稳定获益,为突破CDK4/6抑制剂耐药提供了新选择,并且长期用药的安全性可控、易管理。
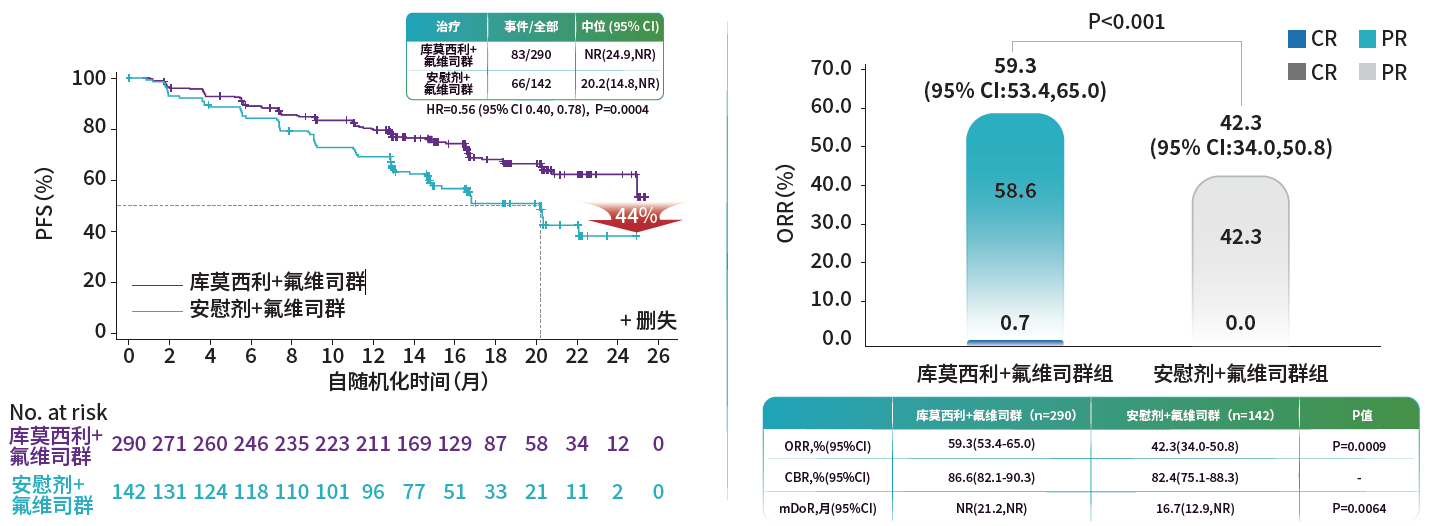
图2. 库莫西利联合氟维司群用于HR+/HER-晚期乳腺癌一线治疗显著延长无进展生存期和提高客观缓解率
二、多点布局,中国生物制药进军乳腺癌领域
库莫西利临床潜力巨大,布局开发的适应症可覆盖HR阳性乳腺癌治疗全周期。其中,联合氟维司群用于既往内分泌治疗后出现疾病进展的HR+/HER2-晚期乳腺癌适应症已于2025年12月9日在国内获批上市。备受关注的HR+早期乳腺癌辅助治疗也在同步进行中,目前已入组完成,正在进行随访中。
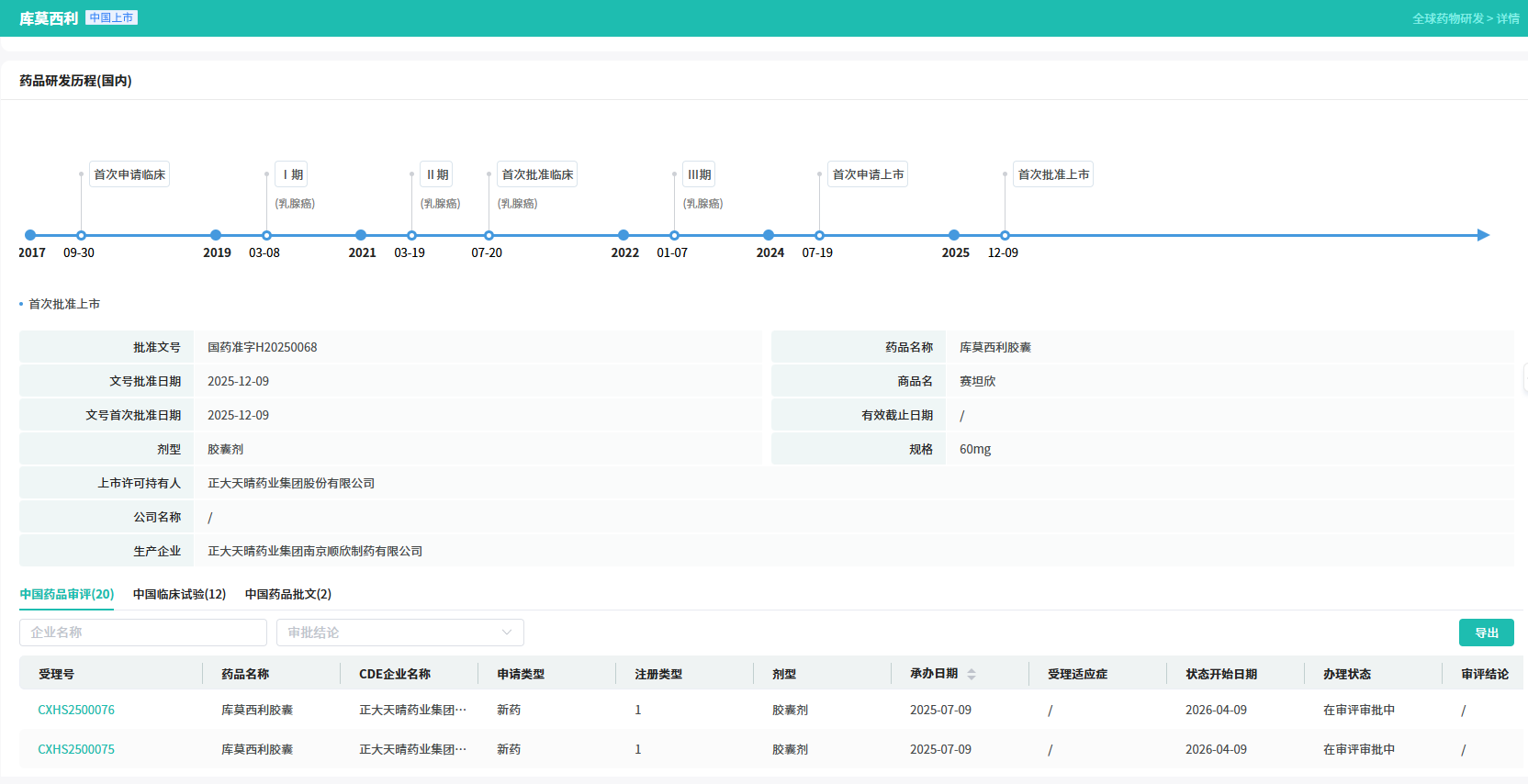
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
当前乳腺癌是全球创新药物的必争之地。据弗若斯特沙利文预测,到2030年全球乳腺癌市场规模达到699亿美元,中国乳腺癌市场将达到172亿美元(10年CAGR8%),是全球肿瘤领域最大、增长最确定的细分赛道之一。中国生物制药长期持续的坚持基于临床治疗需求的创新探索,逐步搭建起其在全球乳腺癌领域极具竞争力的产品线。
聚焦乳腺癌治疗领域,中国生物制药布局的产品线不仅全面覆盖HER2+、HER2低表达、HR+/HER2-以及三阴性乳腺癌(TNBC)分子分型,并且在治疗周期上系统性覆盖从新辅助治疗、辅助治疗到晚期一二线及以上的全线治疗场景,力求为更多乳腺癌患者提供新的治疗选择。
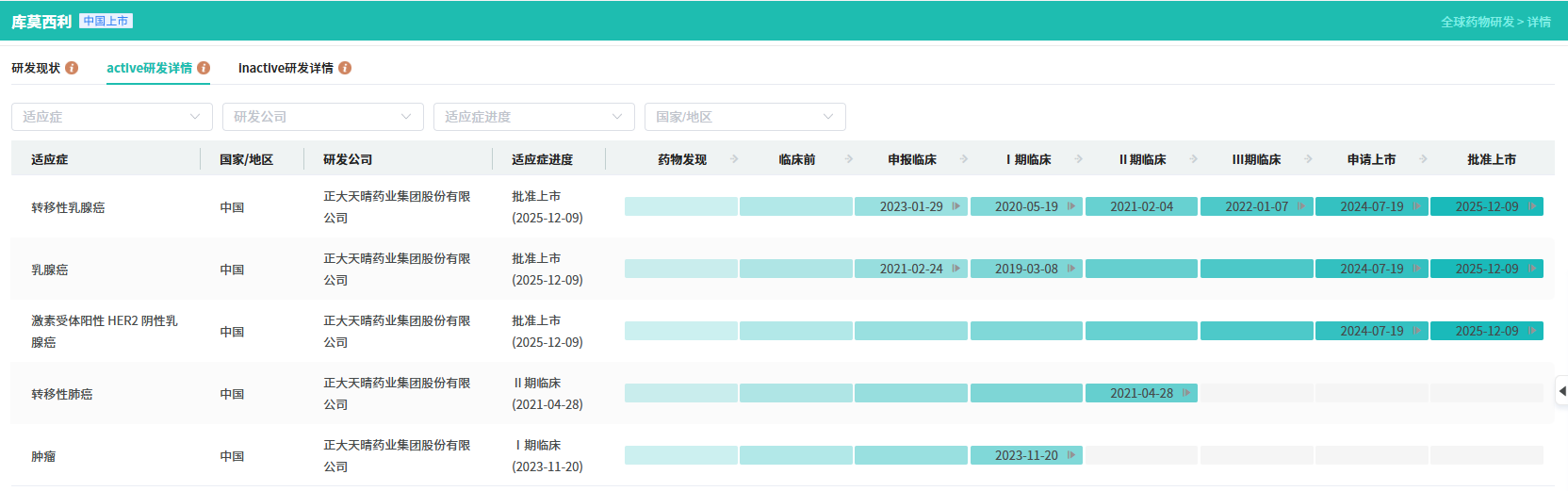
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
在HR+/HER2-领域除库莫西利,还差异化布局了TQB3126(ER-PROTAC)、TQB3122(PARP1)、TQB2101(ROR1 ADC)等产品。今年以来,拟用于HER2表达乳腺癌治疗的TQB2102(HER2双抗ADC)接连两次被CDE纳入突破性治疗品种,用于HER2低表达和HER2阳性乳腺癌等多项适应症的Ⅲ期临床试验已完成患者入组,同样用于HER2阳性乳腺癌治疗的TQB2930(HER2双抗)也已处于Ⅲ期临床研究阶段。此外,“得福组合”(贝莫苏拜单抗+安罗替尼)在三阴性乳腺癌的相关研究中创35.81个月OS(总生存期)新高,显示可能为这种难治性乳腺癌提供更有效方案的潜力。
随着库莫西利用于HR阳性晚期乳腺癌一线治疗适应症的获批上市,以及潜力管线的推进,中国生物制药有望形成覆盖全分型、全周期的产品矩阵,重塑整个乳腺癌的治疗格局。
参考文献:
[1] 邬昊,吕青.全球及中国乳腺癌的流行病学趋势及防控启示:2018–2022年《全球癌症统计报告》解读[J].中国普外基础与临床杂志,2024,31(07):796-802.
[2] National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guideline).Breast Cancer, version 5. 2023[EB/OL]. [2024-01-12].
[3] 中国临床肿瘤学会指南工作委员会,编著.中国临床肿瘤学会乳腺癌诊疗指南 2025[M].北京:人民卫生出版社.
[4] Xu Z, Liu Y, Song B, et al. Discovery and preclinical evaluations of TQB3616, a novel CDK4-biased inhibitor. Bioorganic & Medicinal Chemistry Letters 2024; 107.
[5] Erwei song, et al. Culmerciclib plus fulvestrant as first-line treatment for HR+/HER2- advanced breast cancer cancer:A phase 3 trial(CULMINATE-2),ESMO 2025 LBA25.
[6] NMPA官网
[7] 摩熵医药(原药融云)数据库
扩展阅读:
1. 中国生物制药LM-302联合PD-1抑制剂启动Ⅲ期临床,突破CLDN18.2阳性胃癌一线“去化疗”治疗
2. 2025年药企财报:中国生物制药、恒瑞医药、复星医药创新药收入集体爆发,石药营收下滑行业分化加剧
3. 中国生物制药:全球首创新药罗伐昔替尼独家授权赛诺菲,解锁药企全链条研发新价值与出海新路径
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论