1.4.1 本周全球TOP10创新药研发进展
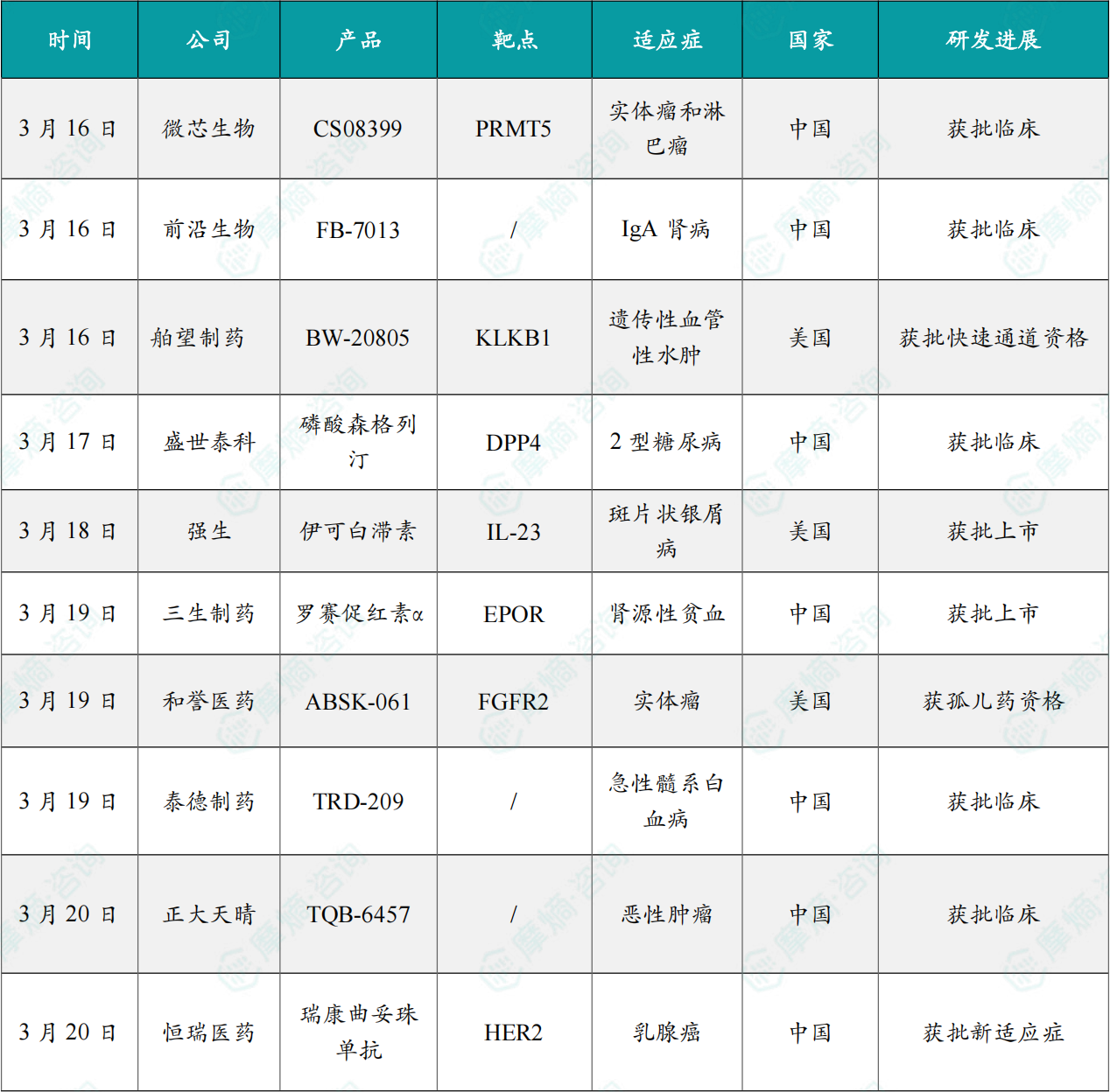
(1)微芯生物PRMT5-MTA抑制剂获批临床
3月16日,微芯生物宣布其全资子公司成都微芯药业自主研发的1类原创新药CS08399片用于治疗甲硫基腺苷磷酸化酶(MTAP)缺失的实体瘤和淋巴瘤的临床试验申请(IND)已获中国国家药品监督管理局(NMPA)批准。
CS08399片是一款脑透过性口服甲硫腺苷(MTA)协同型蛋白精氨酸甲基转移酶5(PRMT5)小分子抑制剂。该候选药物针对MTAP缺失型肿瘤细胞具有高度选择性抗肿瘤活性,其作用机制明确且具有独特的靶向优势。
(2)前沿生物siRNA新药获批临床,针对IgA肾病
3月16日,中国国家药监局药品审评中心(CDE)官网公示显示,前沿生物1类新药FB7013注射液获批临床,拟用于原发性IgA肾病的治疗。
根据公示信息,FB7013注射液是靶向MASP-2的GalNAc偶联的siRNA药物,抑制MASP-2可能对IgA肾病的肾小球和小管间质都有保护作用。
(3)舶望制药siRNA疗法获FDA授予快速通道资格
3月16日,舶望制药宣布,其在研siRNA疗法BW-20805获得美国FDA授予快速通道资格,用于治疗遗传性血管性水肿(HAE)。
HAE是一种罕见的遗传性疾病,会导致身体不同部位突然出现不可预测的肿胀。重症患者可出现喉部水肿,致死率高达约40%。
BW-20805是一种靶向前激肽释放酶(PKK)的siRNA疗法,通过靶向PKK mRNA而抑制PKK基因的表达,有望为HAE患者提供长效的发作预防。PKK是目前HAE治疗领域已获得充分验证的作用靶点。
近期舶望制药在美国过敏、哮喘与免疫学会年会(AAAAI)上公布的数据显示,BW-20805可显著降低血浆PKK水平,并实现具有临床意义的HAE发作率降幅。
(4)盛世泰科降糖复方制剂获批临床
3月17日,盛世泰科宣布,其自主开发的磷酸森格列汀与盐酸二甲双胍的复方制剂获批临床,用于经二甲双胍单药治疗血糖仍控制不佳或正在接受二者联合治疗的2型糖尿病患者。
盛世泰科新闻稿表示,这是该公司继1类新药森格列汀上市后,在降糖药物研发中又一重要进展。
(5)强生全球首创口服IL-23R拮抗剂在美国获批上市
3月18日,强生宣布Icotrokinra(商品名:Icotyde)获得FDA批准上市,用于治疗12岁及以上青少年和成人的中重度斑块状银屑病(PsO)。
Icotrokinra是一款可靶向阻断IL-23受体(IL-23R)的口服多肽药物,与IL-23R的结合亲和力可达到个位数的pM级别。此次批准是基于ICONIC系列III期临床研究的数据,包括ICONIC-LEAD研究、ICONIC-TOTAL研究、ICONIC-ADVANCE 1研究和ICONIC-ADVANCE 2研究结果。
(6)三生制药罗赛促红素α获批上市
3月19日,国家药监局(NMPA)官网显示,三生制药的罗赛促红素α注射液(商品名:新比澳)获批上市,用于治疗因慢性肾脏病引起的贫血,且正在接受促红细胞生成素治疗的血液透析患者。这是首个获批上市的国产重组促红细胞生成素(EPO)创新药。
罗赛促红素α(曾用研发代号:SSS06)是一款高糖基化长效重组蛋白产品,利用基因重组技术对rHuEPO基因进行定位突变,增加了3个N-糖基化位点。NMPA此次批准是基于一项注册性III期研究的结果。2024年1月,三生制药宣布SSS06的III期临床研究达到预设主要终点。该研究旨在比较SSS06与益比奥在血液透析的慢性肾衰竭贫血患者中维持治疗的有效性及安全性。
(7)和誉医药FGFR2/3抑制剂获FDA授予孤儿药资格
3月19日,和誉医药宣布,其自主研发的高选择性小分子FGFR2/3抑制剂ABSK061已获得美国FDA授予的孤儿药资格(ODD),用于治疗软骨发育不全(ACH)。
新闻稿表示,这是ABSK061近期获得FDA针对ACH适应症的罕见儿科疾病(RPD)资格后,在全球开发进程中斩获的又一关键进展。
(8)靶向SHP2,泰德制药蛋白降解剂1类新药获批临床
3月19日,中国国家药监局药品审评中心(CDE)官网公示显示,中国生物制药下属企业泰德制药申报的1类新药注射用TRD209获批临床,拟开发治疗成人急性髓系白血病。公开资料显示,这是一款靶向SHP2的双特异性蛋白降解疗法。
(9)正大天晴CCR8+PD-1复方制剂1类新药获批临床
3月20日,正大天晴宣布其1类创新药TQB6457注射液在中国获批临床,用于治疗晚期恶性肿瘤。这是一款CCR8单克隆抗体与PD-1抗体组成的固定复方制剂,旨在通过探索以单一制剂代替联合用药,助力提升晚期肿瘤患者用药依从性、打破用药限制。
(10)恒瑞医药HER2 ADC获批新适应症,治疗乳腺癌
3月20日,恒瑞医药宣布,国家药品监督管理局批准其HER2 ADC瑞康曲妥珠单抗(商品名:艾维达®)新增适应症:适用于治疗既往接受过一种或一种以上抗HER2药物治疗的局部晚期或转移性HER2阳性成人乳腺癌患者。这是瑞康曲妥珠单抗获批上市的第二项适应症,也是该药在乳腺癌领域获批的首个适应症。
Ⅲ期研究HORIZON-Breast01结果显示,瑞康曲妥珠单抗组经盲法独立中心审查委员会(BICR)评估的中位无进展生存期(mPFS)达30.6个月,客观缓解率(ORR)高达81.7%。基于该突破性数据,瑞康曲妥珠单抗成为我国HER2阳性晚期乳腺癌二线治疗领域首个mPFS突破30个月的新型ADC。
1.4.2 本周全球TOP10积极/失败临床结果
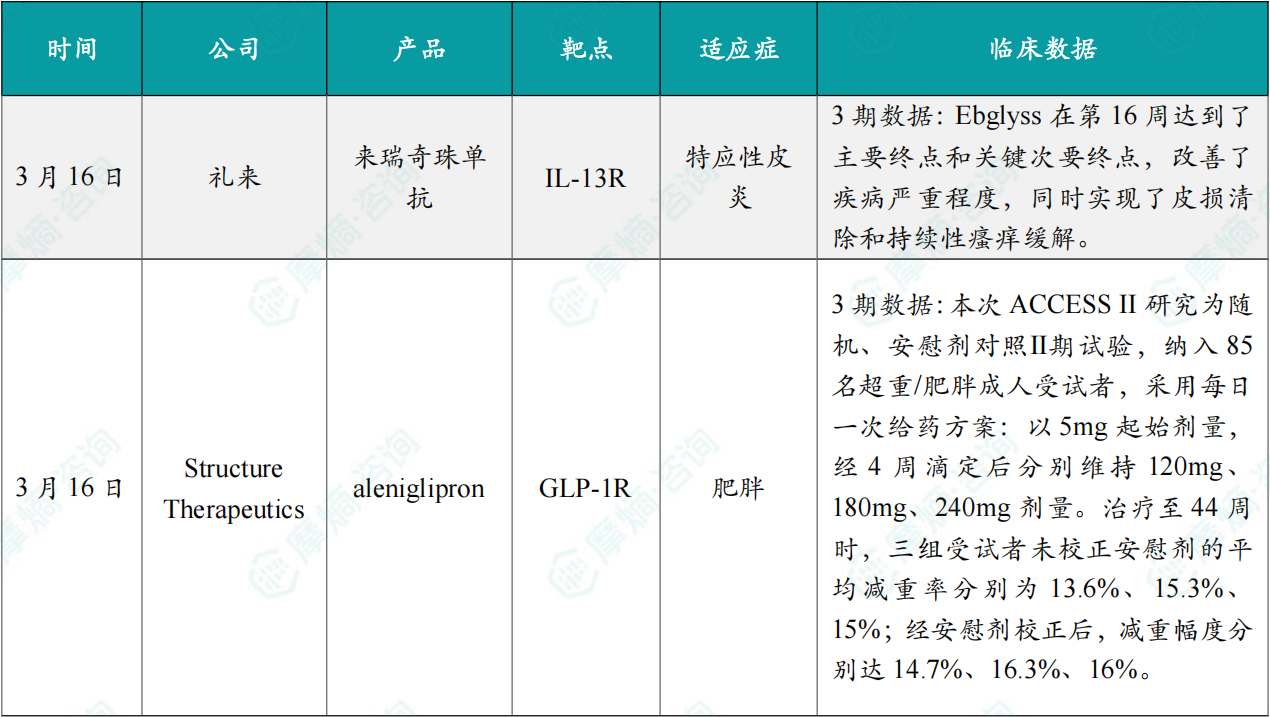
(1)礼来IL-13单抗一项III期研究成功,拟申请扩大适应症
3月16日,礼来公布了III期ADorable-1研究的积极结果,该研究评估了Ebglyss(来瑞奇珠单抗)在中重度特应性皮炎儿科患者(包括6个月大的婴儿和儿童)中的安全性与疗效。Ebglyss在第16周达到了主要终点和关键次要终点,改善了疾病严重程度,同时实现了皮损清除和持续性瘙痒缓解。特应性皮炎在儿童中的患病率高于成人,在美国影响960万儿童,其中三分之一患有中重度疾病。礼来计划将这些数据提交给美国及全球监管机构,以申请扩展适应症。
(2)口服小分子GLP-1二期临床结果亮眼,即将启动三期研究
3月16日,Structure Therapeutics公布其每日一次口服小分子GLP-1受体激动剂aleniglipron的Ⅱ期ACCESS II临床试验顶线数据:经安慰剂校正后最高减重幅度达16%(约39磅),公司宣称该数据为目前口服GLP-1药物中最优疗效,且减重效果未出现平台期,即将推进Ⅲ期临床开发。
本次ACCESS II研究为随机、安慰剂对照Ⅱ期试验,纳入85名超重/肥胖成人受试者,采用每日一次给药方案:以5mg起始剂量,经4周滴定后分别维持120mg、180mg、240mg剂量。治疗至44周时,三组受试者未校正安慰剂的平均减重率分别为13.6%、15.3%、15%;经安慰剂校正后,减重幅度分别达14.7%、16.3%、16%。公司明确表示,截至观察节点,未观察到减重效果进入平台期,持续减重潜力突出。
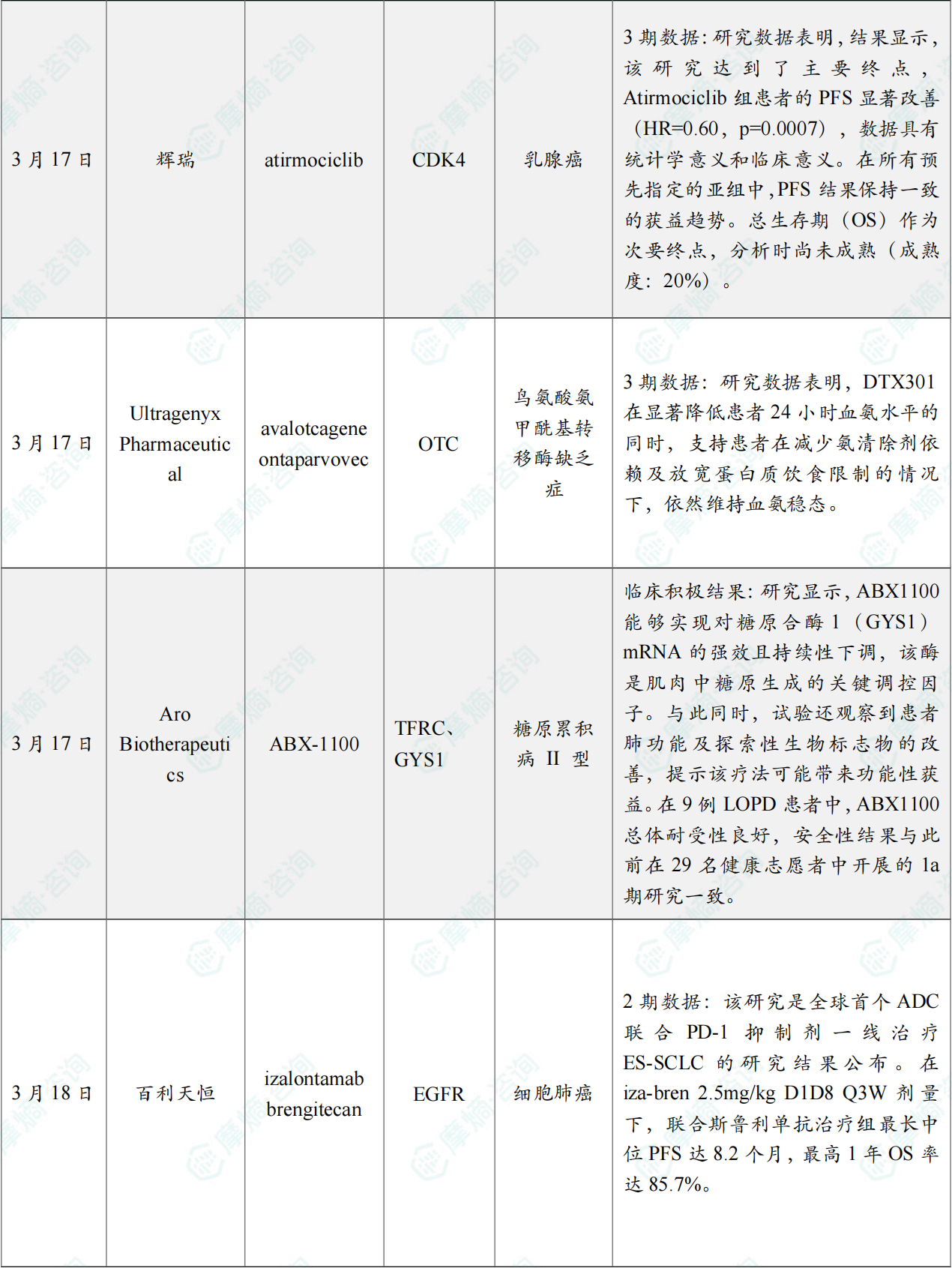
(3)全球首个CDK4抑制剂II期研究成功
3月17日,辉瑞宣布CDK4抑制剂Atirmociclib治疗HR+/HER2-晚期或转移性乳腺癌的II期FOURLIGHT-1研究取得了积极结果。这是全球首个完成II期研究的CDK4抑制剂。
该研究是一项介入性、开放标签、随机、多中心临床试验(n=264),评估了Atirmociclib联合氟维司群对比氟维司群或者依维莫司联合依西美坦治疗经CDK4/6抑制剂治疗后疾病进展的HR+/HER2-晚期或转移性乳腺癌成年患者的有效性和安全性。研究的主要终点为研究者评估的无进展生存期(PFS)。
结果显示,该研究达到了主要终点,Atirmociclib组患者的PFS显著改善 (HR=0.60,p=0.0007),数据具有统计学意义和临床意义。在所有预先指定的亚组中,PFS结果保持一致的获益趋势。总生存期(OS)作为次要终点,分析时尚未成熟(成熟度:20%)。
(4)罕见病AAV基因疗法III期临床成功
3月17日,Ultragenyx Pharmaceutical宣布其在研AAV8基因疗法DTX301(avalotcagene ontaparvovec)用于治疗鸟氨酸转氨甲酰酶(OTC)缺乏症的关键III期Enh3ance研究取得了积极的顶线结果。
研究数据表明,DTX301在显著降低患者24小时血氨水平的同时,支持患者在减少氨清除剂依赖及放宽蛋白质饮食限制的情况下,依然维持血氨稳态。
DTX301是目前全球进展最快的、唯一一款进入III期临床研究的OTC缺乏症基因疗法,可以利用AAV8载体将正常的OTC基因递送至肝脏细胞,使患者能够自主合成功能性酶,从根本上恢复尿素循环。
(5)创新庞贝病siRNA疗法临床积极结果公布
3月17日,Aro Biotherapeutics公布其在研siRNA疗法ABX1100用于治疗晚发型庞贝病(LOPD)的1b期部分临床试验积极顶线结果。
研究显示,ABX1100能够实现对糖原合酶1(GYS1)mRNA的强效且持续性下调,该酶是肌肉中糖原生成的关键调控因子。与此同时,试验还观察到患者肺功能及探索性生物标志物的改善,提示该疗法可能带来功能性获益。在9例LOPD患者中,ABX1100总体耐受性良好,安全性结果与此前在29名健康志愿者中开展的1a期研究一致。ABX1100由可结合CD71受体的Centyrin与siRNA偶联构成,通过特异性抑制GYS1表达以降低肌肉中糖原生成水平,目前已获得美国FDA孤儿药资格和罕见儿科疾病认定。
(6)百利天恒双抗ADC联合PD-1一线治疗小细胞肺癌II期数据公布
3月18日,百利天恒宣布其自主研发的全球首创EGFR×HER3双抗ADC药物iza-bren(BL-B01D1)联合PD-1单抗斯鲁利单抗,用于初治广泛期小细胞肺癌(ES-SCLC)的II期临床研究取得积极成果,并成功入选2026年欧洲肺癌大会(ELCC 2026)口头报告专场。
百利天恒新闻稿指出,该研究是全球首个ADC联合PD-1抑制剂一线治疗ES-SCLC的研究结果公布。在iza-bren 2.5mg/kg D1D8 Q3W剂量下,联合斯鲁利单抗治疗组最长中位PFS达8.2个月,最高1年OS率达85.7%。
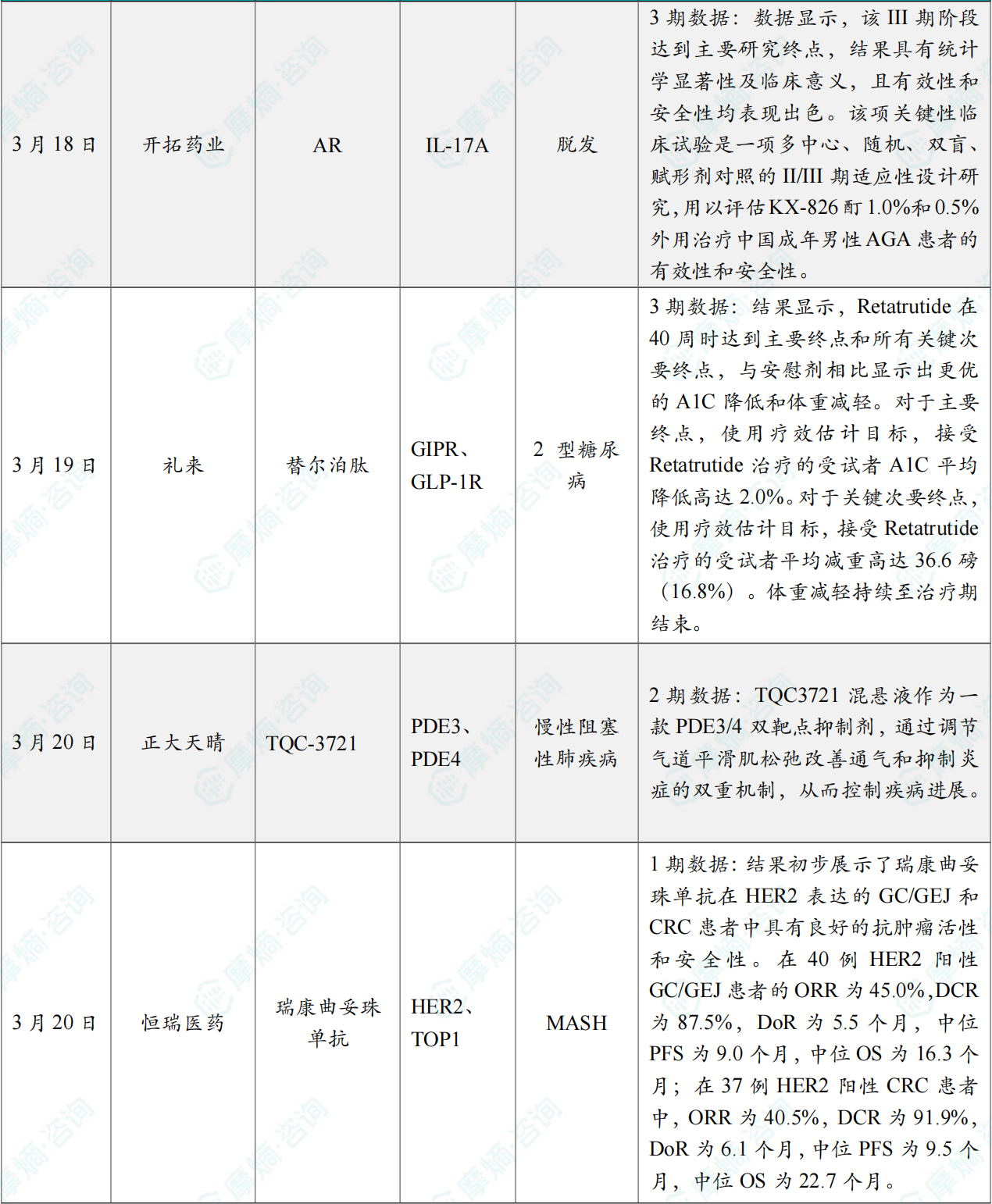
(7)开拓药业男性脱发药物III期成功,即将申报上市
3月18日,开拓药业宣布,其自主研发、潜在同类首创的KX-826酊1.0%治疗中国成年男性雄激素脱发(AGA)的关键性临床试验III期阶段已获得顶线数据。数据显示,该III期阶段达到主要研究终点,结果具有统计学显著性及临床意义,且有效性和安全性均表现出色。
该项关键性临床试验是一项多中心、随机、双盲、赋形剂对照的II/III期适应性设计研究,用以评估KX-826酊1.0%和0.5%外用治疗中国成年男性AGA患者的有效性和安全性。
KX-826是开拓药业目前进展最快的外用创新药物之一,作为外用药物,通过与雄激素竞争结合靶组织中的雄激素受体,直接阻断雄激素信号传导的通道。开拓药业计划于近期递交KX-826 1.0%的上市许可申请。
(8)礼来GIPR/GLP-1R/GCGR三靶点激动剂2型糖尿病III期研究成功
3月19日,礼来宣布III期TRANSCEND-T2D-1研究取得了积极结果,该研究旨在评估GIPR/GLP-1R/GCGR三靶点激动剂Retatrutide与安慰剂作为辅助治疗,在仅靠饮食和运动血糖控制不佳的2型糖尿病成人患者中的疗效和安全性。
结果显示,Retatrutide在40周时达到主要终点和所有关键次要终点,与安慰剂相比显示出更优的A1C降低和体重减轻。对于主要终点,使用疗效估计目标,接受Retatrutide治疗的受试者A1C平均降低高达2.0%。对于关键次要终点,使用疗效估计目标,接受Retatrutide治疗的受试者平均减重高达36.6磅(16.8%)。体重减轻持续至治疗期结束。
(9)正大天晴PDE3/4抑制剂II期临床积极结果发布于知名期刊
3月20日,中国生物制药(1177.HK)核心企业正大天晴自主研发的PDE3/4抑制剂TQC3721混悬液用于慢性阻塞性肺疾病(COPD)的Ⅱ期临床试验(PACER-Ⅱ)研究结果正式发表在国际呼吸领域知名期刊《CHEST》。
TQC3721混悬液作为一款PDE3/4双靶点抑制剂,通过调节气道平滑肌松弛改善通气和抑制炎症的双重机制,从而控制疾病进展。基于Ⅱ期研究的积极进展,TQC3721混悬液正在开展用于COPD维持治疗的Ⅲ期关键验证研究(NCT07147946)。
2025年7月,监管部门批准了TQC3721混悬液在COPD治疗的突破疗法申请,首个Ⅲ期试验有望在2026年底获得顶线数据。除吸入混悬液外,TQC3721吸入粉雾剂也已进入Ⅱ期临床试验阶段,预计于2026年年中获得顶线数据。
(10)恒瑞HER2 ADC I期结果发布,治疗胃癌和结直肠癌
3月20日,恒瑞医药自主研发的以HER2为靶点的抗体偶联物(ADC)瑞康曲妥珠单抗治疗晚期胃/胃食管结合部腺癌(GC/GEJ)和结直肠癌(CRC)患者的Ⅰ期临床数据,重磅发表于肿瘤学领域顶级期刊《临床肿瘤学杂志》(Journal of Clinical Oncology,简称JCO,IF:43.4)。
本研究由中国药科大学上海高博肿瘤医院李进教授担任通讯作者。研究结果初步展示了瑞康曲妥珠单抗在HER2表达的GC/GEJ和CRC患者中具有良好的抗肿瘤活性和安全性。在40例HER2阳性GC/GEJ患者的ORR为45.0%,DCR为87.5%,DoR为5.5个月,中位PFS为9.0个月,中位OS为16.3个月;在37例HER2阳性CRC患者中,ORR为40.5%,DCR为91.9%,DoR为6.1个月,中位PFS为9.5个月,中位OS为22.7个月。
同期事件:
1. 2026年第12周03.16-03.22国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第12周03.16-03.22国内仿制药/生物类似物申报/审批数据分析
3. 2026年第12周03.16-03.22国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.03.16-2026.03.22) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论