1.1.1 总体概况
根据摩熵医药数据库统计,2026.03.16-2026.03.22期间共有57个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号44个,进口药品受理号13个。
本周共计75款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药36款,生物药35款,4款中药。其中值得注意的有:
(1)RAG-01注射液
2026年3月16日,CDE官网公示:中美瑞康申报RAG-01注射液获得临床试验默示许可,用于治疗非肌层浸润性膀胱癌(NMIBC)。
公开资料显示,RAG-01是中美瑞康开发的一款特异性靶向激活肿瘤抑制基因p21的双链小激活RNA(saRNA)药物,通过RNAa机制激活p21基因的表达,以抑制肿瘤细胞增殖、诱导细胞凋亡和衰老。
(2)FB-7013注射液
2026年3月16日,CDE官网公示:前沿生物申报的FB-7013注射液获得临床试验默示许可,用于治疗原发性IgA肾病。
公开资料显示,FB7013注射液是靶向补体系统凝集素途径关键蛋白MASP-2的GalNAc偶联的siRNA药物,抑制MASP-2可能对IgA肾病的肾小球和小管间质都有保护作用。该产品通过特异性抑制MASP-2活性阻断凝集素途径异常激活,减少补体介导的肾脏组织损伤。
(3)IN-10028肠溶片
2026年3月19日,CDE官网公示:应世生物申报的IN-10028肠溶片获得临床试验默示许可,拟用于晚期实体瘤的治疗。
公开资料显示,IN10028为下一代FAK抑制剂,可有效靶向FAK1和FAK2,并显著抑制FAK相关信号通路。与第一代FAK抑制剂IN10018相比,IN10028显示出更好的癌细胞细胞毒性。IN10028也表现出比几种第一代FAK抑制剂更强的靶标结合性。
本周1款新药获批上市。
2026年3月19日,国家药品监督管理局发布监管工作通知:国家药品监督管理局批准广东三生制药有限公司申报的罗赛促红素α注射液(商品名:新比澳)上市,该品种用于治疗因慢性肾脏病引起的贫血,且正在接受促红细胞生成素治疗的血液透析患者。
公开资料显示,罗赛促红素α是三生制药自主研发的一款高糖基化重组蛋白创新产品。其核心技术在于通过基因重组技术,在促红细胞生成素分子上精准增加糖基化位点,优化蛋白稳定性,在完整保留生物学活性的同时,显著延长体内半衰期。
1.1.2 本周获批临床创新药/改良型新药信息速览(不含补充申请)

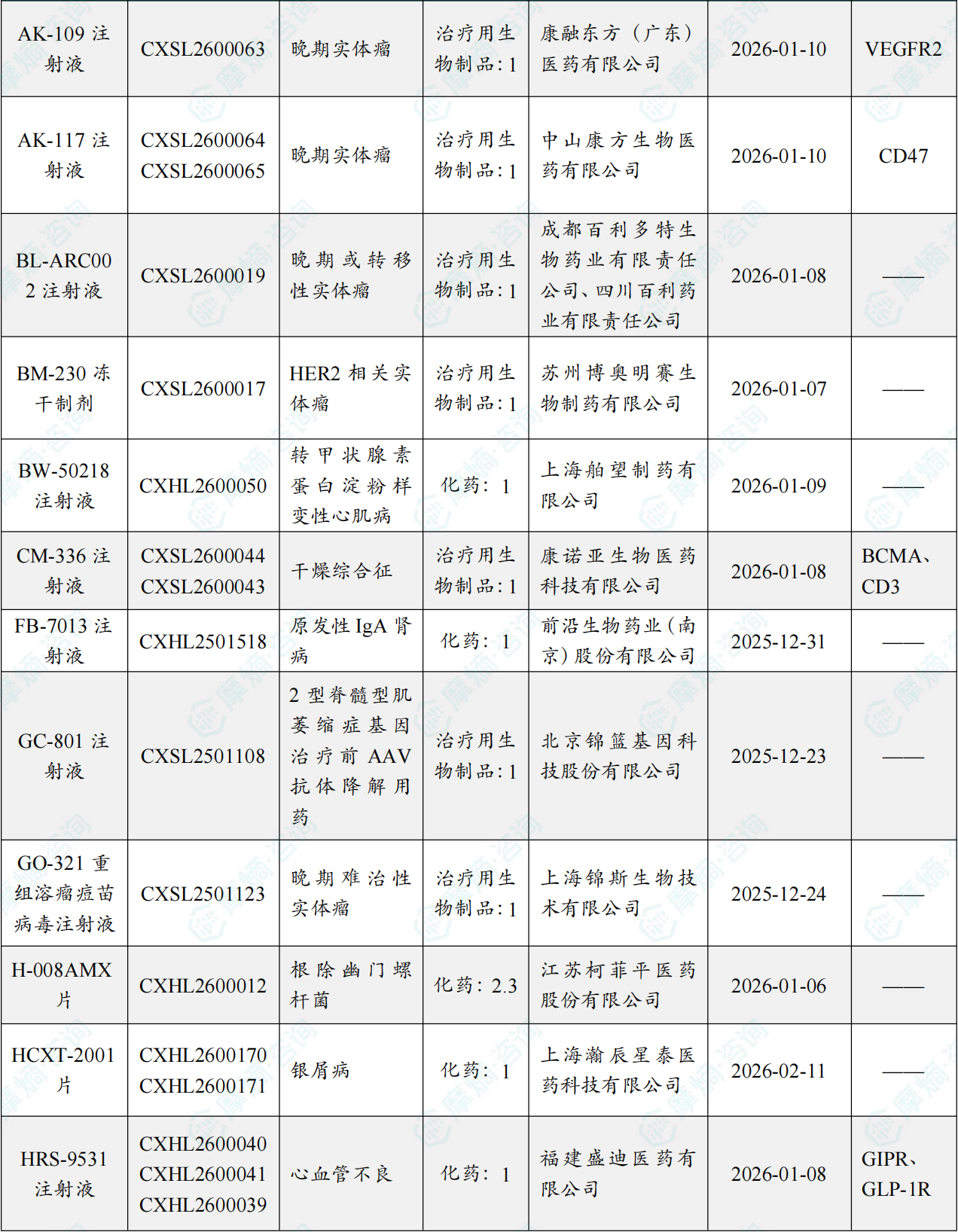
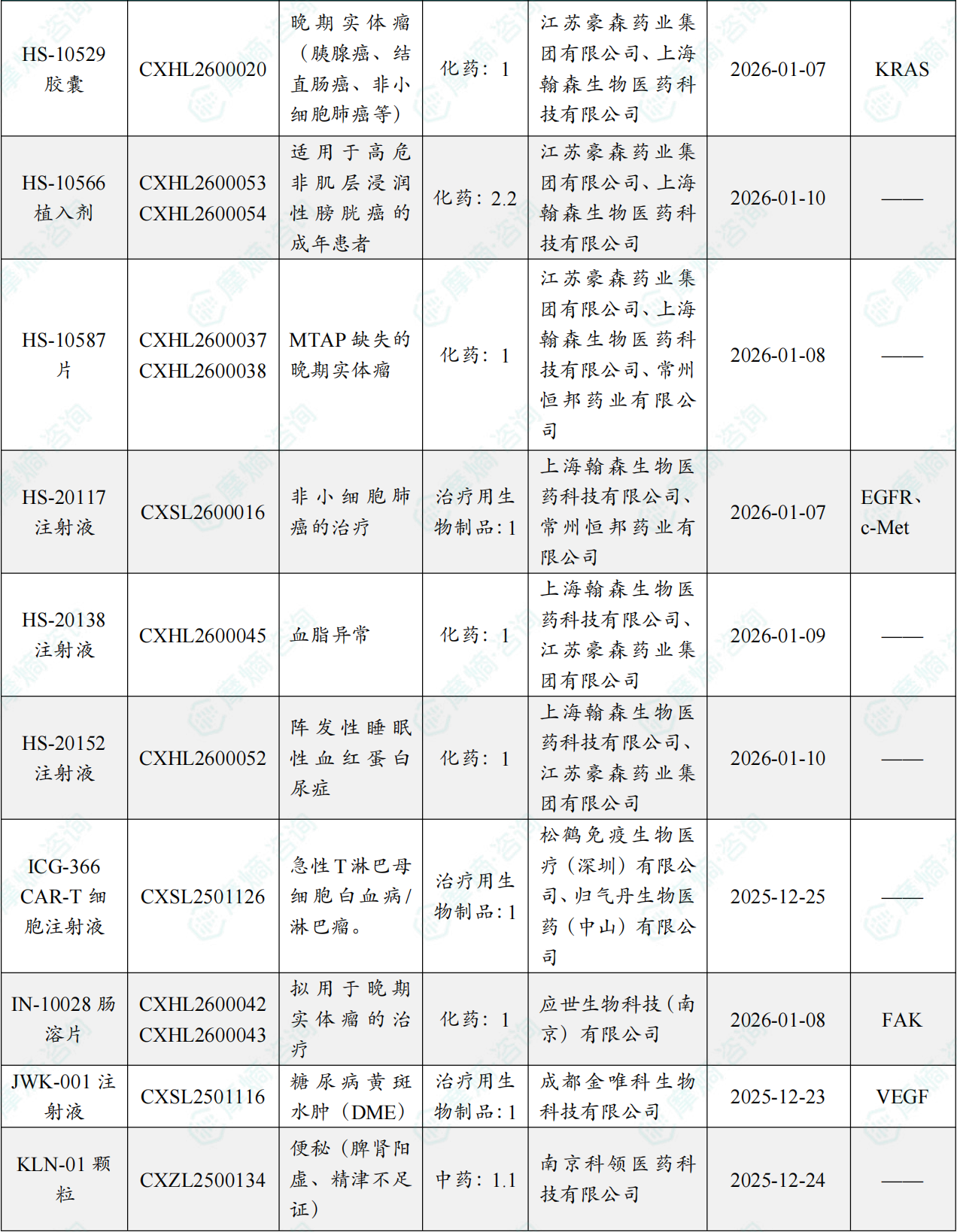
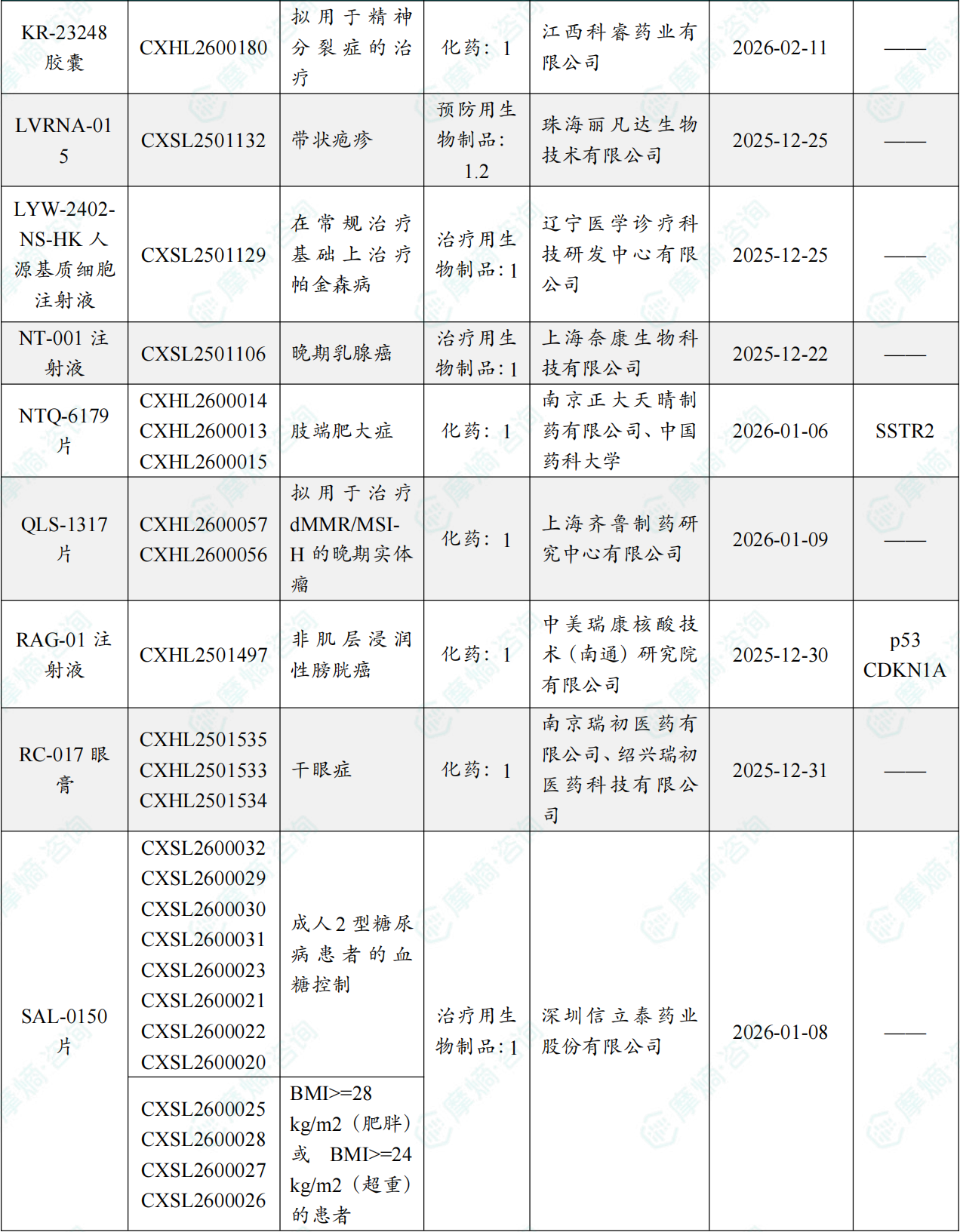
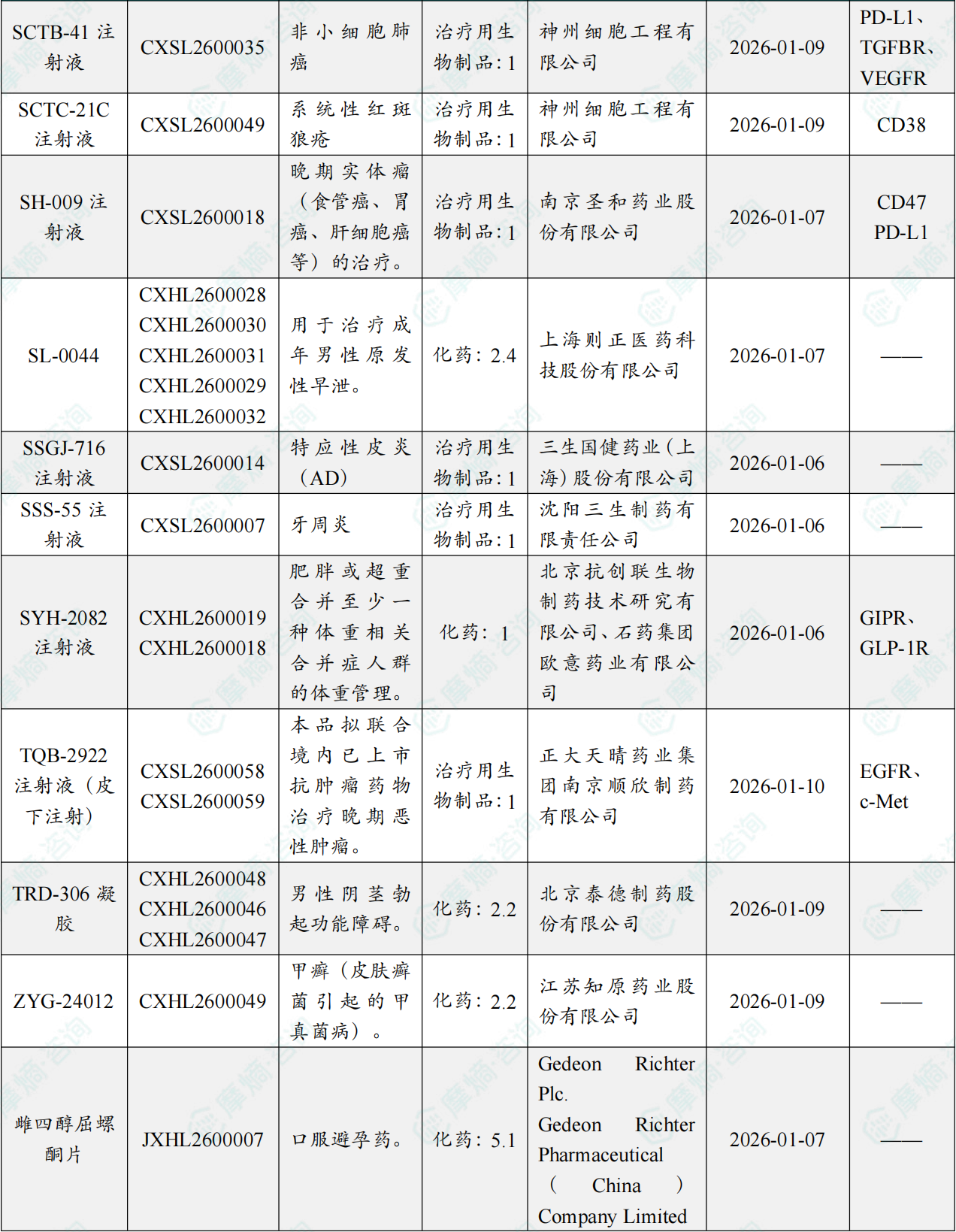
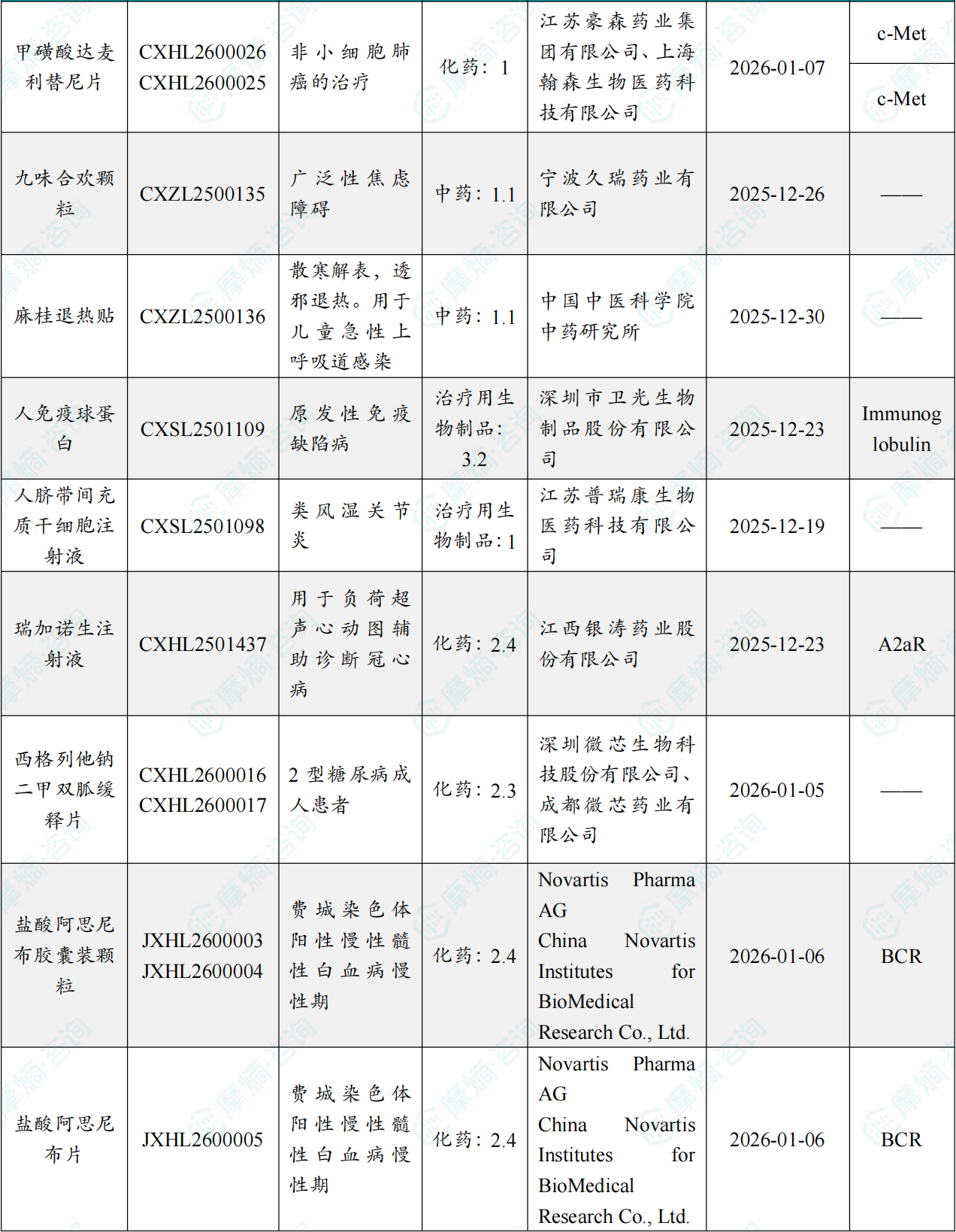
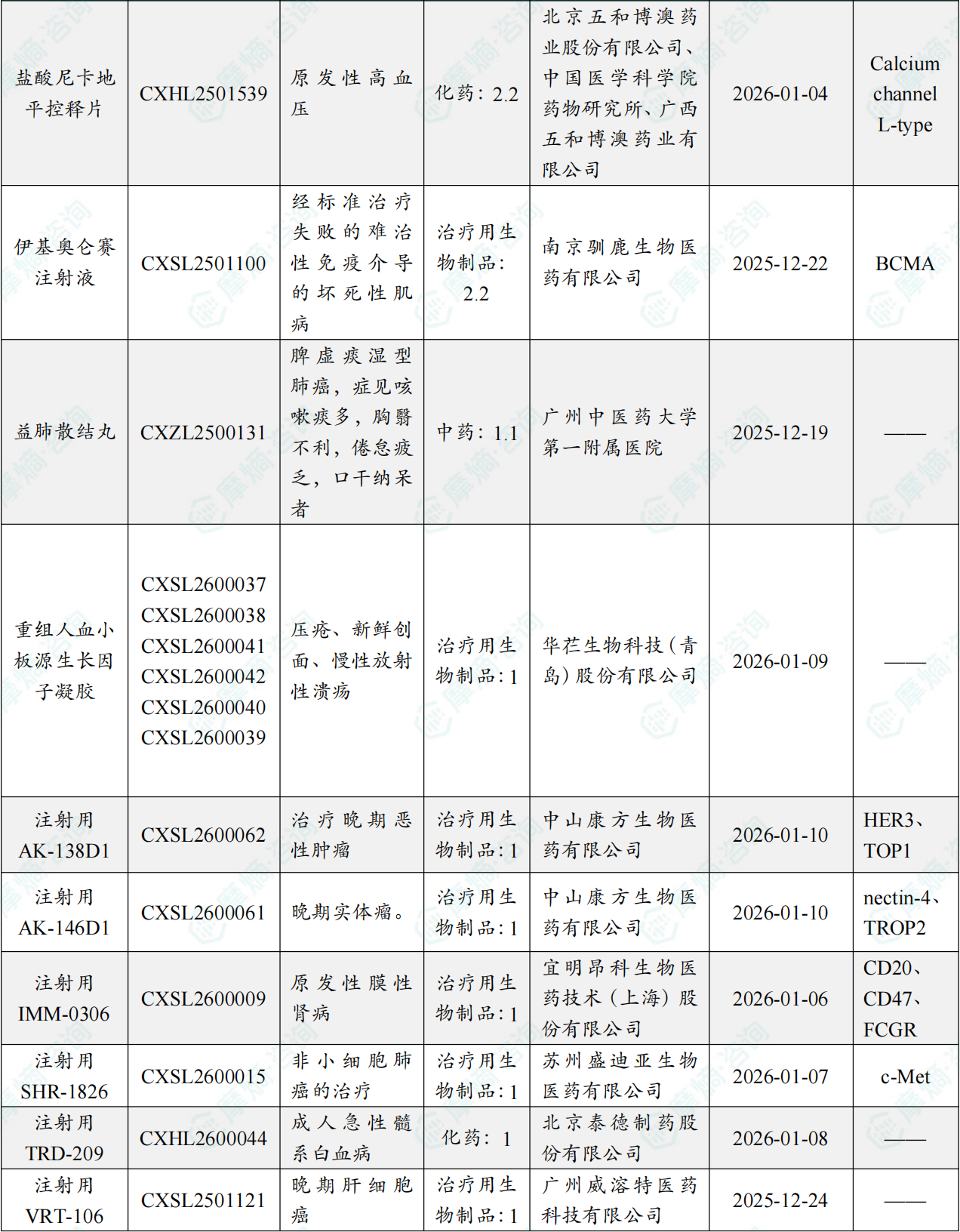
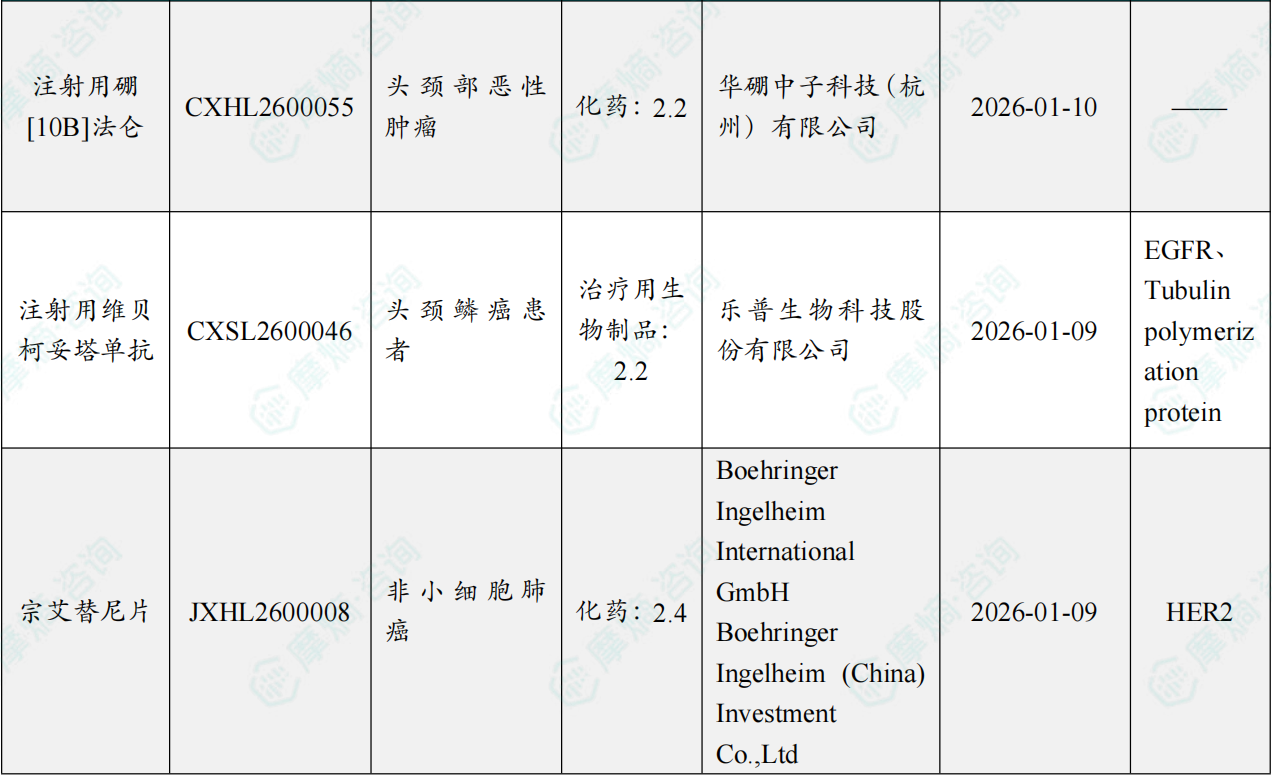
备注:(1)此处未包括补充申请之情形;(2)此处所列创新药/改良型新药,主要是指CDE受理批准的1类、2类、5.1类以及生物制品3.1类和3.2类。(3)更多获批临床信息及研发进展详情及相关靶点全局分析等,可通过摩熵中国药品审评数据库获取并下载EXCEL表格。
1.1.3 本周获批上市创新药信息速览
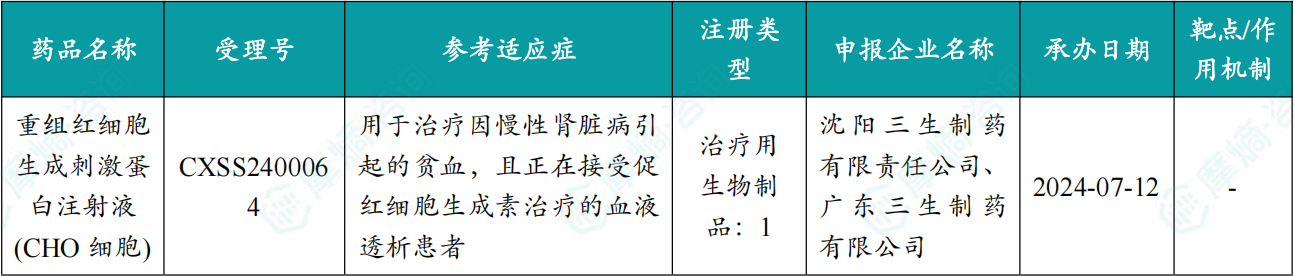
备注:(1)此处所列新药,主要是指国家药品监督管理局(NMPA)首次批准在中国上市的药品,包括新分子实体(以及包含有新分子实体的复方)、生物药、中药和疫苗。其中,新分子实体主要是化药注册分类下的1类(境内外均未上市的创新药)、5.1类(境外上市的原研药申请在国内上市);生物药主要为NMPA首次批准的国产及进口生物药;不包括生物类似物、新适应症、新剂型。(2)更多信息如获批临床品种相关靶点、研发企业、全球上市及研发进展及相关靶点全局分析等,可通过摩熵医药数据库获取并下载EXCEL表格。
同期事件:
1. 2026年第12周03.16-03.22国内仿制药/生物类似物申报/审批数据分析
2. 2026年第12周03.16-03.22国内医药大健康行业政策法规汇总
3. 2026年第12周03.16-03.22全球创新药研发概览
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.03.16-2026.03.22) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论