1.4.1 本周全球TOP10创新药研发进展
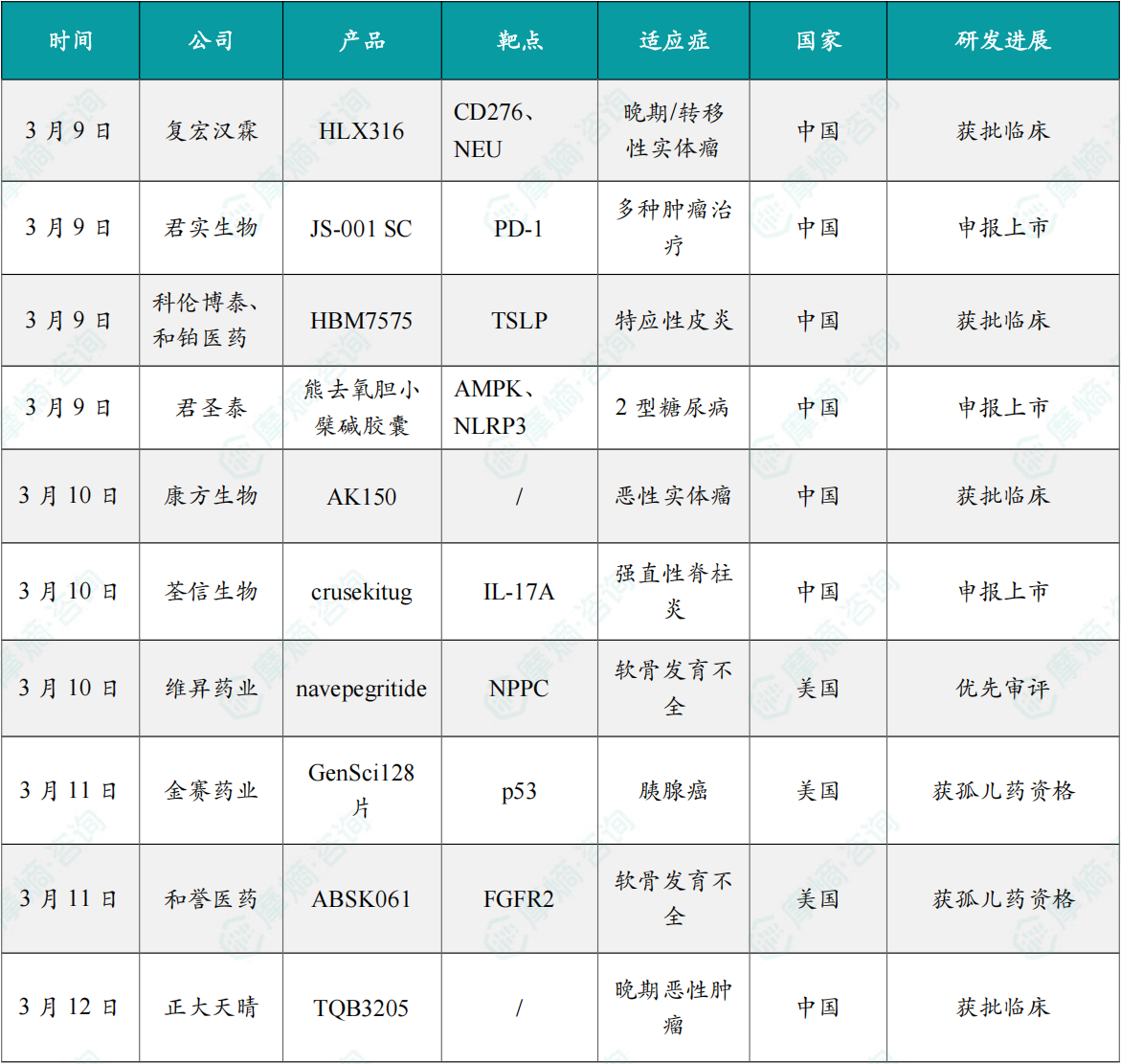
(1)复宏汉霖1类融合蛋白癌症新药获批临床
3月9日,中国国家药监局药品审评中心(CDE)官网公示显示,复宏汉霖1类新药注射用HLX316获批临床,拟开发治疗晚期/转移性实体瘤。公开资料显示,这是一款B7H3-唾液酸酶融合蛋白。
B7H3是一种免疫检查点蛋白,在多个上皮癌(包括肺癌、乳腺癌、结直肠癌、胰腺癌、前列腺癌和卵巢癌等)中过表达,且与肿瘤进展和预后不良相关,但其在正常组织中的表达水平很低。肿瘤高唾液酸化会衔接白细胞上的抑制性 Siglec 受体,从而削弱先天性和适应性免疫效应功能,导致 ICI 耐药性。
HLX316是一款基于蛋白工程平台开发的靶向B7同源物3(B7H3/CD276)的人唾液酸酶融合蛋白。据复宏汉霖此前新闻稿介绍,通过酶促作用去除末端唾液酸并浓缩其在 B7H3 阳性肿瘤细胞中的活性,HLX316可解除糖免疫检查点抑制,并恢复肿瘤微环境内的先天性和适应性抗肿瘤功能。HLX316有潜力靶向PD-1/PD-L1以外的免疫抑制生物学机制,拓宽免疫治疗在实体瘤中的应用范围,突破现有治疗方案局限。
(2)君实生物皮下注射抗PD-1单抗12项癌症适应症申报上市
3月9日,君实生物宣布,该公司自主研发的抗PD-1单抗皮下制剂特瑞普利单抗注射液(皮下注射)(产品代号:JS001sc)用于肿瘤治疗的12项适应症上市申请于近日获得中国国家药品监督管理局(NMPA)受理。
JS001sc是君实生物在已上市产品特瑞普利单抗注射液(产品代号:JS001)的基础上开发的皮下注射制剂,有望给患者带来用药的便捷性。
本次JS001sc上市申请中的12项适应症为特瑞普利单抗注射液目前在中国内地已获批的全部适应症。这意味着,JS001sc有望覆盖非小细胞肺癌(NSCLC)、鼻咽癌、食管癌、肾癌、肝癌等多种肿瘤治疗。
(3)科伦博泰/和铂医药长效TSLP双抗获批临床,针对特应性皮炎
3月9日,中国国家药监局药品审评中心(CDE)官网显示,科伦博泰与和铂医药共同申报注册的双抗SKB575(HBM7575)获批临床,拟用于治疗特应性皮炎。
SKB575是一款由科伦博泰主导研发的靶向胸腺基质淋巴细胞生成素(TSLP)及一个未公开靶点的超长效双特异性抗体,具有双重作用机制:一方面通过阻断TSLP与其受体的相互作用,可抑制TSLP介导的信号通路以及Th2免疫细胞的激活;另一方面,其针对另一未公开靶点的结合与阻断可产生协同效应,有潜力克服TSLP单靶点抗体的耐药问题。
(4)君圣泰全球首创新药申报上市,治疗糖尿病
3月9日,CDE网站显示,君圣泰的熊去氧胆小檗碱(HTD1801)胶囊申报上市,用于治疗2型糖尿病。
HTD1801是一款全球首创的新分子实体,旨在解决心肾代谢系统疾病(CKM)的未满足临床需求。HTD1801作为单一分子,是具有独特双机制的口服抗炎及代谢调节剂(AIMM),通过激活AMPK及抑制NLRP3炎症小体发挥其生物学活性。目前,HTD1801在2型糖尿病人群中已完成3项III期临床试验。
(5)康方生物三抗1类癌症新药获批临床
3月10日,康方生物宣布,该公司研发的三特异性抗体新药AK150(ILT2/ILT4/CSF1R三抗)获得中国国家药品监督管理局药品审评中心(CDE)临床试验默示许可批准,开展用于治疗晚期恶性实体瘤的临床试验。AK150也是康方生物首个进入临床阶段的三抗新药,为该公司基于AI制药研发技术平台和Tetrabody多抗技术平台而开发。
ILT2、ILT4 和CSF1R在多种实体瘤中具有较高的表达水平,尤其在免疫抑制微环境显著的肿瘤类型中表现突出,包括非小细胞肺癌、肝细胞癌、胰腺癌以及部分难治性乳腺癌等。尽管当前全球范围内针对巨噬细胞的单靶点或双靶点药物(如靶向ILT2、ILT4或CSF1R)已展现出一定潜力,但这些药物仍难以进一步打破肿瘤微环境的免疫抑制网络,亟需能够实现多维度免疫重塑的多靶点协同创新疗法,提高抗肿瘤疗效,尤其是进一步破解传统免疫治疗对“冷肿瘤”不敏感的临床难题。
据康方生物新闻稿介绍,AK150可协同靶向CSF1R、ILT2和ILT4靶点,这三个靶点在肿瘤免疫微环境中各自发挥重要的免疫调节作用,共同构建复杂的免疫抑制网络,而三靶点协同阻断作用可以实现在不同层面解除免疫抑制,通过双向调节髓系细胞和淋巴细胞的功能,激活CD8+ T细胞及自然杀伤(NK)细胞,增强抗肿瘤免疫效应。
(6)荃信生物IL-17A抗体申报上市,治疗强直性脊柱炎
3月10日,荃信生物宣布,其首款创新药鲁塞奇塔单抗(QX002N)的新药上市申请(NDA)已获国家药品监督管理局受理(受理号:CXSS2600039),用于治疗成人活动性强直性脊柱炎(AS)。
此次NDA受理基于一项多中心、随机、双盲、安慰剂对照的III期临床试验(登记号:CTR20232574)。该研究的核心成果已于2025年10月在美国风湿病学会年会(ACR Convergence)上以口头报告形式发布。
研究结果显示,对于非甾体抗炎药反应不足或存在禁忌的活动性AS患者,鲁塞奇塔单抗在52周的治疗周期中持续显著改善疾病活动度及临床症状,并展现出良好的安全性与耐受性,治疗组和安慰剂组ASAS40分别为40.4%、18.9%,ASAS20分别为65.2%、41.3%。
(7)侏儒症新药拟纳入优先审评
3月10日,CDE官网显示,维昇药业递交的注射用那韦培肽拟纳入优先审评,适应症为适用于2岁及以上骨骺未闭合软骨发育不全儿童患者的治疗。那韦培肽由 Ascendis Pharma 公司开发,维昇药业拥有那韦培肽在大中华区的独家开发、生产及商业化权利。
作为 CNP 的研究性前药,那韦培肽采用每周一次的给药方式,其设计机制可向全身组织(包括生长板、骨骼肌)持续递送活性CNP,以此实现对软骨发育不全症患者的治疗作用。2月27 日,那韦培肽已获美国FDA加速批准上市,用于治疗2岁及以上患有软骨发育不全的儿童患者。
(8)金赛药业1类新药获FDA孤儿药资格,治疗胰腺癌
3月11日,金赛药业宣布,其自主研发的GenSci128片已获得美国FDA授予的孤儿药资格(ODD),用于胰腺癌的治疗。
GenSci128片是一种针对TP53 Y220C突变的选择性重激活剂,旨在选择性地与TP53 Y220C突变蛋白的口袋结合,从而恢复TP53 Y220C突变蛋白的正常构象,增加稳定性,恢复转录和抑制肿瘤的功能。GenSci128片在美国新药注册类别"505b1",拟用于治疗携带TP53 Y220C突变的局部晚期或转移性实体瘤,涵盖胰腺癌、卵巢癌、乳腺癌、结直肠癌等。其新药临床试验申请已获得FDA批准。此前,GenSci128片也已在中国获批开展用于携带TP53 Y220C突变的局部晚期或转移性实体瘤的临床试验。
(9)和誉医药FGFR2/3抑制剂获FDA授予罕见儿科疾病资格
3月11日,和誉医药宣布,其自主研发的高选择性小分子FGFR2/3抑制剂ABSK061治疗软骨发育不全(ACH)适应症获得美国FDA授予的罕见儿科疾病(RPD)资格认定。
ABSK061是和誉医药自主研发的高活性、高选择性小分子FGFR2/3抑制剂,通过降低对FGFR1的抑制以及保持对FGFR2/3的高活性,该产品作为第二代FGFR抑制剂有望在临床上取得更好的安全窗及疗效。目前ABSK061正在开展针对3-12岁ACH儿童患者的2期临床研究。
(10)正大天晴泛KRAS抑制剂1类癌症新药获批临床
3月12日,正大天晴宣布其自主研发的口服Pan-KRAS抑制剂——TQB3205首次获得中国国家药品监督管理局(NMPA)的临床试验默示许可,拟用于治疗晚期恶性肿瘤。
TQB3205胶囊是一款口服的Pan-KRAS抑制剂,核心作用机制为与多种KRAS突变蛋白实现高亲和力结合,通过抑制SOS1介导的KRAS核苷酸交换来阻断RAS的激活,进而抑制KRAS下游的ERK磷酸化,最终实现对多种KRAS突变肿瘤细胞增殖的有效抑制,从靶点层面精准发挥抗肿瘤效果。
1.4.2 本周全球TOP10积极/失败临床结果
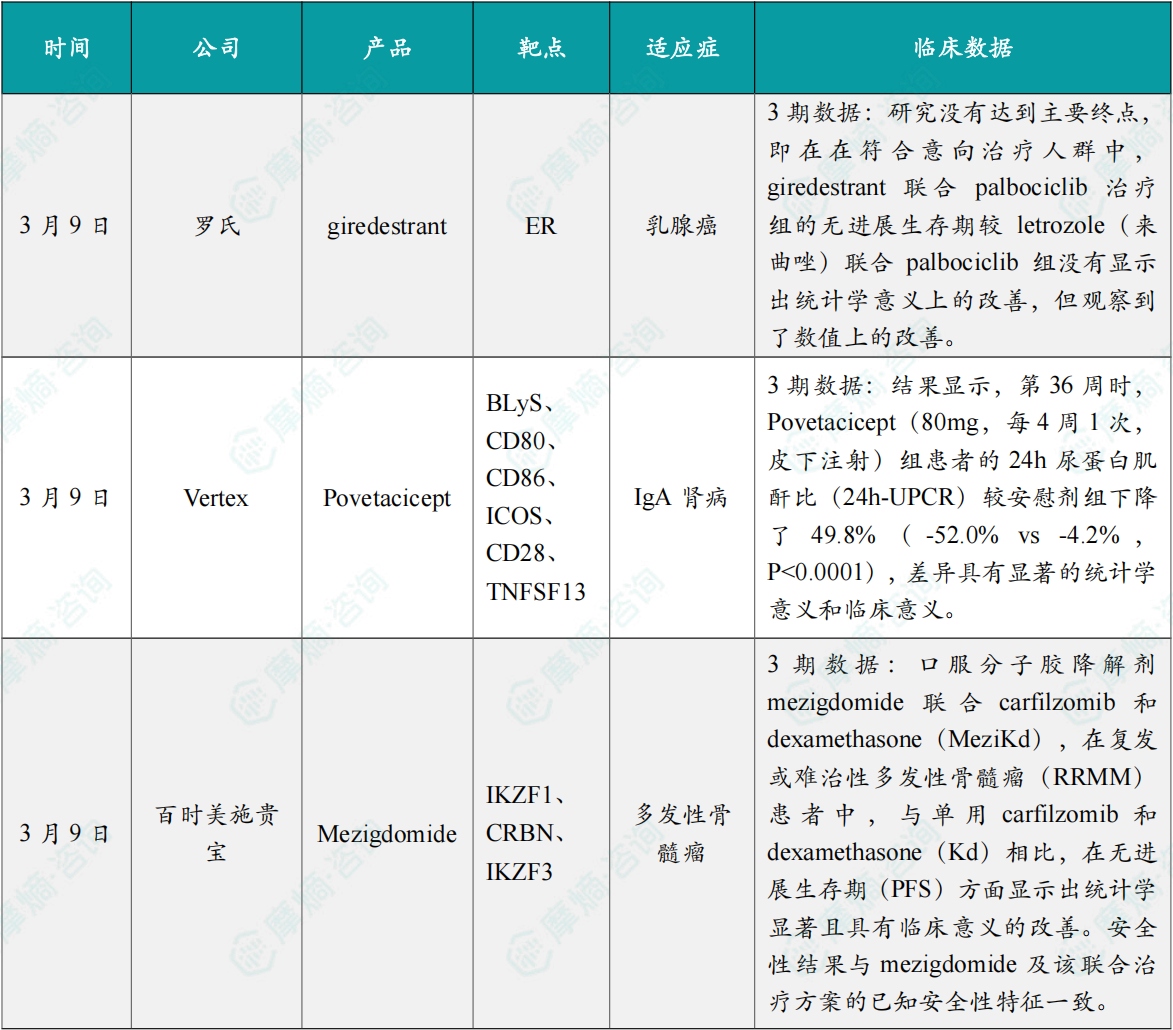
(1)罗氏口服SERD新药一项III期临床失败
3月9日,罗氏公布了 giredestrant 联合 palbociclib(哌柏西利)治疗雌激素受体(ER)阳性、人表皮生长因子受体 2(HER2)阴性、局部晚期或转移性乳腺癌患者的 III 期 persevERA 研究的结果。
persevERA 是一项随机、双盲、安慰剂对照、多中心 III 期临床试验。该研究在全球范围内共纳入了 992 名受试者,主要终点是研究者评估的无进展生存期,次要终点包括总生存期、客观缓解率、缓解持续时间和安全性。结果显示,该研究没有达到主要终点,即在在符合意向治疗人群中,giredestrant 联合 palbociclib 治疗组的无进展生存期较 letrozole(来曲唑)联合 palbociclib 组没有显示出统计学意义上的改善,但观察到了数值上的改善。
(2)每月1次IgA肾病新药III期研究成功,即将申报上市
3月9日,Vertex宣布Povetacicept治疗IgA肾病的III期RAINIER研究取得了积极结果。
Povetacicept是一种靶向B细胞激活因子(BAFF)和增殖性诱导配体(APRIL)的双重抑制剂,以此抑制B细胞激活、分化和/或存活,从而治疗多种自身免疫性疾病。RAINIER研究的中期分析结果显示,第36周时,Povetacicept(80mg,每4周1次,皮下注射)组患者的24h尿蛋白肌酐比(24h-UPCR)较安慰剂组下降了49.8%(-52.0% vs -4.2%,P<0.0001),差异具有显著的统计学意义和临床意义。在所有预先指定的亚组中,蛋白尿也呈现出一致的下降趋势。
(3)百时美施贵宝分子胶降解剂3期临床结果积极
3月9日,百时美施贵宝(Bristol Myers Squibb)宣布,3期临床试验SUCCESSOR-2研究取得积极进展。Mezigdomide是一款在研口服E3泛素连接酶cereblon调节药物(CELMoD)。
在该试验中,口服分子胶降解剂mezigdomide联合carfilzomib和dexamethasone(MeziKd),在复发或难治性多发性骨髓瘤(RRMM)患者中,与单用carfilzomib和dexamethasone(Kd)相比,在无进展生存期(PFS)方面显示出统计学显著且具有临床意义的改善。安全性结果与mezigdomide及该联合治疗方案的已知安全性特征一致。研究将继续对患者进行随访。SUCCESSOR-2研究的数据将在未来的医学会议上公布,并将提交给监管机构。
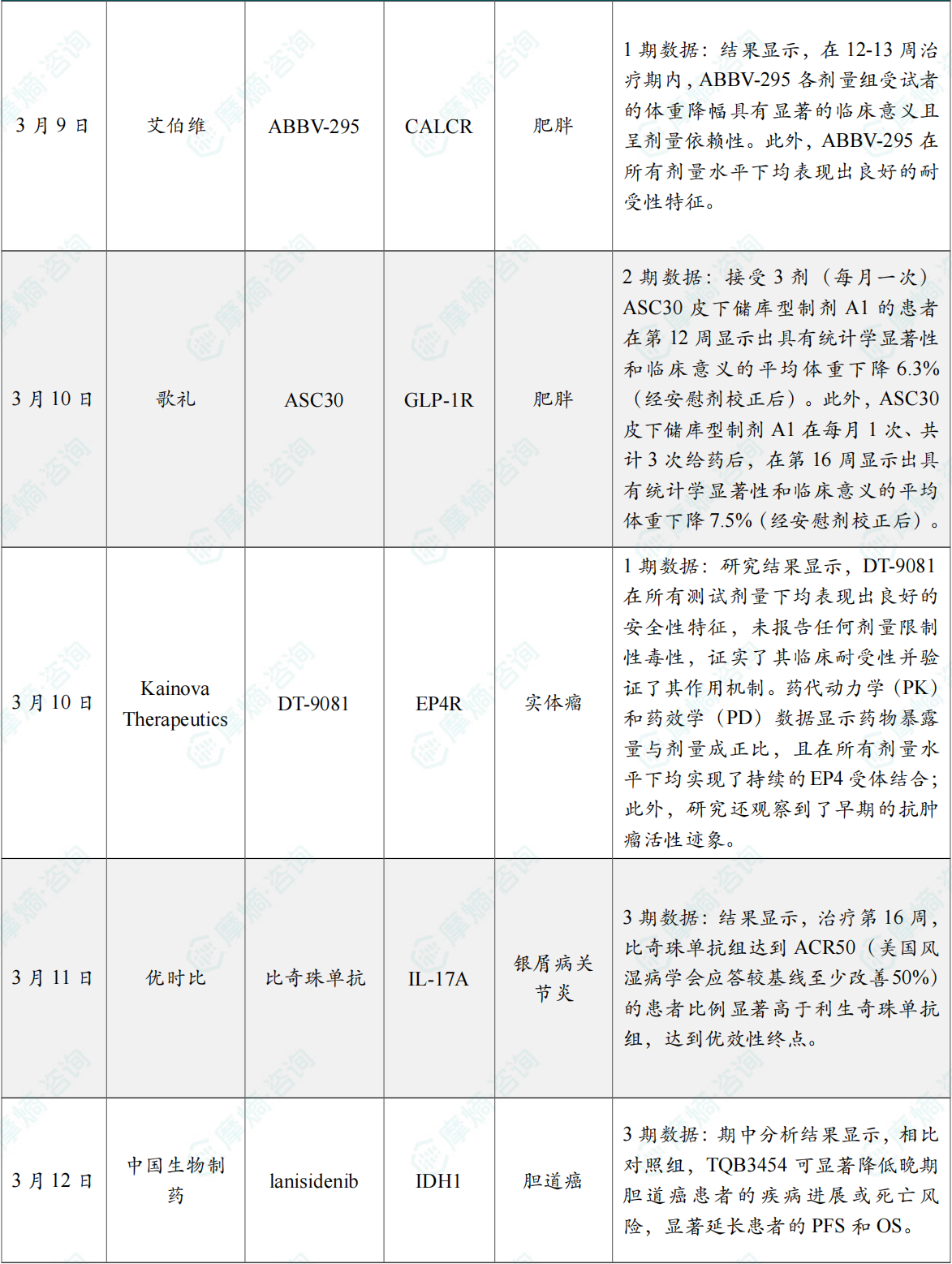
(4)艾伯维长效amylin类似物I期研究取得积极结果
3月9日,艾伯维宣布ABBV-295的I期剂量递增(MAD)研究取得了积极结果。ABBV-295是艾伯维自Gubra引进的一款长效多肽类amylin类似物,可激活amylin受体(AMYR)和降钙素受体(CALCR)。该研究在平均BMI小于30kg/m2的成人受试者中评估了ABBV-295(2-14mg)多个皮下注射方案的安全性、耐受性、药代动力学(PK)和药效动力学(PD)。结果显示,在12-13周治疗期内,ABBV-295各剂量组受试者的体重降幅具有显著的临床意义且呈剂量依赖性。此外,ABBV-295在所有剂量水平下均表现出良好的耐受性特征。
(5)歌礼小分子GLP-1R激动剂美国2期研究获积极结果,治疗肥胖
3月10日,歌礼宣布,其小分子GLP-1受体(GLP-1R)激动剂ASC30皮下储库型(depot)制剂针对肥胖适应症的美国2期24周研究(NCT06679959)取得积极顶线结果。三个队列共入组65名受试者,采用两种制剂(A1和A2)给药,所有受试者均为肥胖受试者或伴有至少一种体重相关合并症的超重受试者。
该2期研究达到了其主要终点,接受3剂(每月一次)ASC30皮下储库型制剂A1的患者在第12周显示出具有统计学显著性和临床意义的平均体重下降6.3%(经安慰剂校正后)。此外,ASC30皮下储库型制剂A1在每月1次、共计3次给药后,在第16周显示出具有统计学显著性和临床意义的平均体重下降7.5%(经安慰剂校正后)。
(6)Kainova Therapeutics公布DT-9081 1期临床试验积极结果
3月10日,Kainova Therapeutics公司宣布,其用于治疗晚期、复发性和转移性实体瘤患者的候选药物DT-9081取得了积极的1期临床试验结果。
DT-9081是一款潜在“best-in-class”的口服小分子EP4受体拮抗剂,旨在通过阻断由COX-2阳性肿瘤产生的前列腺素E2(PGE2)所介导的免疫抑制,恢复免疫功能正常环境并支持免疫再激活,从而提升包括化疗和某些免疫检查点抑制剂在内的抗癌治疗效果。临床前研究显示,在三阴性乳腺癌、肉瘤和结直肠癌模型中,DT-9081无论是单药还是与化疗或免疫检查点抑制剂联合使用,均具有显著的抗肿瘤效果。
研究结果显示,DT-9081在所有测试剂量下均表现出良好的安全性特征,未报告任何剂量限制性毒性,证实了其临床耐受性并验证了其作用机制。药代动力学(PK)和药效学(PD)数据显示药物暴露量与剂量成正比,且在所有剂量水平下均实现了持续的EP4受体结合;此外,研究还观察到了早期的抗肿瘤活性迹象。这些发现进一步支持了DT-9081用于提高患者对免疫检查点抑制剂治疗反应的潜力。
(7)优时比IL-17A/F单抗一项III期临床成功,头对头打败利生奇珠单抗
3月11日,优时比(UCB)宣布比奇珠单抗(Bimekizumab,商品名:Bimzelx)对比利生奇珠单抗(商品名:Skyrizi)治疗银屑病关节炎(PsA)的头对头III期临床(BE BOLD)达到了主要终点。
结果显示,治疗第16周,比奇珠单抗组达到ACR50(美国风湿病学会应答较基线至少改善50%)的患者比例显著高于利生奇珠单抗组,达到优效性终点。这是首次有生物制剂在III期研究中证明优效于利生奇珠单抗。同时,这也是比奇珠单抗第四项取得优效性结果的头对头III期临床,前三项为BE VIVID(对比乌司奴单抗)、BE RADIANT(对比司库奇尤单抗)、BE SURE(对比阿达木单抗)。
(8)中国生物制药IDH1抑制剂III期研究成功
3月12日,中国生物制药宣布IDH1抑制剂TQB3454治疗伴IDH1突变晚期胆道癌的III期临床研究(TQB3454-III-01)已完成方案预设的期中分析,独立数据监查委员会(IDMC)判定主要研究终点无进展生存期(PFS)、总生存期(OS)均达到方案预设的优效界值。
中国生物制药已与CDE就该适应症的上市申请进行沟通,并获得CDE书面同意,将于近期递交上市申请。这是全球第2个、国内第1个IDH1抑制剂在胆道癌取得成功的III期临床研究,同时也是第一个完成III期研究的国产IDH1抑制剂。
期中分析结果显示,相比对照组,TQB3454可显著降低晚期胆道癌患者的疾病进展或死亡风险,显著延长患者的PFS和OS。其安全性数据与已知风险一致,未发现新的安全性信号。中国生物制药计划于今年开展的国际权威学术大会公布详细研究数据。
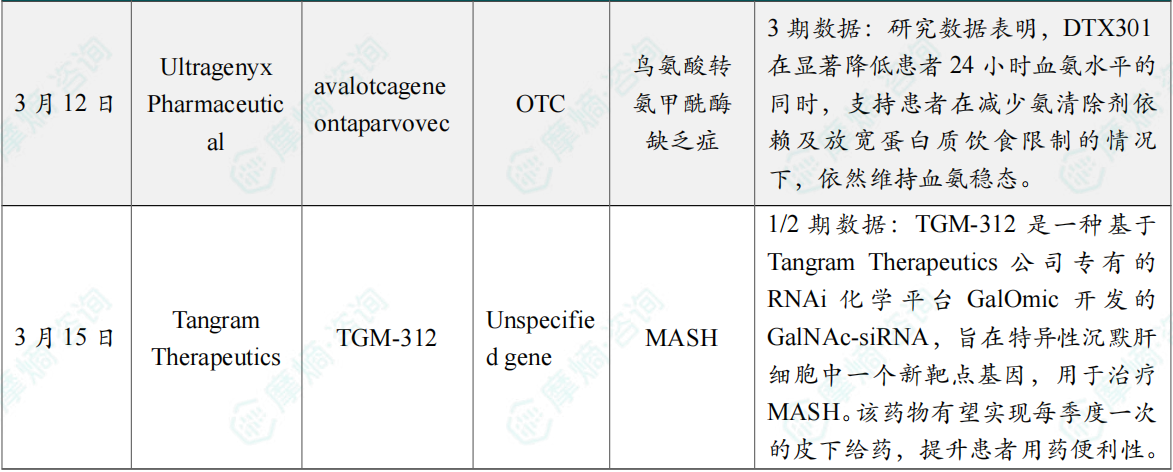
(9)AAV基因疗法DTX301 III期临床成功,治疗罕见病OTC缺乏症
3月12日,Ultragenyx Pharmaceutical宣布其用于治疗鸟氨酸氨甲酰基转移酶(OTC)缺乏症的在研AAV8基因疗法 DTX301,在名为 “Enh3ance” 的III期临床研究中,取得了积极的36周顶线数据。
数据显示,在第36周,DTX301治疗组(18人)的24小时血浆氨曲线下面积(AUC0-24)较安慰剂组(19人)实现了18%的显著降低(p=0.018)。值得一提的是,在基线时因当前标准治疗(药物+饮食控制)仍存在血氨异常的9名患者中,有8人在接受DTX301治疗后,血氨水平迅速降至正常,并在整个治疗期间基本维持在正常范围内!治疗组在第6周时就观察到了血氨的快速下降,展现出了极快的起效速度。完整数据预计将于2027年上半年公布。
(10)TGM-312 1/2期临床试验完成首例受试者给药
3月15日,Tangram Therapeutics公司宣布,其主打候选药物TGM-312的1/2期临床试验已完成首例受试者给药。
TGM-312是一种基于Tangram Therapeutics公司专有的RNAi化学平台GalOmic开发的GalNAc-siRNA,旨在特异性沉默肝细胞中一个新靶点基因,用于治疗MASH。该药物有望实现每季度一次的皮下给药,提升患者用药便利性。
在具有高度转化性的Gubra-Amylin NASH饮食诱导肥胖(GAN-DIO)小鼠模型的临床前研究中,TGM-312单药或与已获批及在研MASH疗法联用,均能显著降低NAFLD活动评分(NAS)、减轻肝脏炎症并减缓纤维化进程。
同期事件:
1. 2026年第11周03.09-03.15国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第11周03.09-03.15国内仿制药/生物类似物申报/审批数据分析
3. 2026年第11周03.09-03.15国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.03.09-2026.03.15) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论