
3月19日,华海药业发布公告,宣布其子公司上海华奥泰生物药业的1类新药HB0025注射液联合化疗一线治疗晚期/复发子宫内膜癌的临床研究,已通过与国家药品监督管理局药品审评中心(CDE)的Ⅱ/Ⅲ期衔接沟通,将正式启动III期临床试验。截至目前,华海药业在该项目的累计研发投入已达约3.42亿元。

截图来源:企业公告
HB0025是由华海药业旗下华奥泰自主研发的抗PD-L1/VEGF双特异性融合蛋白。其创新性在于可同时靶向肿瘤免疫逃逸通路PD-L1与肿瘤血管生成通路VEGF,通过“免疫增强+抗血管”双重机制协同发挥抗肿瘤作用。
该药物设计旨在实现对两个靶点的高亲和力结合,从而协同调控肿瘤免疫微环境与血管生成,有望在多种实体瘤中实现更好的疗效。据摩熵医药数据库显示,2025年前三季度,抗肿瘤药物及免疫机能调节药物(化药或生物药)在全终端医院市场的销售总额超1400亿元。
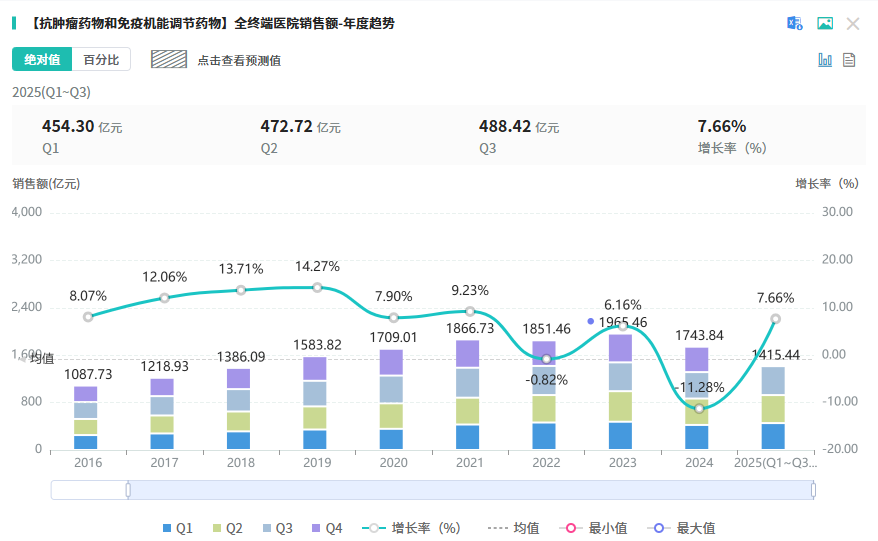
查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
本次启动的III期临床试验,将针对晚期/复发子宫内膜癌患者,重点评估HB0025注射液联合化疗的治疗效果、安全性及耐受性。目前,国内外尚无完全同类机制产品上市,该研究有望为这类患者提供新的治疗选择。
除子宫内膜癌外,HB0025的临床试验布局广泛,多个适应症研究正在同步推进中,涵盖非小细胞肺癌(鳞状/非鳞状)、结直肠癌、三阴乳腺癌等多种高发实体瘤,显示出该药物广阔的临床应用潜力。
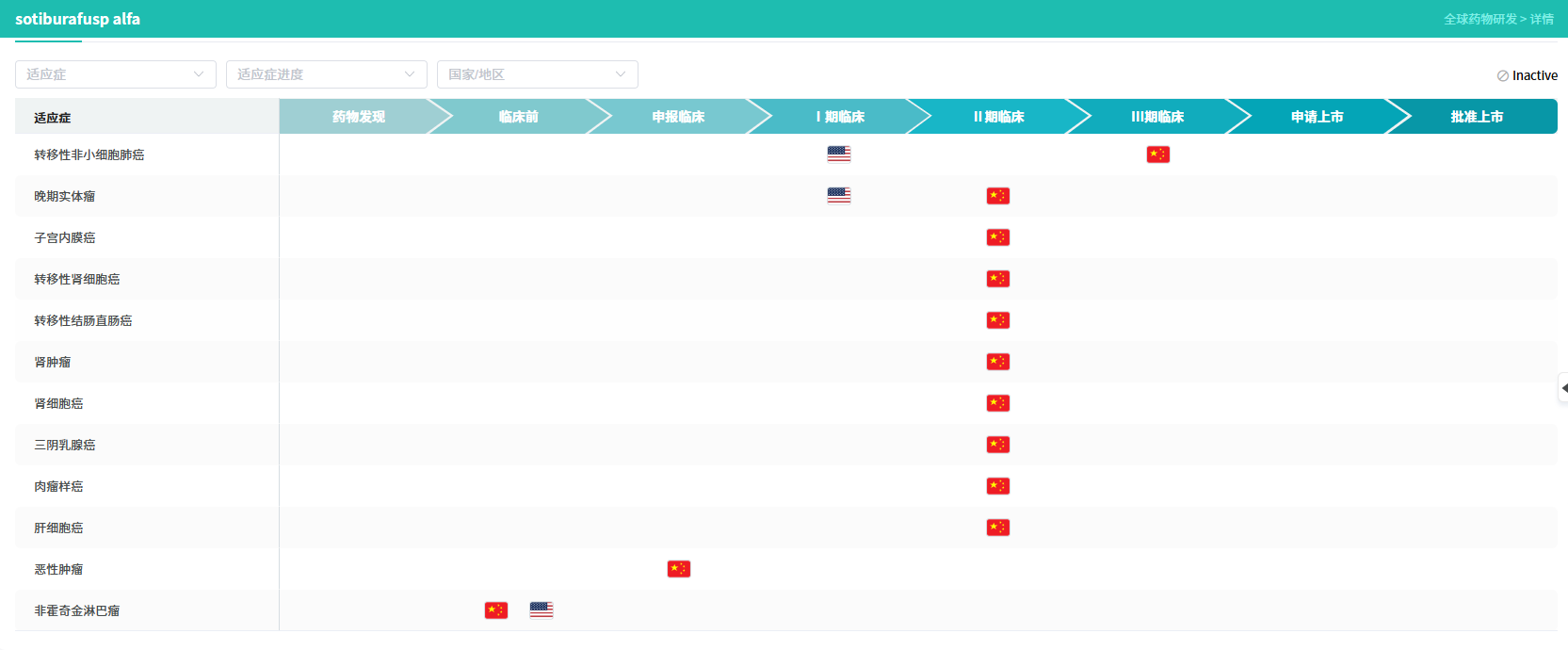
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
截至公告日,华海药业在HB0025项目上的累计研发投入已达约3.42亿元,体现了公司对该创新管线的持续投入与信心。
在创新药领域,华海药业将创新管线研发与拓展作为核心战略,持续加大资源投入。截至目前,公司已取得阶段性战略成果,其中有一款1类化药康泰唑胺片新药获批生产。此外有超15款1类新药获批临床,为公司的长远发展筑牢了坚实基础。
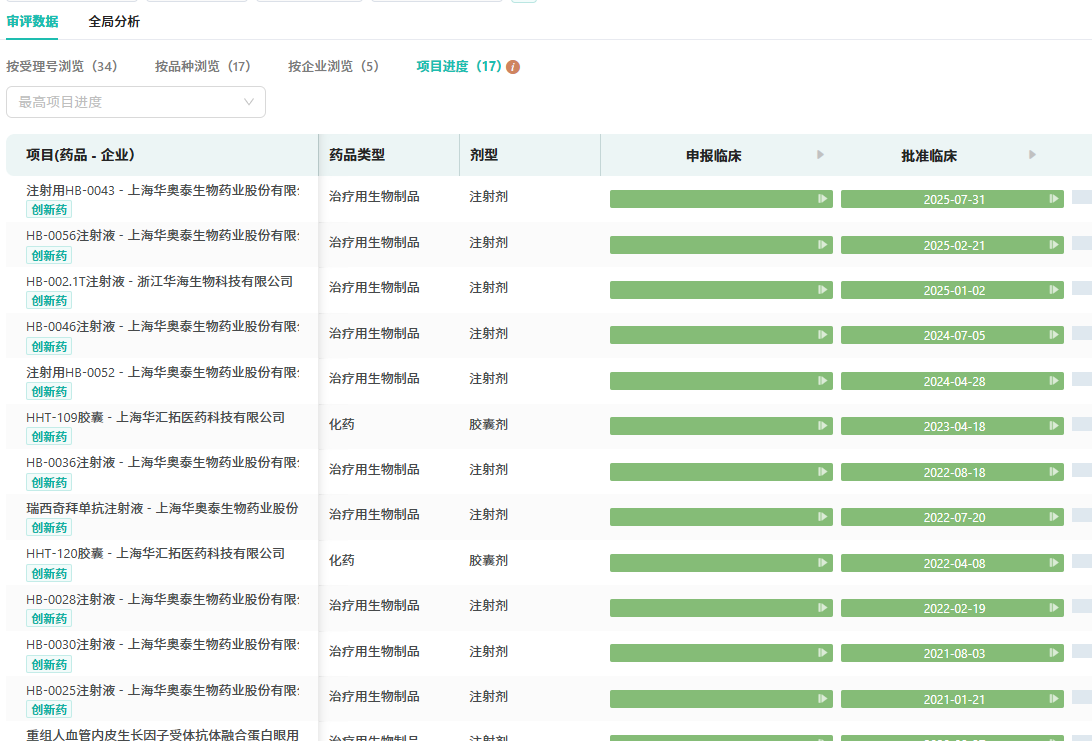
查数据,找摩熵!图源:摩熵医药-中国药品审评数据库
HB0025作为具有全球创新性的双特异性抗体药物,其研发进展不仅有望丰富华海药业在肿瘤治疗领域的产品管线,更将显著提升公司在生物创新药领域的核心竞争力,为长远发展注入新动能。
随着III期临床的正式启动,HB0025的上市进程迈出了关键一步,其后续进展值得持续关注。
参考来源:
[1] 企业公告/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 出海破卷!华海药业加巴喷丁胶囊获美国FDA批准,870万研发投入切入1.5亿美金神经痛市场
2. 华海药业入局艾伯维重磅药盐酸卡利拉嗪胶囊首仿争夺战,百亿精神分裂症市场迎变局
3. 华海药业或成「阿达帕林凝胶」国内第3家过评,热门痤疮药市场迎变局
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论