
3月19日,和誉医药发布公告宣布,其自主研发的高选择性口服小分子FGFR2/3抑制剂ABSK061获得美国食品药品监督管理局(FDA)授予的孤儿药资格认定,用于治疗软骨发育不全(ACH)。

截图来源:企业公告
这是继近期获FDA罕见儿科疾病(RPD)资格认定后,ABSK061全球开发进程中的又一重要里程碑,为其未来的商业化前景与临床价值增添了重磅砝码。
一、孤儿药资格加持,市场独占与政策红利可期
孤儿药资格认定是FDA为激励针对罕见病(美国患者人数少于20万)的创新疗法开发而设立的关键政策。此次ABSK061获得认定,不仅彰显了FDA对其解决未满足临床需求潜力的认可,更将带来一系列实质性利好:包括符合条件临床研究的税费抵免、新药上市申请(NDA)用户费减免,以及一旦获批后在美国市场享有的七年独家销售权。这些政策组合拳将显著降低研发与注册成本,并为其构筑坚实的市场护城河。
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
ACH是一种因FGFR3基因功能获得性突变引起的罕见遗传性骨骼发育疾病,表现为严重的生长发育障碍,目前临床上存在巨大的未满足治疗需求。其核心发病机制在于FGFR3信号通路过度激活,抑制软骨内成骨。因此,靶向抑制FGFR3成为极具前景的治疗策略。
二、高选择性口服抑制剂直击疾病核心机制
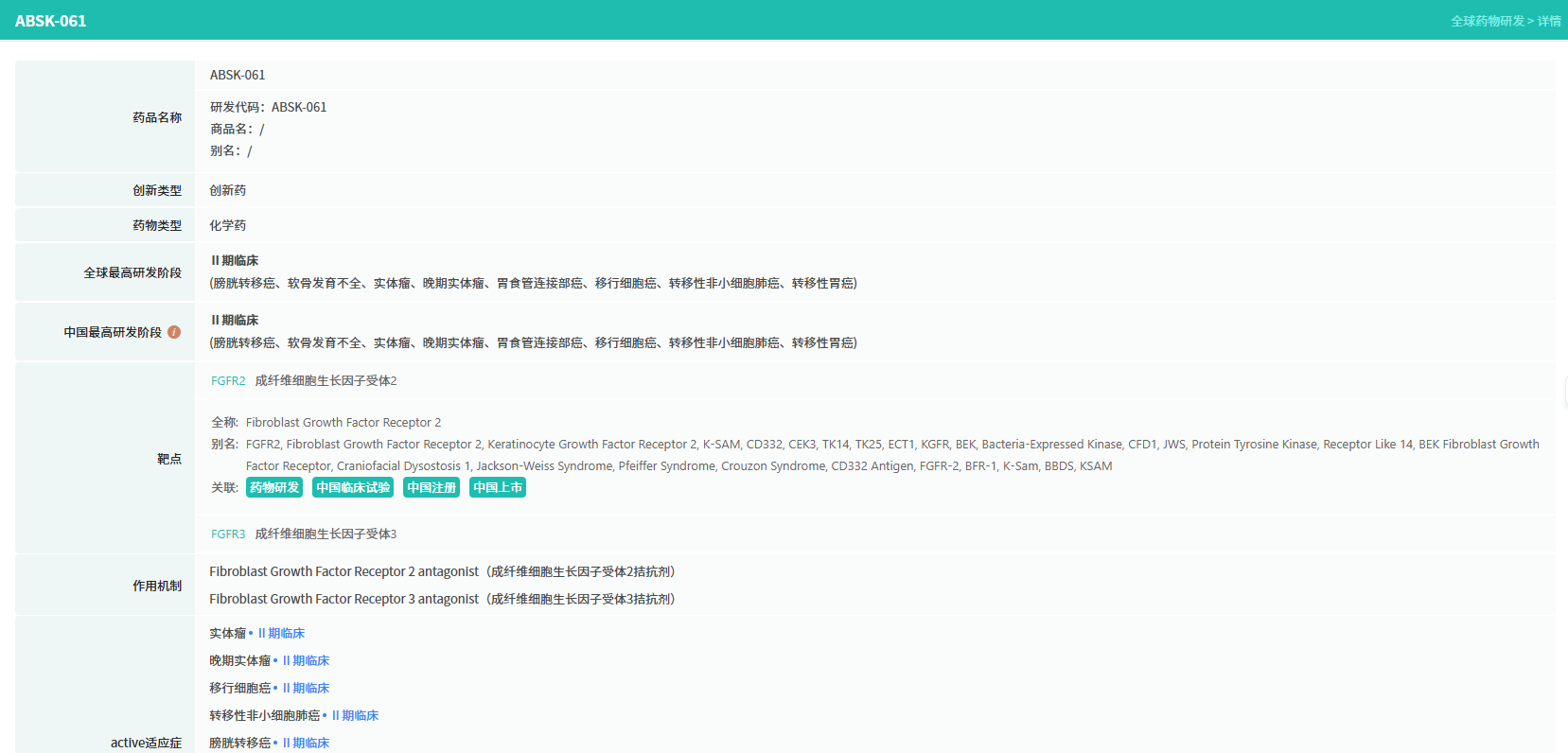
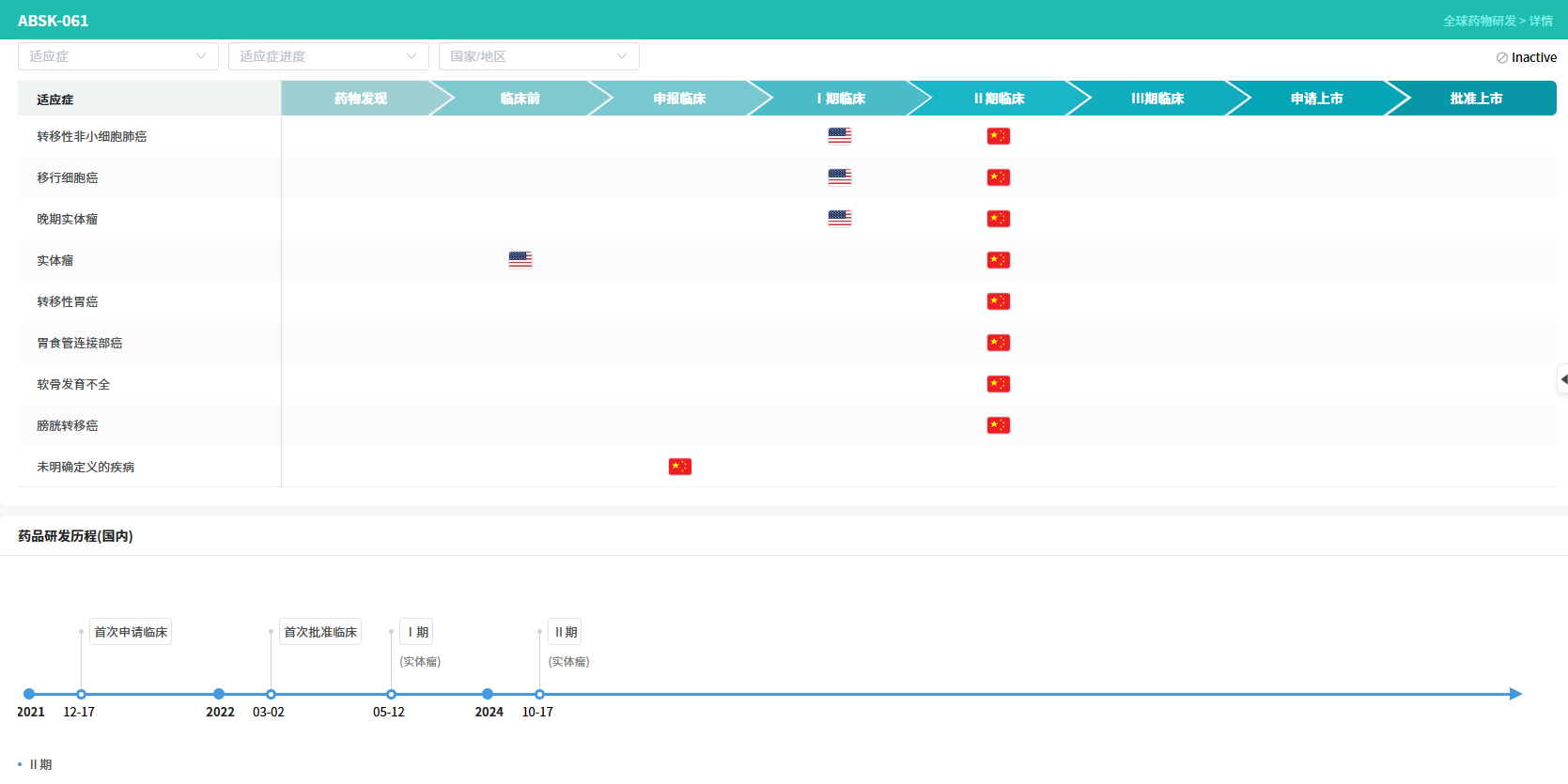
据摩熵医药数据库显示,ABSK061是和誉医药自主研发的一款旨在高选择性抑制FGFR2及FGFR3的口服小分子抑制剂。在国内,该药于2021年12月首次申请临床,次年3月获批,2024年实体瘤进入Ⅱ期临床。临床前研究数据表明,ABSK061在抑制靶点活性方面表现出强效性和高选择性,并具备良好的药代动力学特征与潜在的安全性优势。口服给药的方式有望极大提升患者(尤其是儿童群体)的用药便利性和长期治疗依从性,凸显了其作为ACH患者,特别是儿童及青少年患者潜在优选治疗方案的价值。
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
目前,ABSK061正在开展一项针对3-12岁ACH患儿的国际多中心II期临床试验,以评估其有效性、安全性、耐受性及药代动力学特征。该研究已于2025年12月在中国完成首例患者给药,初步数据预计将于2026年下半年公布,进展备受业界关注。
从FGFR4抑制剂ABSK011(依帕戈替尼)到如今的FGFR2/3抑制剂ABSK061,和誉医药在FGFR靶点领域的管线布局正持续深化与拓展。此次孤儿药资格的获得,不仅加速了ABSK061的全球化开发步伐,也进一步巩固了公司在精准肿瘤学及罕见病治疗领域的创新地位。
参考来源:
[1] 企业公告/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 1类创新药「盐酸匹米替尼胶囊」获批上市用于TGCT治疗,和誉医药与默克合作斩获巨额收益
2. 和誉医药ABSK141片获CDE、FDA双重认可,攻克晚期实体瘤KRAS G12D突变难题
3. 和誉医药与默克深度合作:8500万美元行权费落定,匹米替尼领航CSF-1R抑制剂赛道新征程
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论