
3月24日,石药集团宣布,其与康宁杰瑞合作开发的HER2双特异性抗体药物安尼妥单抗(KN026),联合石药集团自研白蛋白结合型多西他赛(HB1801)及化疗,用于乳腺癌辅助治疗的Ⅲ期临床研究(KN026-007)已完成首例患者给药。该项研究是目前全球范围内唯一针对“未接受过新辅助治疗、术后高复发风险的HER2阳性乳腺癌辅助治疗”的在研III期临床,有望填补该治疗领域的重大空白。

截图来源:企业官微
一、锁定术后高危患者,冲击辅助治疗新标准
KN026-007是一项随机、对照、开放、多中心III期临床研究,计划纳入约1800例术后经组织学确诊、区域淋巴结阳性数量≥4个的可切除HER2阳性乳腺癌患者。研究旨在头对头比较“安尼妥单抗+白蛋白结合型多西他赛+化疗”方案与当前标准辅助治疗方案——“曲妥珠单抗+帕妥珠单抗+化疗”的疗效与安全性。
研究的主要终点为研究者评估的无浸润性疾病生存期(iDFS),次要终点涵盖多项生存获益与安全性指标。该研究若获得积极结果,有望为术后高复发风险的HER2阳性乳腺癌患者提供一种新型、高效的辅助治疗选择,甚至可能改写临床治疗路径。
二、双抗联用自研化疗,石药创新组合优势凸显
此次临床方案的核心在于“双特异性抗体+创新化疗药物”的协同组合:
安尼妥单抗是康宁杰瑞采用具有自主知识产权Fc异二聚体平台技术(CRIB)开发的一款HER2双特异性抗体,可同时结合HER2的两个非重叠表位,阻断HER2信号传导,并通过抗体诱导的受体聚集,增强抗体依赖的细胞毒性(ADCC)和补体依赖的细胞毒性(CDC)效应,同时下调细胞表面HER2受体表达。
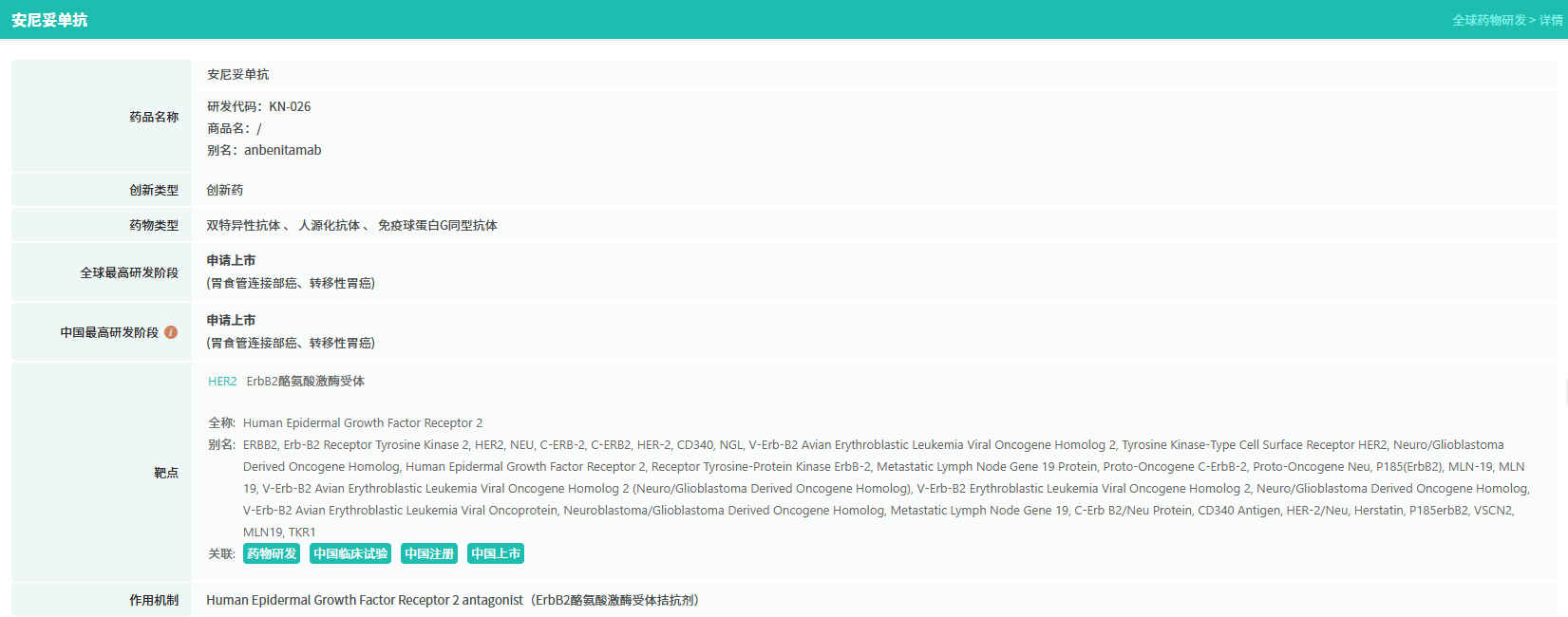
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
该药物研发进展迅速:2025年9月,其在HER2阳性胃癌适应症的首个新药上市申请(NDA)已获国家药品监督管理局(NMPA)受理。目前,针对二线及以上HER2阳性胃癌/胃-食管结合部癌、晚期一线HER2阳性乳腺癌、HER2阳性乳腺癌新辅助等适应症的多项注册临床研究也在积极推进中。此外,安尼妥单抗已获得美国FDA授予的孤儿药资格(用于HER2阳性或低表达胃癌),并获NMPA突破性疗法认定。
HB1801是石药集团自主研发的白蛋白结合型多西他赛,具有靶向递送潜力,有望提升疗效并降低毒性。
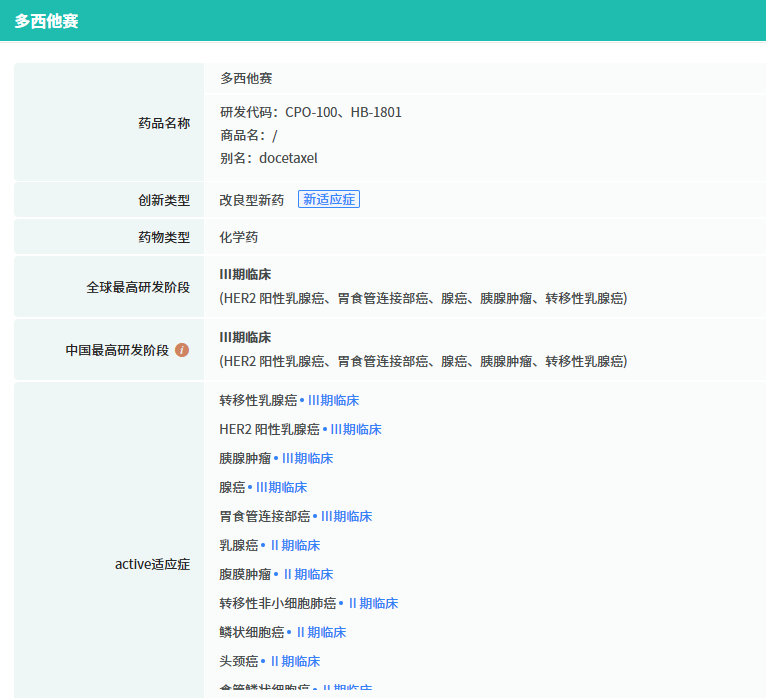
查数据,找摩熵!截图来源:全球药物研发数据库
2021年8月,石药集团通过其全资子公司上海津曼特生物科技,从康宁杰瑞获得了安尼妥单抗在中国内地(不包括港澳台地区)在乳腺癌、胃癌适应症上的排他性开发与商业化权益。此次Ⅲ期临床的启动,不仅是该合作的重要进展,也体现了石药集团在肿瘤创新疗法开发上“内外协同、自主联合”的深度布局。
三、结语
石药集团此次启动的KN026-007研究,聚焦于临床需求迫切但缺乏针对性治疗方案的术后高复发风险HER2阳性乳腺癌人群,凭借具有全球差异化的临床设计与“双抗+创新化疗”的联合策略,展现出冲击该领域治疗标准的潜力。若临床成功,不仅将强化石药在乳腺癌治疗领域的战略地位,更可能为全球HER2阳性乳腺癌的辅助治疗提供首个针对该高危人群的专属解决方案,进一步巩固其从合作引进到自主创新全链条的研发与商业化能力。
参考来源:
[1] 企业官微/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 康宁杰瑞/石药集团重磅新药JSKN003获批Ⅲ期临床!HER2双抗ADC剑指晚期结直肠癌未满足需求
2. 石药集团创新药大突破:降糖新复方、减重双靶点、降压新策略齐获临床批件
3. 石药集团创新药双突破:SYH2053剑指高胆固醇血症,SYH9089填补超长效术后镇痛空白!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论