
2月14日,医药行业传来重磅消息:正大天晴 自主研发的1类创新药——贝莫苏拜单抗注射液,成功获批新适应症,将用于不可切除Ⅲ期非小细胞肺癌(NSCLC)患者放化疗后的巩固治疗。
这一获批意义非凡,它不仅是 贝莫苏拜单抗 在国内斩获的第四个适应症,更使其跻身全球前列,成为继 度伐利尤单抗、舒格利单抗 之后,全球第三款应用于该治疗场景的PD - L1抑制剂,为众多肺癌患者带来了新的希望。
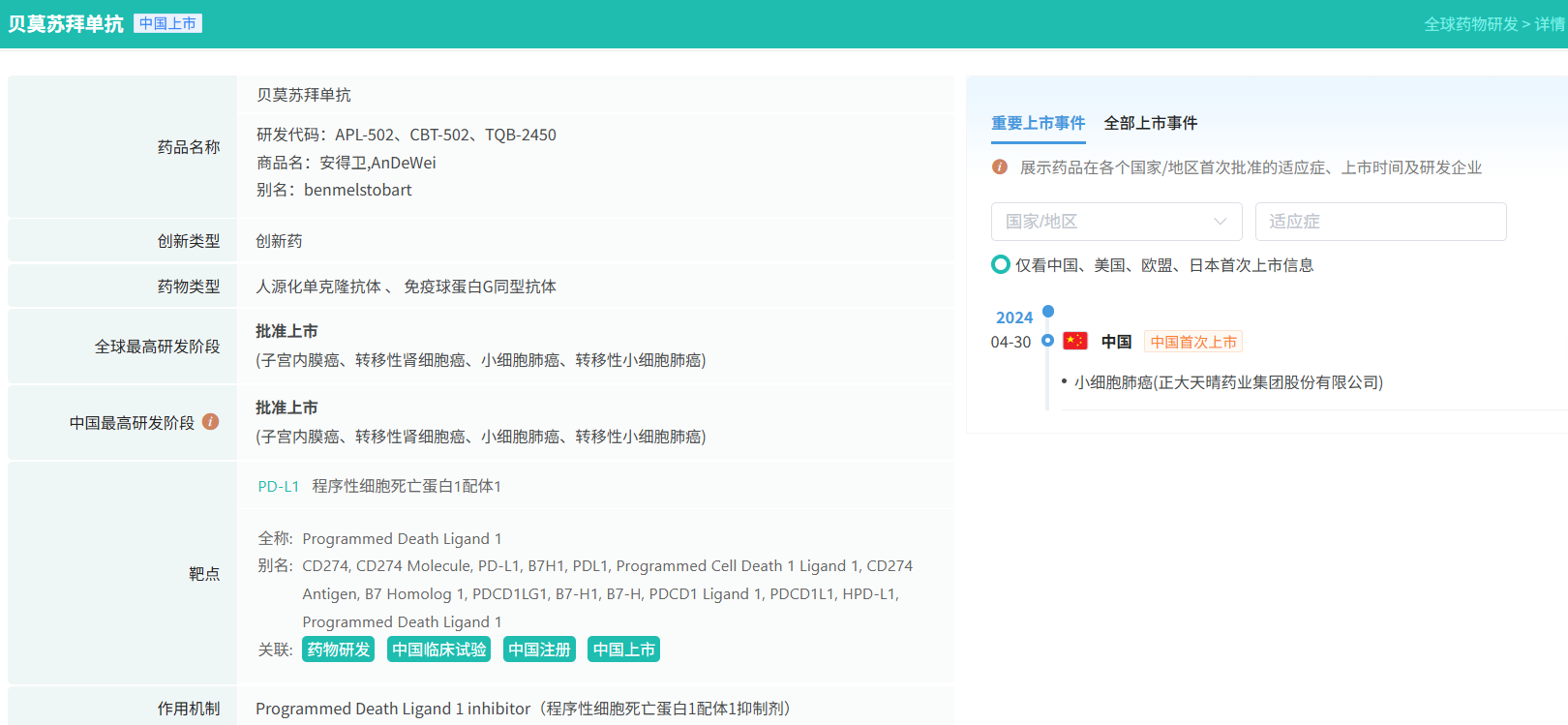
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
获批依据:R-ALPS研究阳性结果奠定基础
此次新适应症的获批,得益于R - ALPS研究取得的令人瞩目的阳性结果。该研究聚焦于同步/序贯放化疗后病情未进展的局部晚期/不可切除的Ⅲ期非小细胞肺癌(NSCLC)患者。在研究过程中,129例患者接受 贝莫苏拜单抗 巩固治疗,132例患者则接受安慰剂治疗直至疾病出现进展。研究设定的主要终点是由盲态独立中心审查(BICR)评估的无进展生存期(PFS)。
研究数据令人振奋:经过中位19.4个月的随访,接受 贝莫苏拜单抗 巩固治疗的患者中位PFS达到9.69个月,而安慰剂组仅为4.17个月(HR = 0.53,95% CI 0.39 - 0.72,P < 0.0001)。这意味着,使用 贝莫苏拜单抗 巩固治疗可使患者的疾病进展或死亡风险降低47%。此外,预设的亚组分析(涵盖是否吸烟、前序治疗方式为同步/序贯等情况)结果显示,各亚组与ITT人群的获益趋势高度一致,充分彰显了该治疗方案的广泛适用性。
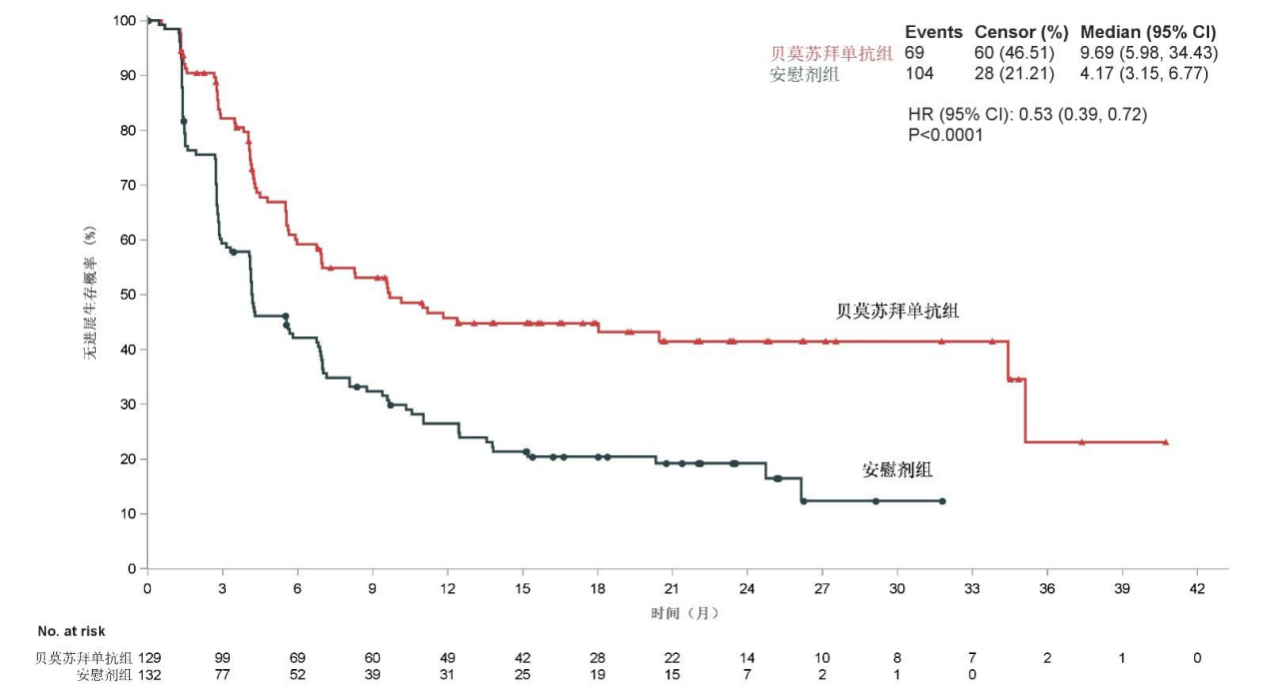
在总生存期(OS)方面,虽然目前数据尚未成熟,中位OS尚未达到,但两组风险比HR = 0.76(0.50,1.14),贝莫苏拜单抗 巩固治疗组已初步显现出OS获益趋势,这无疑为患者的长期生存带来了更多期待。安全性数据同样可圈可点,≥3级治疗相关不良事件发生率在贝莫苏拜单抗组为29.4%,安慰剂组为19.7%,相对较低的不良反应发生率,为患者长期治疗的依从性提供了有力保障。
适应症布局:多领域拓展,彰显创新实力
目前,贝莫苏拜单抗 在国内已获批4项适应症,此前已获批的适应症分别为联合安罗替尼一线治疗广泛期小细胞肺癌、复发性或转移性子宫内膜癌以及一线治疗晚期不可切除或转移性肾细胞癌。这些适应症的获批,充分体现了贝莫苏拜单抗在不同肿瘤治疗领域的广泛适用性和强大疗效。

查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
不仅如此,贝莫苏拜单抗 的研发脚步并未停歇。目前,联合 安罗替尼(得福组合)一线治疗鳞状非小细胞肺癌,以及用于晚期或不可切除腺泡状软组织肉瘤的两项适应症正处于上市审评阶段。一旦获批,将进一步丰富 贝莫苏拜单抗 的适应症版图,为更多肿瘤患者提供有效的治疗选择,也再次彰显了正大天晴在创新药研发领域的雄厚实力和坚定决心。
随着 贝莫苏拜单抗 新适应症的获批,我们有理由相信,在未来的肿瘤治疗领域,它将发挥越来越重要的作用,为更多患者带来生存的希望和生活的质量提升。
参考来源:
[1] CDE/NMPA官网
[2] 企业官方披露
[3] 摩熵医药(原药融云)数据库
扩展阅读:
1. 正大天晴的贝莫苏拜单抗拟优先审评,治疗腺泡状软组织肉瘤!
2. 正大天晴贝莫苏拜单抗III期临床研究突破:NSCLC巩固治疗迎来优效进展
3. 正大天晴PD-L1单抗贝莫苏拜获批!奥赛康药业拿下注射用硫酸艾沙康唑首仿...
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论