
5月9日,据NMPA 官网公示,正大天晴 1 类创新药 PD-L1 单抗贝莫苏拜单抗(TQB2450)注射液(受理号:CXSS2300003)获批上市,联合盐酸安罗替尼胶囊、卡铂和依托泊苷用于广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。同日江苏奥赛康药业的注射用硫酸艾沙康唑(受理号:CYHS2200985)仿制药获批上市并视同过评,拿下国内首仿。

截图来源:NMPA
正大天晴PD-L1单抗获批,国产再添新力
贝莫苏拜单抗是正大天晴自主研发的一款 PD-L1 单克隆抗体。据药融云数据库统计,这款药物在2017年5月启动临床试验申请,同年10月获得临床试验批准,并于2018年4月首次公示启动临床阶段。经过多轮严格审批与临床验证,贝莫苏拜单抗在去年1月递交了上市申请。

截图来源:药融云全球药物研发数据库
在全球市场来看,PD-L1单抗领域竞争激烈,此前有7 款 PD-L1 单抗(创新药)获批上市,包括阿斯利康的度伐利尤单抗、罗氏的阿替利珠单抗和默沙东的Avelumab以及4款国产PD-L1单抗,康宁杰瑞的恩沃利单抗、基石药业的舒格利单抗等国产药物先后获批上市。
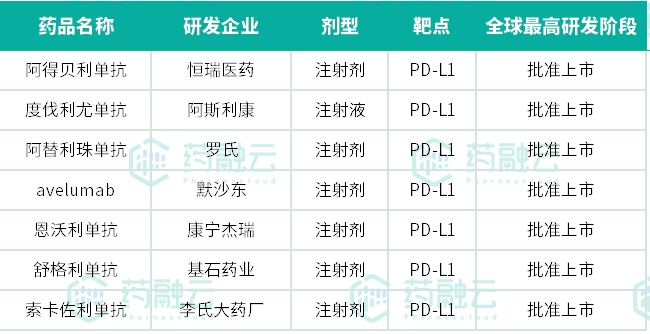
截图来源:药融云全球药物研发数据库
PD-L1单抗市场自2021年起便迎来了爆发式增长,此次正大天晴的贝莫苏拜单抗的加入,无疑为国产PD-L1单抗市场注入了新的活力。
近1亿元重磅注射剂,奥赛康拿下首仿
艾沙康唑是由Basilea开发的一款广谱的新型三唑类抗菌药物,主要用于18周岁及以上患者侵袭性曲霉菌病和侵袭性毛霉菌病的治疗。相关研究表明,硫酸艾沙康唑疗效不亚于目前抗真菌药物“老大”伏立康唑,而不良反应较伏立康唑更低。注射用硫酸艾沙康唑于2022年6月在国内上市,同年该品种纳入了医保乙类品种目录,随后迎来医院市场的快速放量。据药融云数据显示,注射用硫酸艾沙康唑在2023年(截止Q3)全国院内市场销售额逼近1亿元。
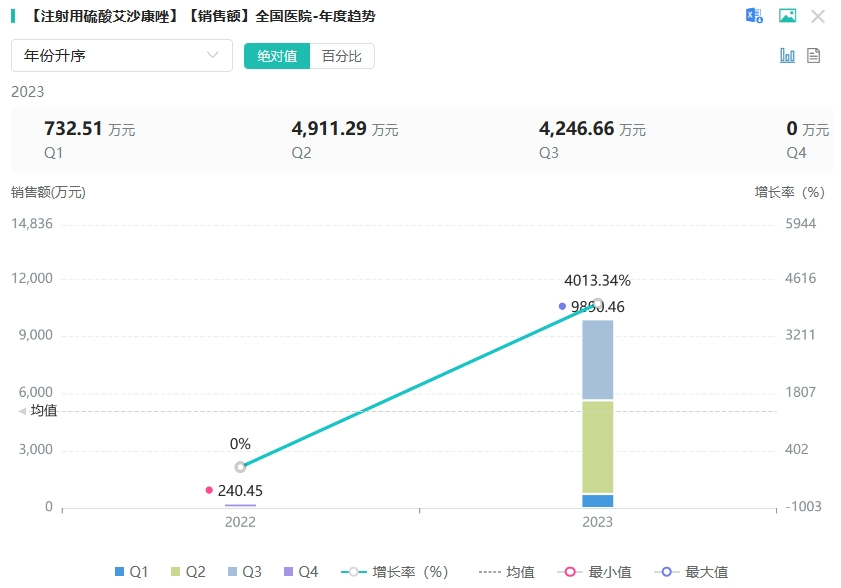
截图来源:药融云全国医院销售数据库
据药融云数据库统计,2022年6月,辉瑞的注射用硫酸艾沙康唑成功获得进口批准。此前,国内市场尚无国产药企的注射用硫酸艾沙康唑获批。此次江苏奥赛康药业的注射用硫酸艾沙康唑仿制药获批并拿下国内首仿。
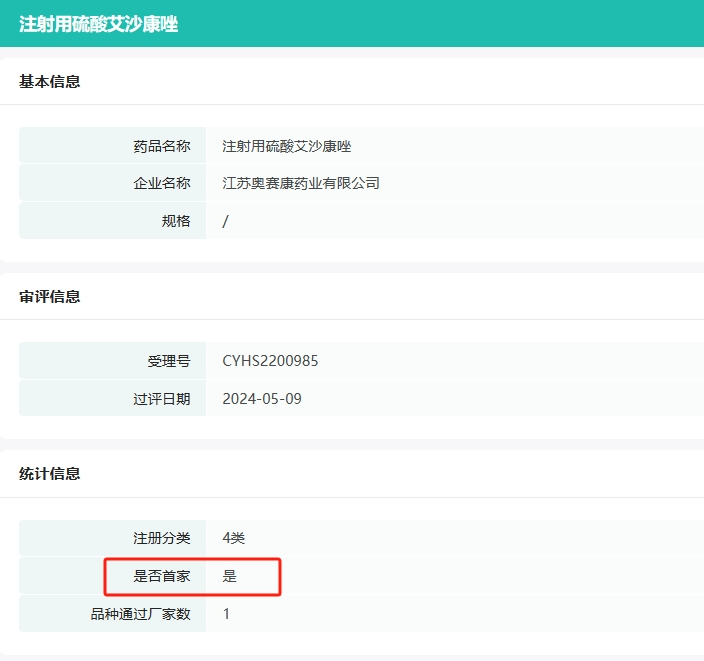
截图来源:药融云过评药品汇总数据库
在仿制药布局领域,注射用硫酸艾沙康唑有华北制药、四川宏明博思药业、山东新华制药、山东齐都药业、齐鲁制药等13家药企提交了仿制申请,均在审评审批中。

截图来源:药融云中国药品审评数据库
2024年至今,江苏奥赛康药业已有注射用硫酸艾沙康唑、枸橼酸托瑞米芬片、艾曲泊帕乙醇胺片3个品种过评。
推荐阅读:中国新药研发成果斐然:受理数量创新高,PD-L1、EGFR、PD-1稳坐前三甲
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论