
全链条支持创新药发展以“真支持创新、支持真创新、支持差异化创新” 为核心导向,激发企业原始创新活力,平衡创新价值回报与患者用药可及性,推动医药产业高质量发展并更好服务健康中国战略。
为贯彻国务院全链条支持创新药发展的文件精神,系统展示中国创新药从研发到商业化全流程能力建设中的成绩与痛点,2025年E药经理人研究院借助医药产业商业化领域专家的实践经验,构建了“创新药卓越商业生态(OCEID,简称‘奥赛德’)”评估体系。

“奥赛德”评估体系,打破传统商业价值评估仅侧重单一环节的局限,更全面客观评估公司在创新药商业化全流程的综合表现,用5个维度、11项可量化指标,覆盖了调研访谈所反映的创新药商业化全流程,包括上市准入、市场准入、终端准入、学术影响、商业表现。
2025年基于“奥赛德”体系,E药经理人研究院历时4个月,通过体系搭建、数据检索、清洗、汇总,最终形成“中国创新药商业卓越Top10榜单(肿瘤治疗领域)”。
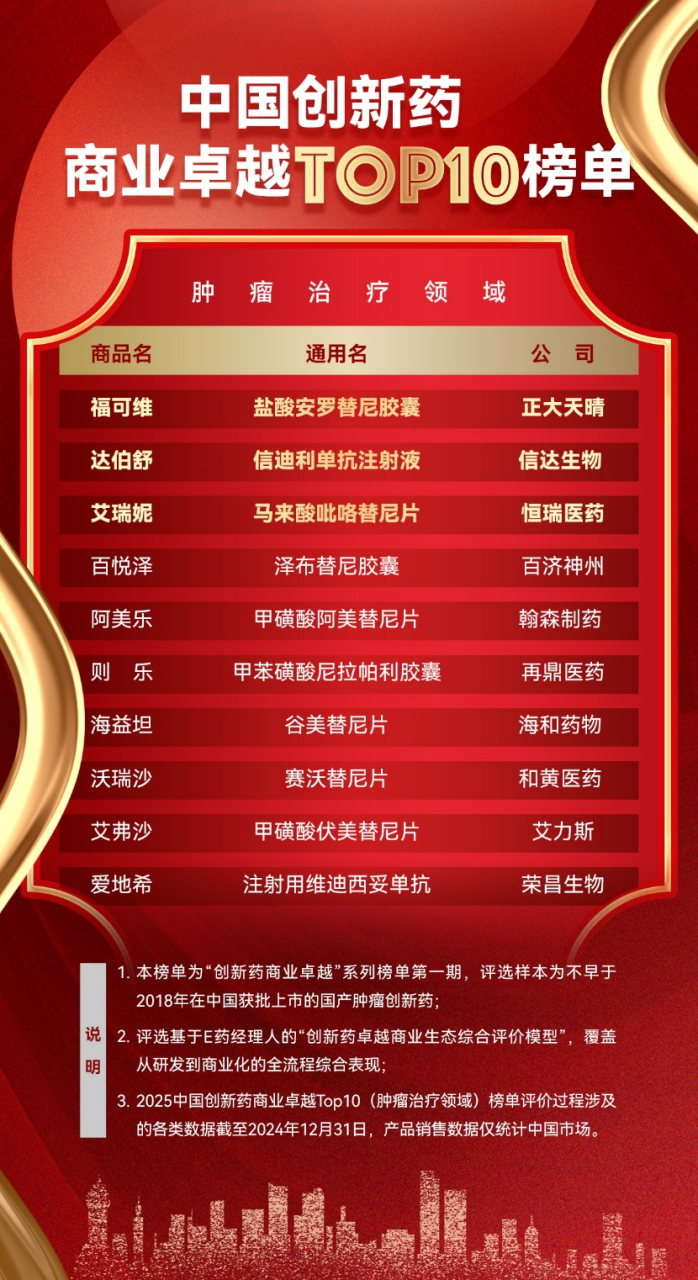
“中国创新药商业卓越Top10榜单(肿瘤治疗领域)”作为医药行业首份聚焦商业卓越生态建设的榜单,其意义不仅在于选出“Top10”,更在于建立了可复制、可迭代的评估框架。
我们希望通过“奥赛德”研究不仅为破解中国创新药“商业化价值困境”提供了诊断工具和实践路径,更从产业层面推动了价值导向的竞争生态形成,为创新药从“中国新”走向“中国优”乃至“全球优”提供了关键支撑框架。
接下来,E药经理人研究院将覆盖更多治疗领域,且随创新药上市加速、政策优化动态调整“奥赛德”体系,并逐步形成中国创新药商业化的“行业标尺”,引导企业从“短期冲销量”转向“长期建生态”,为“研发、商业化、再研发”的正向循环提供支撑。
一、痛点是什么?
中国创新药产业达到了一个结构性拐点,即研发能力已快速提升至国际水平,但商业化的成熟度亟待提升。国产创新药研发和商业化的巨大落差,与中国创新药商业化生态存在密切关系。
过去十年,中国创新药的成果堪称“狂飙突进”。2024年全球首发创新药里,38%来自中国(共39个);2025年上半年,中国首发创新药更达43个,直接超过去年全年总量。
国产创新药正以“量产”速度涌现,可摆在面前的现实是:研发的“高光”,还没完全转化为商业化的“实效”。
历经十年(2015-2024),国产创新药在核心医院市场的份额仅从4.24%增至8.70%,约为782亿元,仅是跨国药企创新药市场份额的40%。不论总体药品市场结构还是创新药市场结构,国产创新药仍有巨大的市场空间。
仿制药时代,商业化就是把药卖出去,创新药远没这么简单。但创新要实现可持续,商业化价值的兑现是必答题,而这道题的答案,已经从一个环节的“单打独斗”,提升至创新药全生命周期价值链的“协同作战”。这恰是跨国药企创新药在中国市场引入创新药后,快速组队、落地,跑通商业化路径的关键。
在构建“奥赛德”评估体系过程中,E药经理人研究院访谈了多家国内外知名药企的商业化领域实战精英,他们既表达了对中国创新药行业快速发展的欢欣鼓舞,对产业政策和政府支持的感谢赞扬,也反映了在创新药商业化实践中遇到的困难及问题。
总体而言,关切集中在如何提升终端市场渠道的畅通性、如何完善创新药价格体系、如何建设创新药多元支付体系、如何确保指南共识的实用性等。
国产创新药商业化最突出的痛点是“最后一公里”的终端准入不通畅。即使各级医保和卫健部门高度重视和积极推动,谈判药品的医疗机构总体配备水平依然较低,新谈判药品落地更加困难。
谈判药品的进院、处方、支付和供应环节存在多个堵点。医疗机构尚未普遍建立与医保谈判匹配的药事会制度,同时医院用药目录品种数控制导致新药进院数量受限。即使药品进院,仍有部分政策限制临床按需开具处方,如公立医院绩效考核的次均费用增幅、基药占比、医疗服务收入占比等,医保费用管理的医保总额控制、DRG/DIP支付政策。
在医疗机构以外,零售药店在通过“双通道”政策承接谈判药品方面也存在诸多困难。“双通道”药店实施高标准、高要求建设,运营成本较高,而谈判药品实施“零加成”销售,导致药店面临投入产出不匹配的困境,运营难以为继。据报道,扬州市一家老牌连锁药店2022年上半年运营“双通道”药品的毛利率仅3.62%。由于缺乏保盈利运行的制度安排,药店经营谈判药品的可持续性存在挑战。
创新药定价模式也是专家们多次提到的问题,医保谈判的逻辑应转向“以真实世界证据为基础,动态确定支付标准”。并建议,创新药是否可先以与医保目录内同类适应症品种的支付标准纳入医保,后续根据真实世界临床试验证据重新评估,实行优效提价,等效维持,劣效退出。这种动态机制既能保证医保基金的合理使用,又能引导以临床价值为导向的创新研发。
在创新药多元支付体系中,专家们认为亟需建立由国家基本医保和市场化运作的商业健康险构成的多元支付体系。
仅以惠民保为代表、存在地域和户籍边界的商保模式难以支撑创新药支付。真正的商保应以市场化为导向,建立直赔机制与独立药品目录,比如可以参考国家医保局2025年即将制定的第一版商业健康保险创新药品目录,并通过税收抵扣与企业激励政策提高参保率。商保体现市场效率,而医保强调社会公平,二者各司其职、共同构建多元支付体系。
此外,国产创新药在进入临床诊疗指南也面临一些挑战,并且指南的实际应用也存在若干问题。
国产创新药的研发上市速度加快,但指南的制定和更新周期相对较长,导致不能及时收录和推荐已上市并具有临床价值的新药。国产创新药与现有标准疗法(SoC)进行头对头比较的临床证据不足,导致指南难以给予高等级推荐。有些情况下,医生如果放弃常用药物而选择指南推荐的创新但尚未普及的疗法,可能会存在面临医疗纠纷的风险,导致其难以快速转变至最新的指南推荐。
数据和访谈反映,中国创新药市场仍面临规模小、商业化价值实现路径不通畅等挑战。因此,基于全链条支持创新药发展的政策内涵,构建一个支撑中国医药创新可持续提升的“创新药卓越商业生态”成为新周期的核心命题。这也是E药经理人研究院构建“奥赛德”评估体系的初衷。
二、解决路径是什么?
访谈中的得出共识是,构建“创新药卓越商业生态”不能仅局限于终端市场销售这一最终结果表现,而应深入探究成因,将创新药商业化视为一项系统工程,拓展至包括上市准入、市场准入、终端准入、学术影响、商业表现等五个环节,覆盖创新药从研发到回报的完整循环。
基于共识,E药经理人以研究“创新药卓越商业生态”为核心锚点,聚焦代表性创新药的综合表现,构建了一套评估相关公司构建“创新药卓越商业生态” (Outstanding Commercial Ecosystem for Innovative Drugs, OCEID,简称“奥赛德”)能力及其现状的研究框架。
E药经理人研究院的“奥赛德”评估体系,包括5个维度:上市准入、市场准入、终端准入、学术影响、商业表现,以及综合科学性、可量化性、数据可得性合理选取的11项指标,再按照维度及指标的相应权重,经计算得到对公司的创新药商业卓越生态情况的客观、量化评估。
从5个维度和11项指标展示出来的具体数据看,“TOP10新药”的全链条商业生态建设,呈现出不同的能力优势,有些在商业成绩实现上得分较高,而有些则监管上市和市场准入环节得分较高;只有少部分全链条能力较为平均。
通过对上榜及候选创新药全链条商业化生态的建设的分析,我们认为:
- 落实全链条支持创新药发展政策,需从“政府主导” 与“多元共治”相结合,激活全生态角色动能;
- 商业化不是“单点突破”,而是“生态价值链合力”的结果;
- 药企必须将创新药商业化视为“系统工程”,打破“唯销量论”,建立内部商业化全链条评估标准,重塑行业价值导向;
- BD热潮下,“自身商业生态”才是创新可持续的“压舱石”;
- 医药创新的可持续,企业需形成“研发速度”与“商业体系”双强格局,创新药才能实现价值最大化。
文章来源:E药经理人
原文链接: https://mp.weixin.qq.com/s/YMkI_kLIe0n4DElRCQ1h4A
扩展阅读:






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论