
创新药物的研发,是使我国由医药大国走向医药强国的必由之路。近年来,随着国家对医药创新政策的持续加码,以及更多科研机构和企业开始将研发重心转向原创新药,尤其是在肿瘤、心血管疾病、神经系统疾病等重大疾病领域,我国的新药研发成果不断涌现。
I类新药受理数量爆炸式增长,生物制品与化学药数量几乎持平
据药融咨询2023年《中国1类新药靶点白皮书》统计,在2018-2021年期间,我国Ⅰ类新药受理数量逐步提高,2022年出现小幅度下降,2023年大幅回升,较2022年上涨45.1%,创近年历史新高。从申报药品类型来看,仍以化学药为主。
2018-2023年I类新药受理数量(按受理号计)
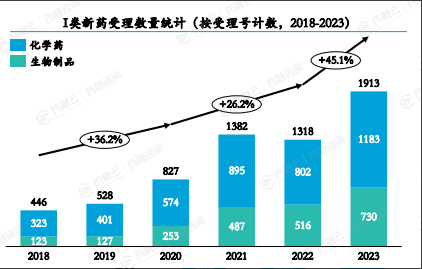
图片来源:药融咨询2023年《中国1类新药靶点白皮书》
同期,Ⅰ类新药涉及的靶点数量整体上升,2021年达到806个。2022年有所回落,但相较于2020年仍有增长,三年CAGR为12.4%。2023年新药涉及靶点数量开始回升,并超过2021年水平。
2018-2022年,获受理I类新药中生物制品数量和占比保持持续增长,2022年生物制品占比超过化药。2023年我国受理I类新药数量爆炸式增长,生物制品数量与化学药数量几乎持平,生物药占比较2018年增长17%。
2018-2023年受理I类新药生物药/化学药占比
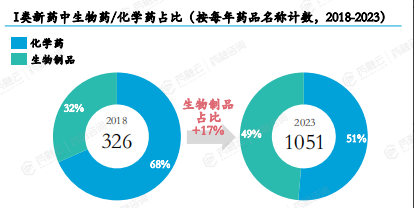
图片来源:药融咨询2023年《中国1类新药靶点白皮书》
I类新药批准上市数量总体保持增长趋势
在2018-2021期间,批准上市的Ⅰ类新药连续快速增长,2018到2021年增长了200%。2022年受各种因素影响,批准上市新药数量首次出现下降,但2023年迅速回升至2021年水平左右。
2023年,批准上市的I类新药共计30款(按药品名称计),其中化学药占比46.7%,生物制品占比53.3%,生物制品数量首次超过化学药。
2019-2023年批准上市I类新药数量
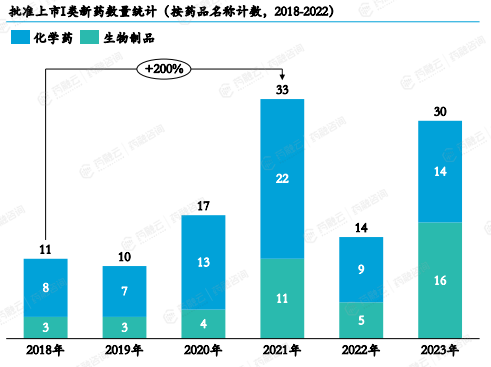
从治疗领域来看,肿瘤领域仍是2023年新药研发最热门的疾病领域,占比51.6%;其次是抗感染领域,占比16.1%。抗肿瘤药物一直是创新药的关注点。
从靶点分布来看,在批准上市I类新药中,排名靠前的靶点中EGFR、PD-L1和c-Met为肿瘤相关靶点,EPOR是血液和造血系统用药,DPP4是消化和代谢系统用药。
2023年批准上市I类新药靶点分布(按药品名称计数)
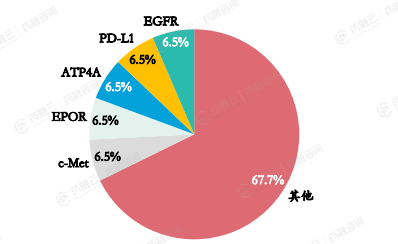
数据来源:药融云数据库
1类新药TOP3热门靶点:PD-L1、EGFR和PD-1
在2018至2023年期间,我国新药受理数量2858个,涉及637个靶点。与2017至2022年相比,PD-L1、EGFR和PD-1这三大靶点继续稳坐热门靶点的前三甲。
值得注意的是,CD19靶点的关注度持续攀升,相关药品数量从2017至2022年间的38个增长到50个,成功超越VEGFR和HER2,跻身热门靶点TOP4。除了CD19,CD3、BTK、CDK6、GLP-1R、JAK1等靶点也展现出日益增长的研发热度。
从靶点集中度来看,2018至2023年期间,前5%的热门靶点所涉及的药物占据所有受理新药的32%,但与2017至2022年期间的44%相比,显示出了一定的下降趋势。
具体到各个靶点,PD-L1的受理药品数量在2018至2021年期间持续上升,但自2022年开始有所回落。EGFR靶点在2021年达到了热度的巅峰,但随后在2022年热度有所下降,虽然2023年有所回升,但仍未恢复到2021年的水平,其相对2021年的CAGR为-7.4%。
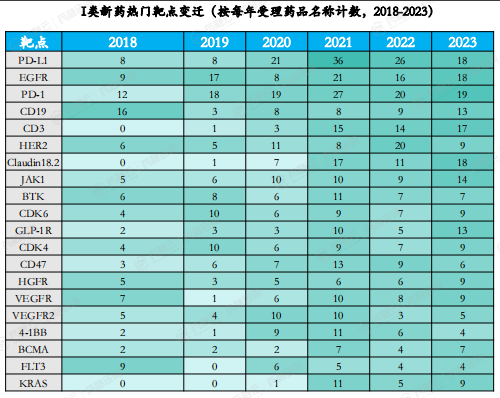
图片来源:药融咨询2023年《中国1类新药靶点白皮书》
PD-1的受理药品数量也经历了类似的增长与回落过程,在2018至2021年期间持续增长,但自2022年开始逐渐下滑。与此同时,CD19靶点自2019年之后热度回升,显示出强劲的增长势头。CD3靶点近年来也备受关注,热度不断攀升。
而HER2靶点虽然在2022年达到了热度的顶峰,但2023年的药品受理数量却相比2022年下降了超过50%,显示出一定的波动性和不确定性。
综合来看,新药研发领域在2018至2023年期间展现出了多样化的趋势,虽然部分热门靶点的热度有所波动,但整体而言,新药研发仍然保持着蓬勃的发展态势。
2018-2023年期间,TOP3靶点受理药品汇总
在2018至2023年期间,新药研发取得了显著进展。其中,共计受理PD-L1药品78个,获批上市4个,有李氏大药厂的索卡佐利单抗、盛迪医药的阿得贝利单抗、基石药业的舒格利单抗以及思路康瑞药业的恩沃利单抗。
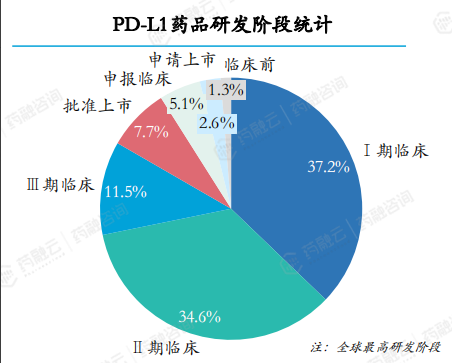
其余PD-L1药品多数处于研发早期阶段,I期和II期临床研究阶段药品占比分别为37.2%和34.6%,而进入III临床及以上研发阶段的药品占比约14.1%。在进度较快的药品中,正大天晴的TQB2450和科伦药业的泰特利单抗已申请上市,信达生物的IBI-318、普米斯生物的PM-8002以及恒瑞医药的SHR-1701则处于III期临床阶段。所有PD-L1药品的治疗领域均集中在肿瘤和免疫调节,其中转移性非小细胞肺癌和小细胞肺癌是适应症开发的重点。
同期,受理EGFR药品72个,其中舒沃替尼、贝福替尼、伏美替尼以及奥美替尼/阿美替尼已获批上市,且适应症均为转移性非小细胞肺癌。与PD-L1药品类似,EGFR药品也主要处于I期和II期临床研究阶段,占比合计约55.5%。进入III临床及以上研发阶段的药品有19个,占比约26.4%,包括奥赛康的ASK-120067、圣和药业的瑞厄替尼/奥瑞替尼/SH-1028、倍而达的瑞泽替尼以及晨泰医药的佐利替尼等。这些EGFR药品同样以肿瘤和免疫调节为主要治疗领域,转移性非小细胞肺癌是研发进展较快的药品的主要适应症。
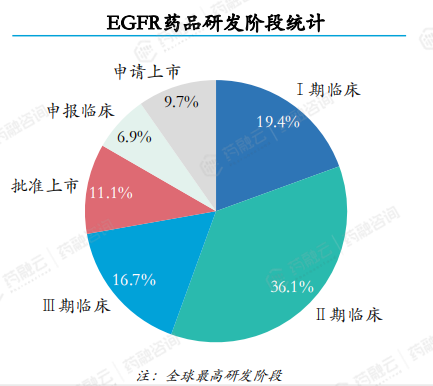
此外,PD-1药品在2018至2023年期间共计受理61个。其中,I期和II期临床研究阶段药品共占比约54.1%,而进入III期临床及以上研发阶段的药品有16个,占比约26.3%。在这61个PD-1药品中,有60个治疗领域为肿瘤和免疫调节,仅有1个为抗感染。
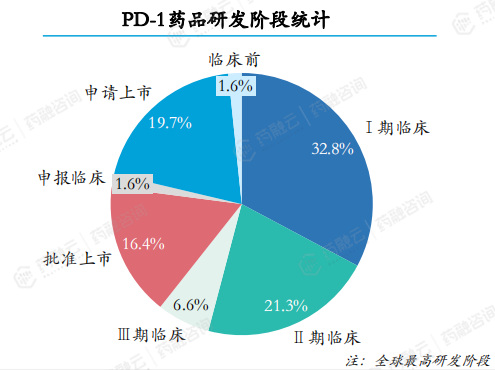
图片来源:药融咨询2023年《中国1类新药靶点白皮书》
已获批上市的PD-1药品多数适应症为转移性非小细胞肺癌和霍奇金淋巴瘤,包括君实生物的特瑞普利单抗、信达生物的信迪利单抗、恒瑞医药的卡瑞利珠单抗、百济神州的替雷利珠单抗以及正大天晴/康方生物的派安普利单抗等。
总的来说,在2018至2023年期间,我国新药研发领域取得了显著进展。尽管部分热门靶点的热度有所波动,但新药研发的整体趋势仍然积极向上。随着研发技术的不断进步和临床数据的积累,相信未来这些新药将能够更好地满足患者的治疗需求,推动医药行业的持续发展。
附:
2018-2023年批准上市Ⅰ类新药(化学药/生物制品)
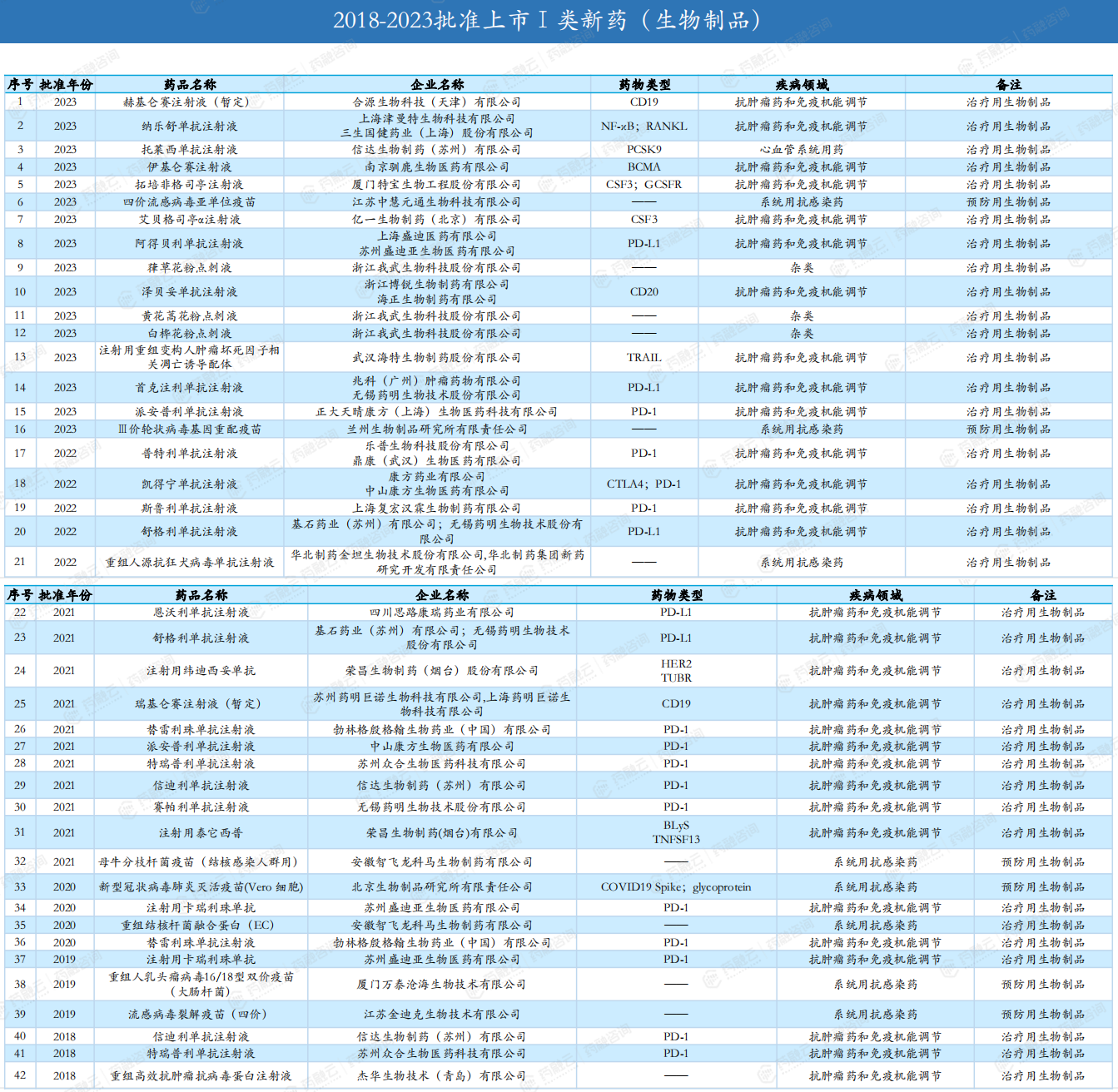
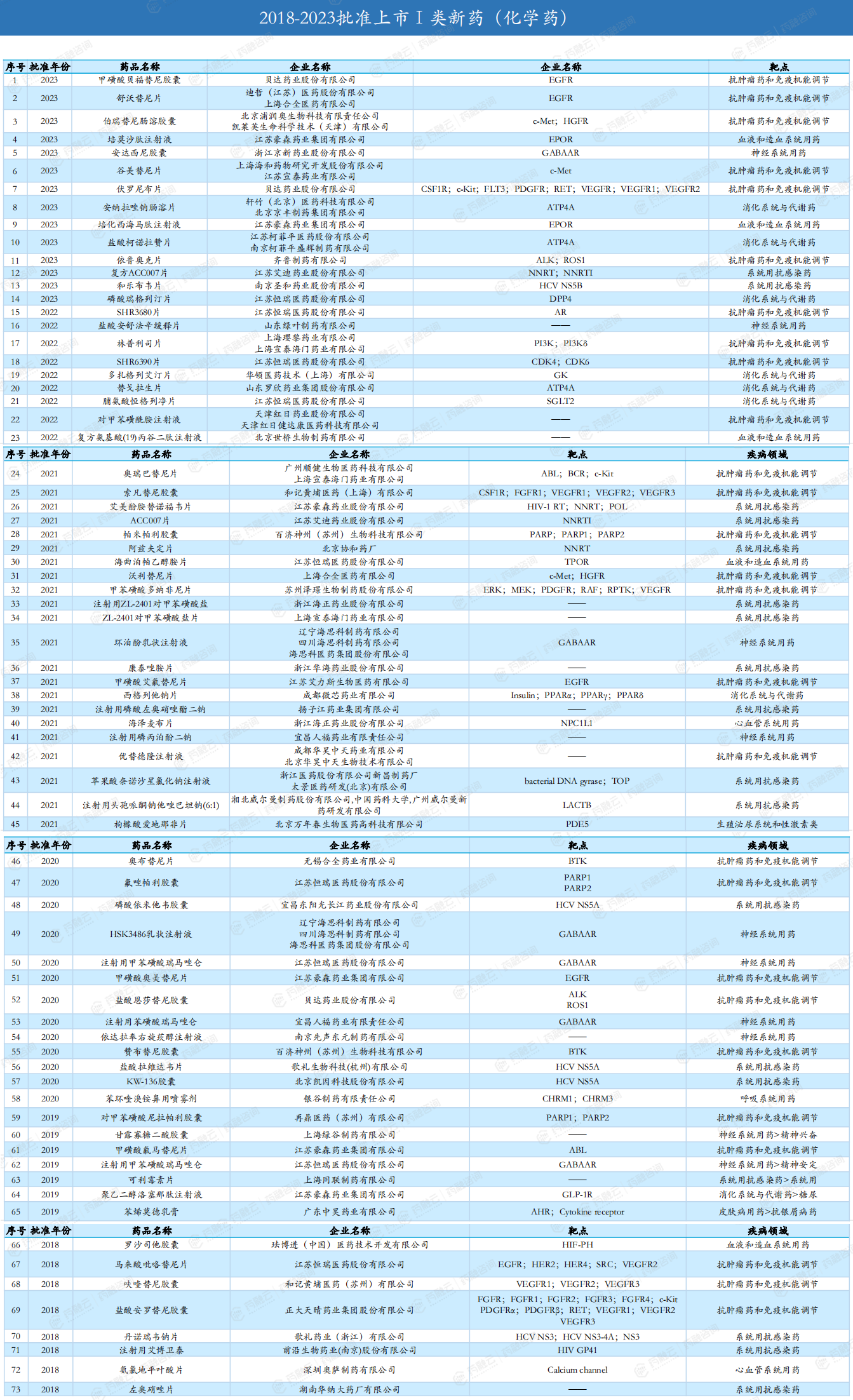
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论