9月全球在研新药月报【内容亮点】
9月国内新药获批临床情况
- 9月共有202款新药获批临床(共计323个受理号),较上个月增加了25款,
- 9月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有134个,占比41%,
- 9月获批剂型主要为注射剂与片剂,分别有167个,98个。
全球获孤儿药/突破性/快速通道资格认定品种盘点
- 9月共有34款药物获孤儿药/突破性/快速通道资格认定品种。
全球在研创新药积极/失败临床结果最新动态速递
- 默沙东的Enlicitide治疗高胆固醇血症3期研究取得积极结果;
- 赛诺菲全球首创OX40L单抗Amlitelimab 3期研究成功;
- 礼来口服GLP-1RA orforglipron在3期头对头研究中优于口服司美格鲁肽;
- 罗氏口服SERD药物Giredestrant 3期研究成功。
每月相关创新药最新政策速递、国内新药注册申报、全球获孤儿药/突破性/快速通道资格认定品种盘点、全球在研创新药积极/失败临床结果TOP20、全球创新药研发进展TOP20等,摩熵咨询团队基于真实可溯源的全球医药数据,将每月推出「全球在研新药月报」,以期帮助业内人士通盘把握每月全球范围内的新药开发情况,全面而深入的了解全球新药开发动态。
一、9月国内新药获批临床/上市情况
根据摩熵医药数据库统计,2025年9月共有202款新药获批临床(共计323个受理号),较上个月增加了25款,其中包括85款化药,109款生物制品,8款中药。
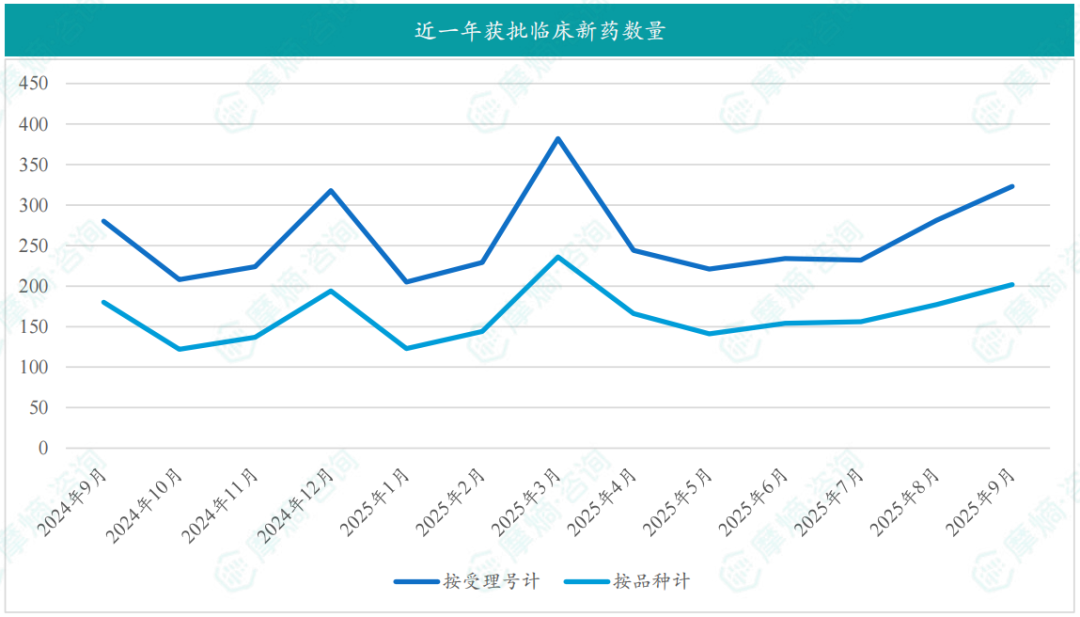
截图来源:摩熵咨询月报
9月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有134个,占比41%,消化系统与代谢药物获批数量也比较多,有24个。获批剂型主要为注射剂与片剂,分别有167个,98个。
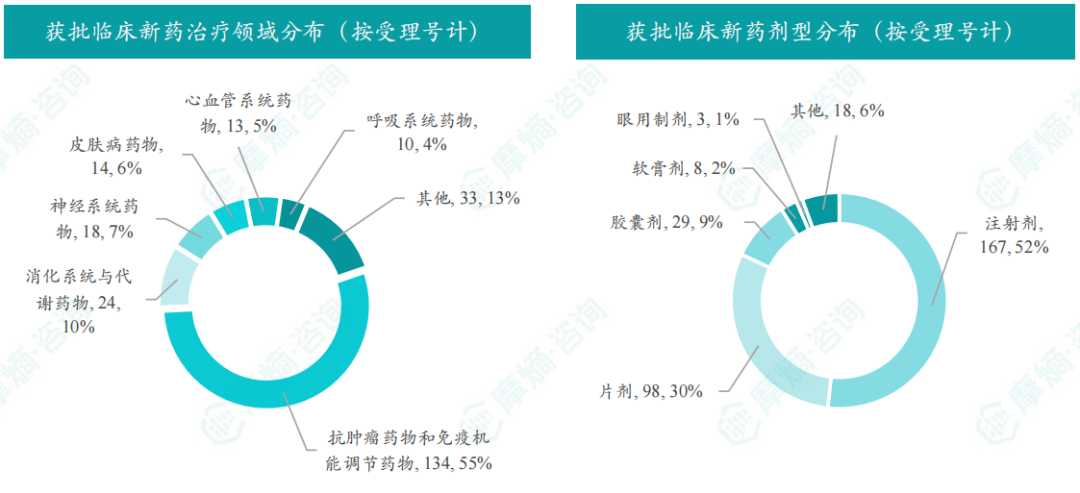
截图来源:摩熵咨询月报
在9月份,国内医药市场迎来了4款创新药物的获批上市,涉及江苏恒瑞医药的泽美妥司他片,用于既往接受过至少1线系统性治疗的复发或难治外周 T 细胞淋巴瘤。
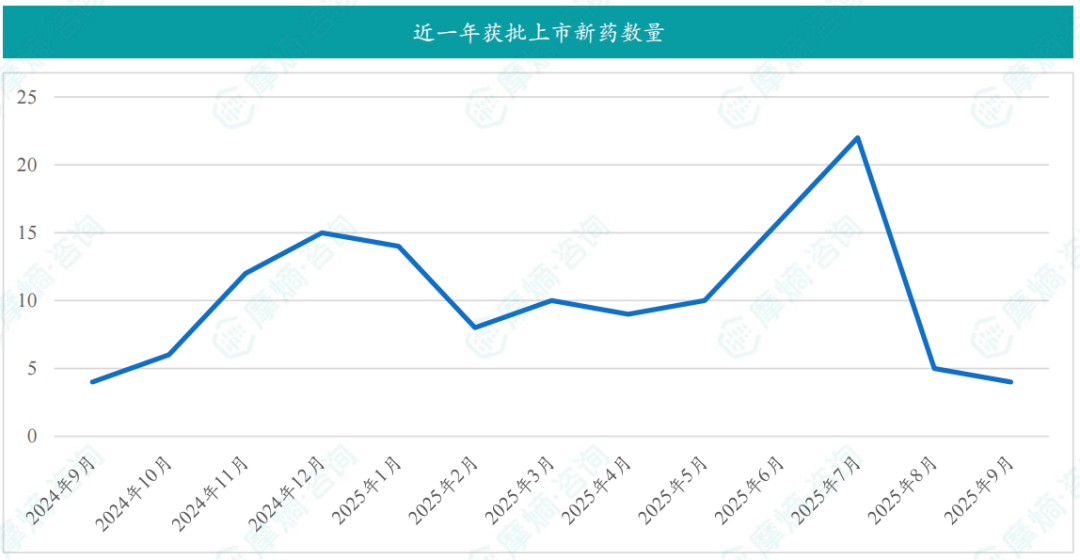
截图来源:摩熵咨询月报
二、全球获孤儿药/突破性/快速通道资格认定品种盘点
9月共有34款药物获孤儿药/突破性/快速通道资格认定。9月15日默沙东(MSD)与第一三共(Daiichi Sankyo)共同开发的在研抗体偶联药物(ADC)raludotatug deruxtecan(R-DXd)已获得美国FDA授予的突破性疗法认定(BTD),用于治疗接受过贝伐珠单抗(bevacizumab)治疗的铂类耐药性CDH6阳性上皮性卵巢癌、原发性腹膜癌或输卵管癌成年患者。本次认定的授予基于raludotatug deruxtecan在早期临床试验中展现出的积极疗效与潜力。
9月全球孤儿药/突破性/快速通道资格认定品种一览表(部分)
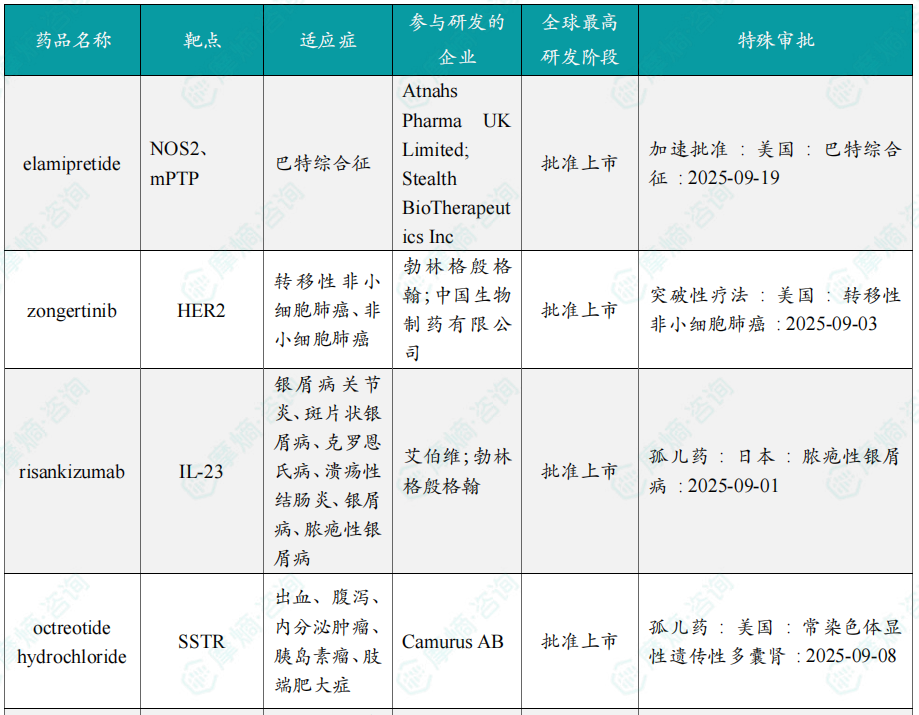
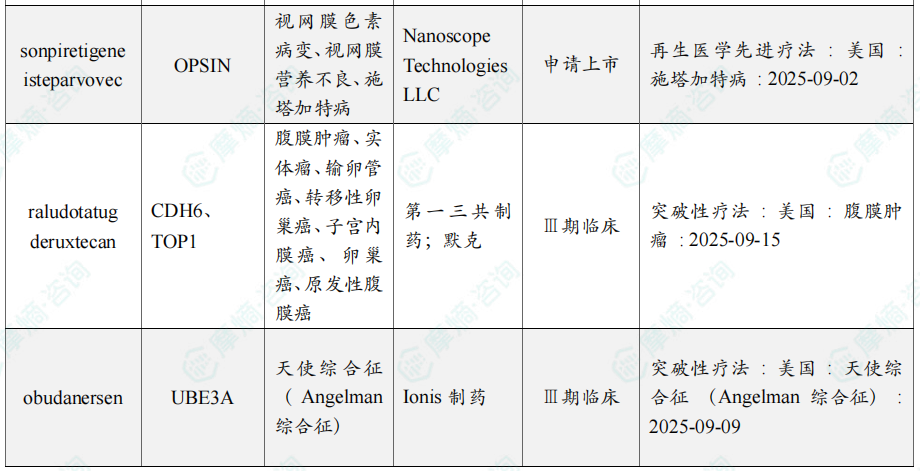
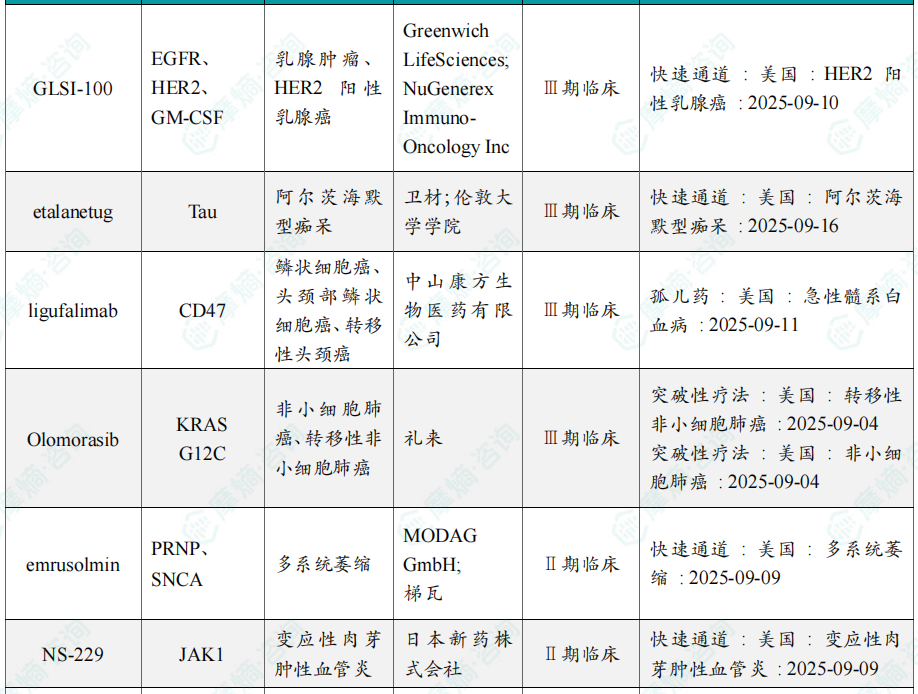
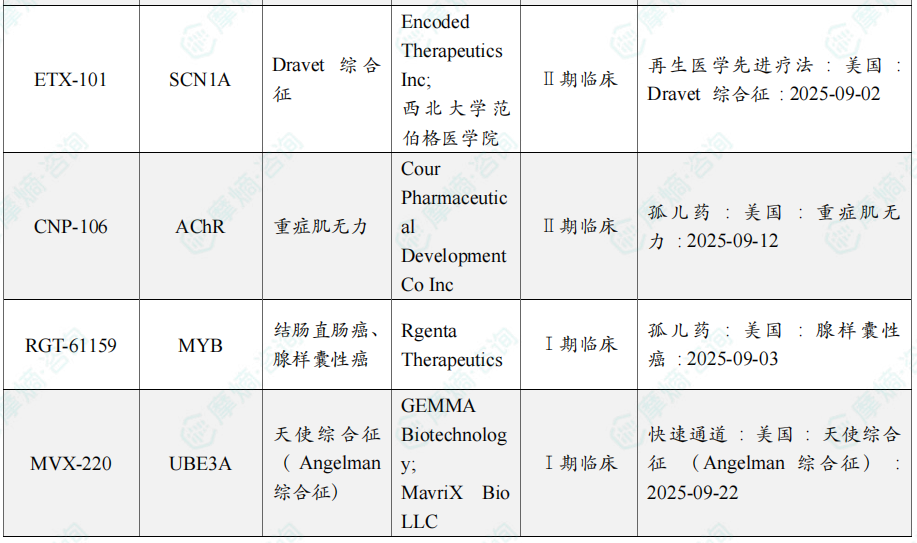
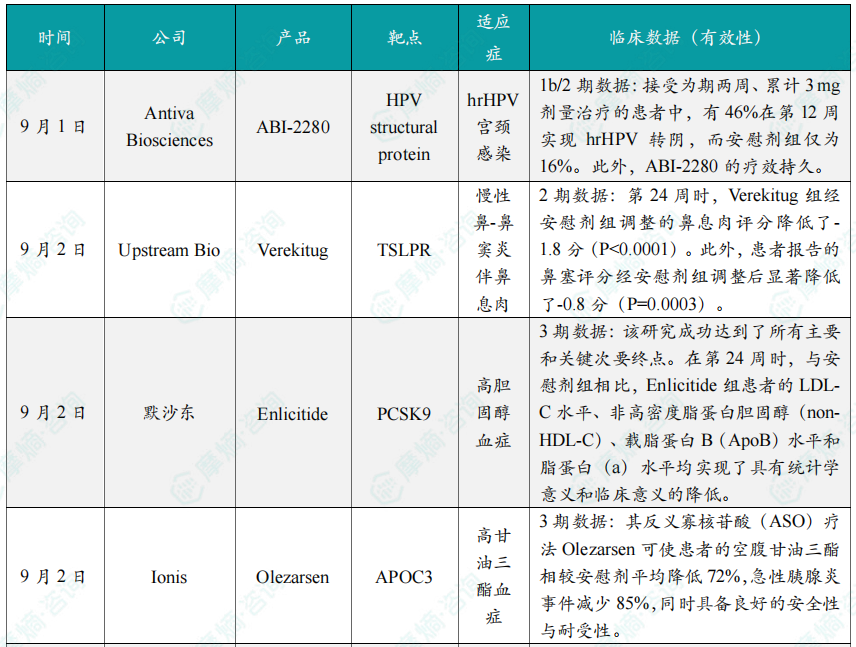
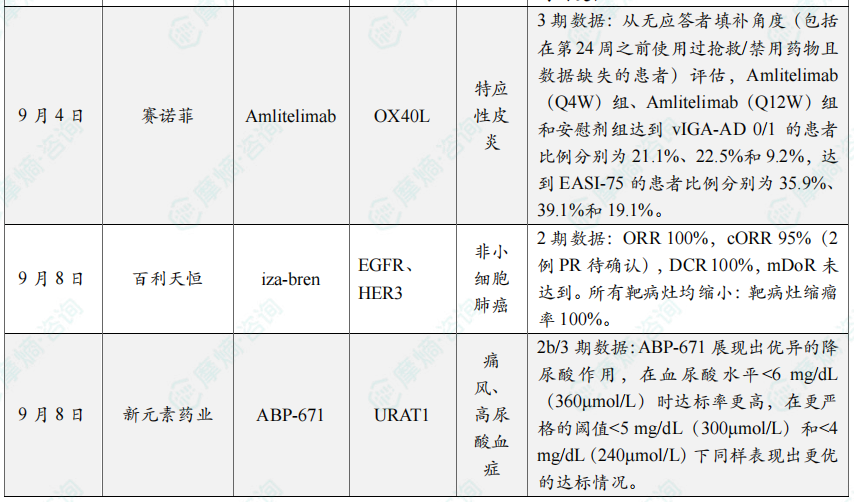
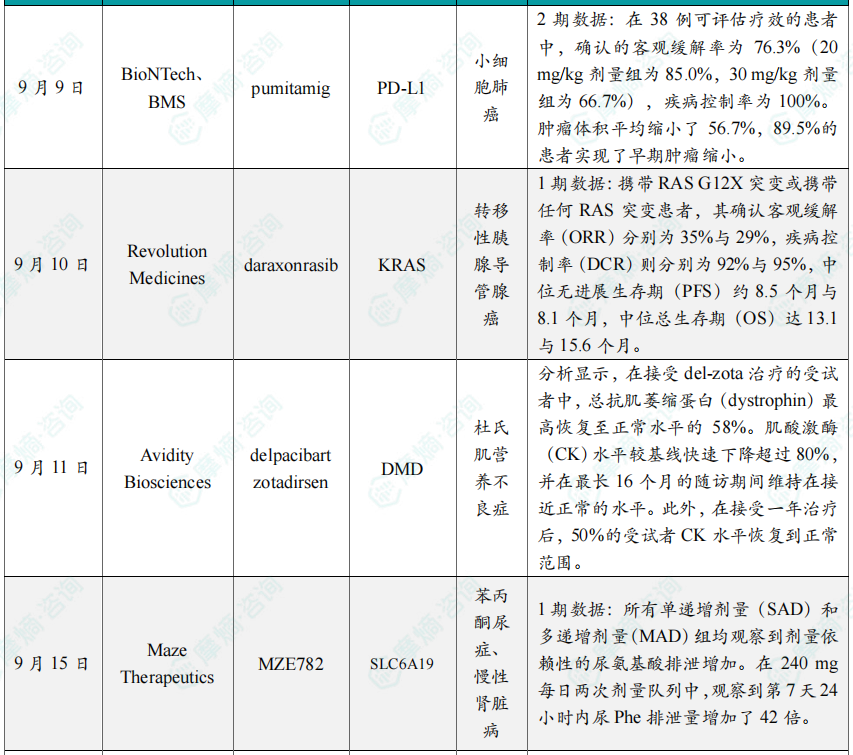
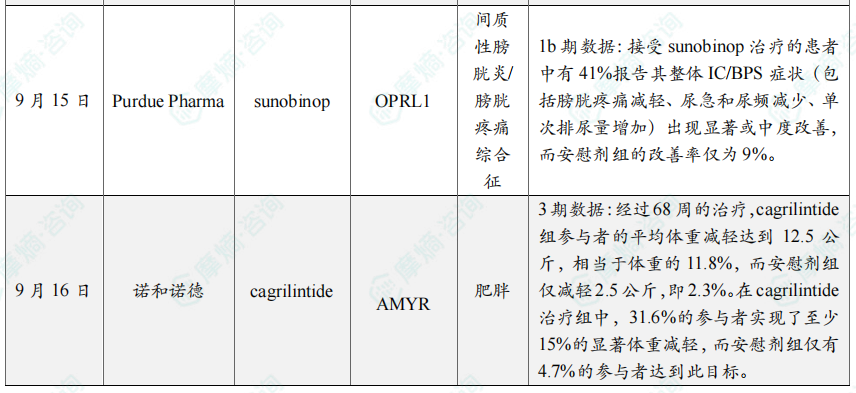
三、全球在研创新药积极/失败临床结果TOP20
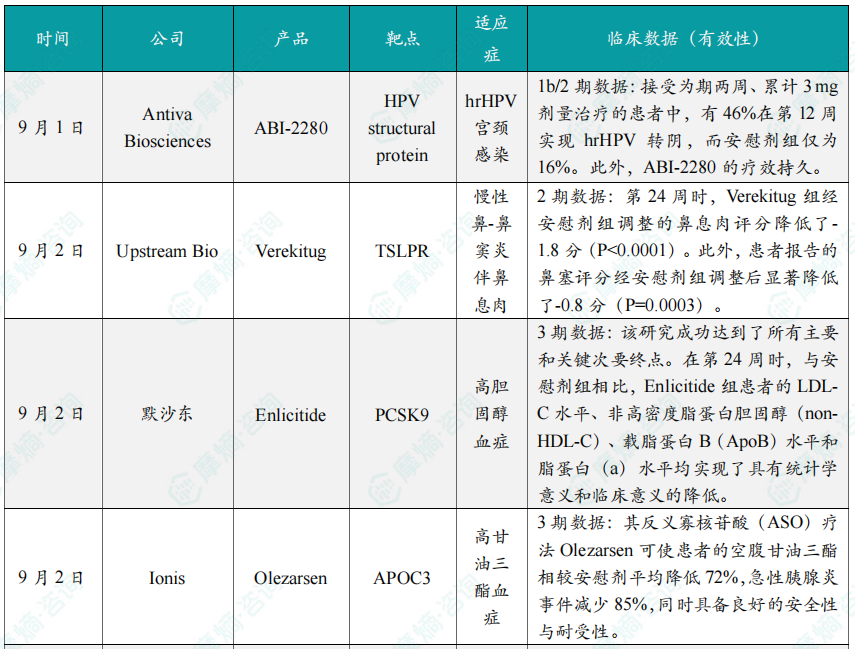
在9月全球创新药研发动态中,9月1日,Antiva Biosciences公司宣布,其治疗hrHPV宫颈感染的局部外用疗法ABI-2280的1b/2期临床试验取得积极的顶线结果。ABI-2280是一种PMEG二磷酸盐的无环核苷膦酸酯前药,可经阴道由患者自行给药。
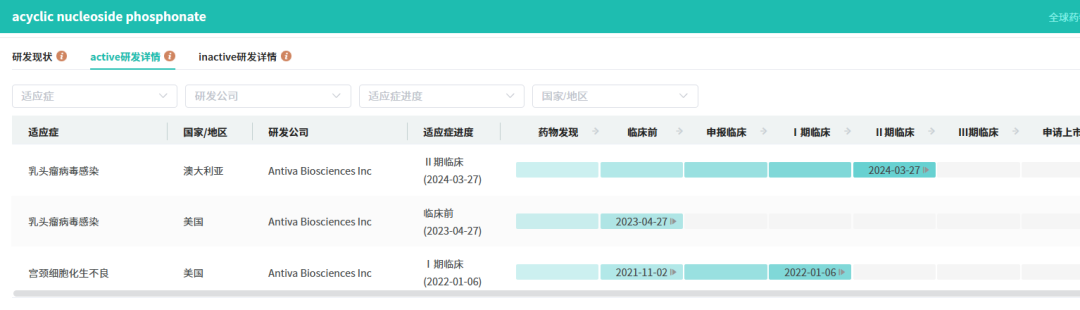
截图来源:摩熵医药全球药物研发数据库
次日,默沙东宣布Enlicitide治疗高胆固醇血症的III期CORALreef Lipids研究取得了积极结果。该研究是Enlicitide目前已完成的最大规模的III期研究。此前,该药物已顺利完成两项III期研究。CORALreef Lipids研究是一项随机、双盲、安慰剂对照临床试验(n=),评估了Enlicitide在接受稳定降脂疗法(包括至少一种他汀类药物)治疗或对他汀类药物不耐受的有主要动脉粥样硬化性心血管疾病(ASCVD)事件史或首次ASCVD事件风险增加的高胆固醇血症成人患者中的疗效、安全性和耐受性。
全球在研创新药积极/失败临床结果TOP20
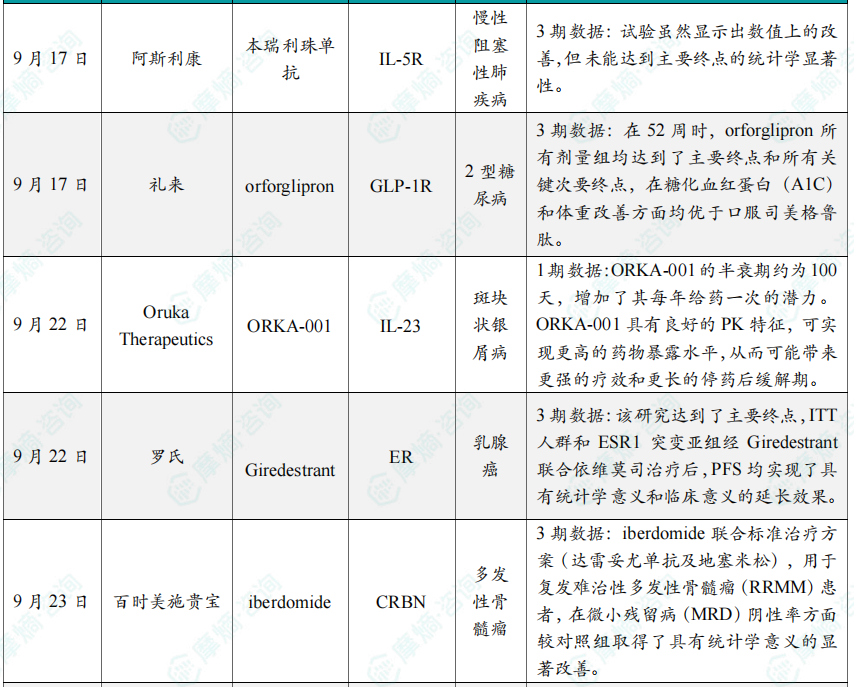
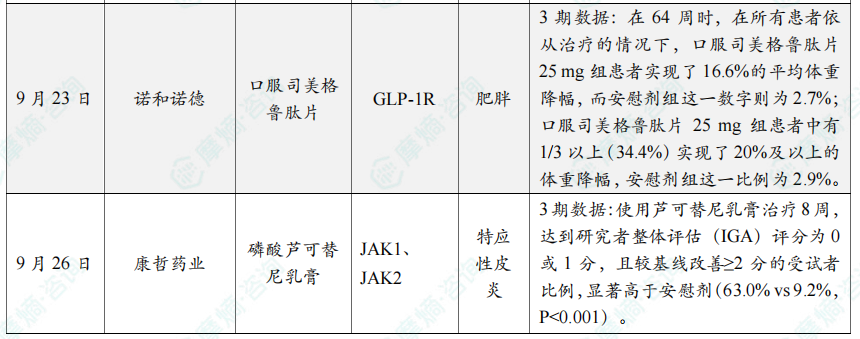
四、全球创新药研发进展TOP20
在9月全球创新药研发进展TOP20榜单中,亮点纷呈。9月1日,迈威生物宣布,其靶向IL-11单抗创新药9MW3811针对病理性瘢痕的2期临床试验申请已获得中国国家药品监督管理局(NMPA)正式受理,有望于2025年底启动该临床试验。白介素-11(IL-11)是一种在慢性炎症和纤维化相关疾病中发挥关键作用的细胞因子,广泛参与肺、皮肤、肾脏和肝脏等多个器官的纤维化进程,并与衰老相关疾病的发生密切相关(Nature,2024)。
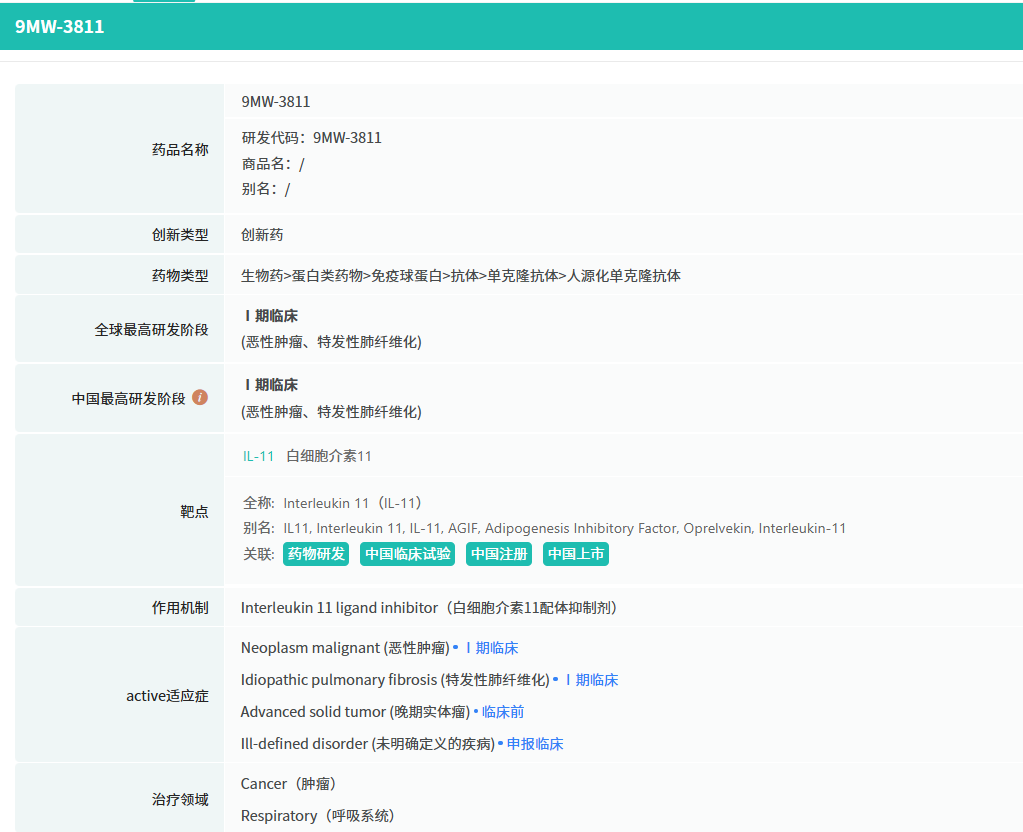
截图来源:摩熵医药全球药物研发数据库
9月2日,中国国家药监局药品审评中心(CDE)官网公示,恒瑞医药申报的1类创新药HRS9531注射液的上市申请获受理,适应症为:本品适用于在控制饮食和增加运动基础上,初始体重指数(BMI)符合以下要求的成人的长期体重管理:≥28kg/㎡(肥胖),或≥24kg/㎡(超重)并伴有至少一种体重相关合并症(例如高血糖、高血压、血脂异常、阻塞性睡眠呼吸暂停、脂肪肝等)。HRS9531注射液是恒瑞医药自主研发的胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素肽(GIP)双重受体激动剂,具有改善胰岛素抵抗、抑制食欲、降低血糖和减轻体重等作用。HRS9531注射液已获得中国国家药监局(NMPA)批准用于开展2型糖尿病、超重或肥胖和阻塞性睡眠呼吸暂停适应症的临床试验。
全球创新药研发进展 TOP20
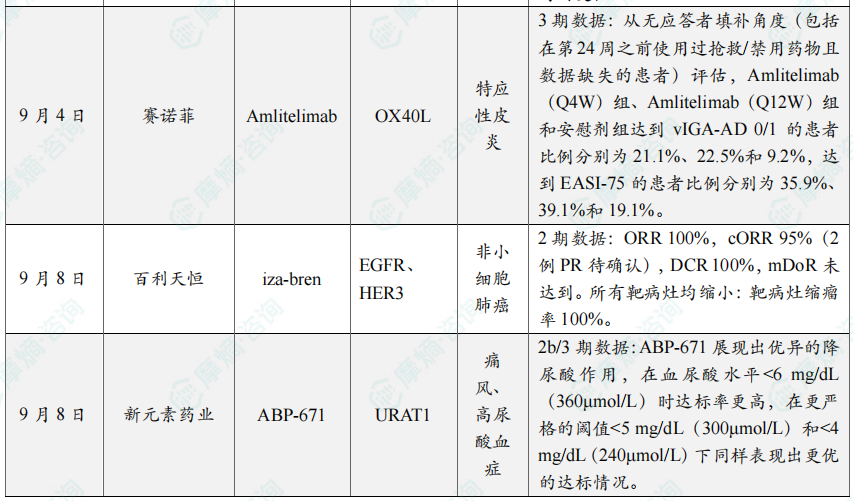
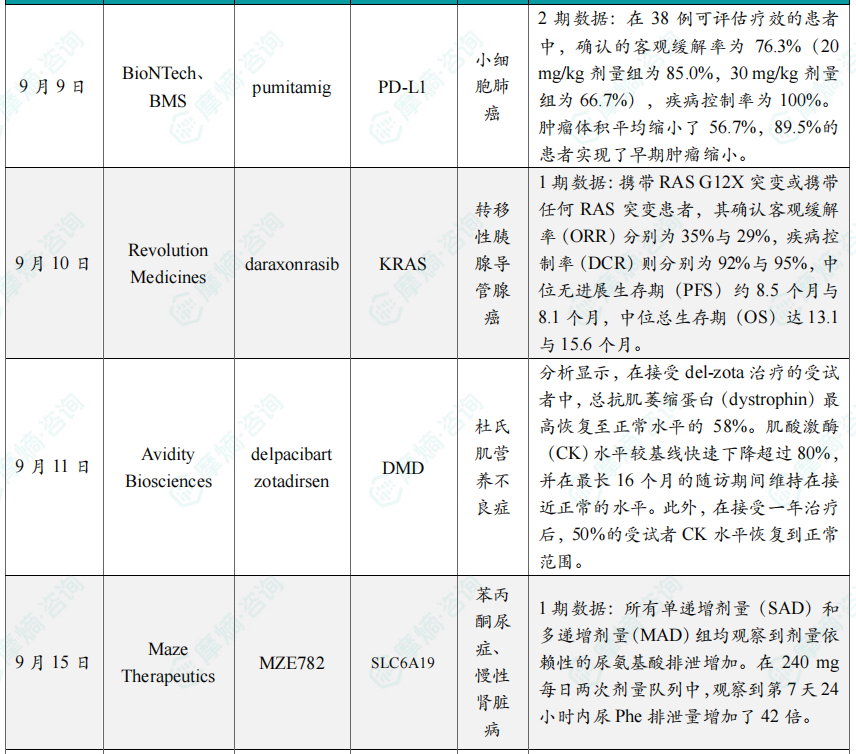
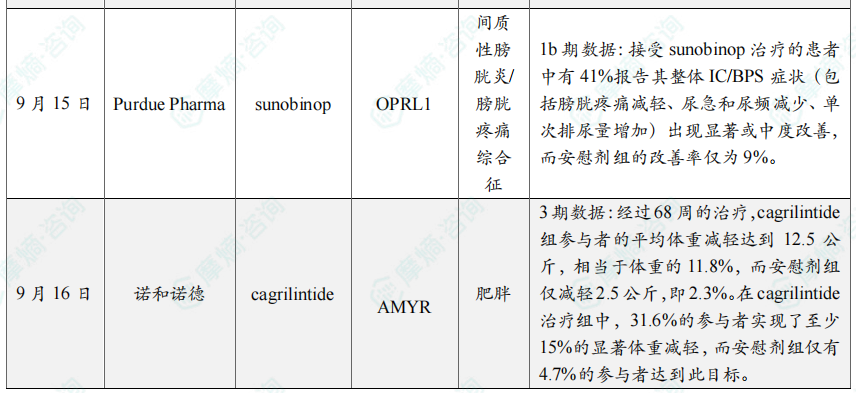
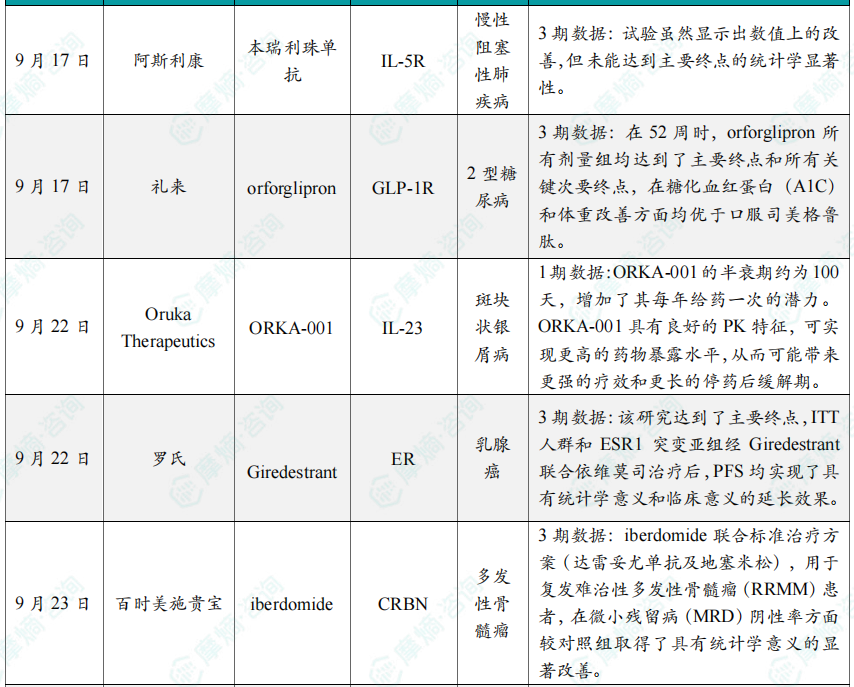
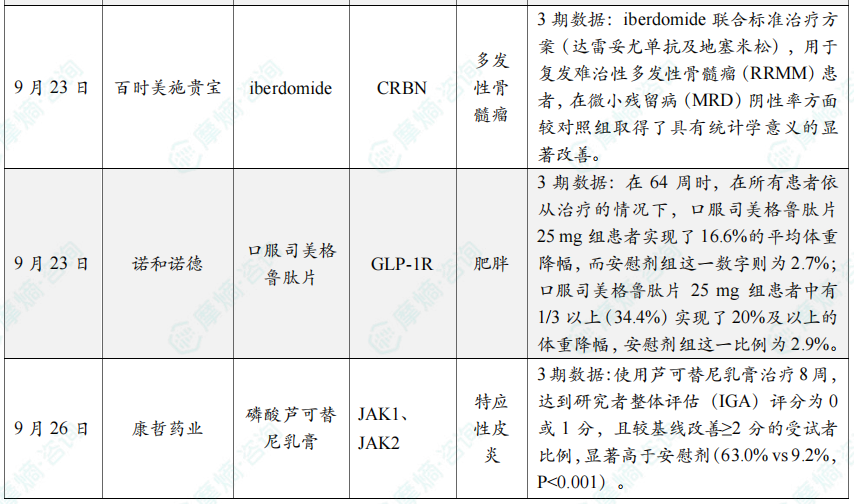
截图来源:摩熵咨询《2025年9月全球在研新药月报》
以上内容均来自摩熵咨询{2025年9月全球在研新药月报},如需查看或下载完整版报告,可点击!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
拓展阅读:
1.2025年2月全球新药研发月报:144款新药获批临床,64款纳入特殊审评
2.2025年9月仿制药月报:164个品种过评,9款首家!杭州中美华东占据亿级重磅注射剂98%的市场份额

























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论