
在现代创新药物发现与开发的漫长链条中,活性药物成分(Active Pharmaceutical Ingredient,简称 API)的物理化学性质往往决定了其最终能否成功跨越从实验室走向临床的“死亡之谷”。面对日益增加的难溶性候选分子,药物固态化学和晶体工程学扮演着至关重要的角色。API 可以以多种固态形式存在,而在药物工业中,最为核心且常见的两种改性策略便是成盐(Salt Formation)与共晶(Cocrystallization)。
本文旨在通过深度的理论剖析与工业实践总结,全面阐述在药物早期及后期开发阶段,如何科学、系统地进行盐与共晶的筛选、评价、放大以及最终的制剂转化。
1. 固态形式的重塑:盐、共晶及其分子本质
1.1 盐与共晶的化学热力学界定
在分子层面上,盐和共晶的形成机制存在着根本的差异。
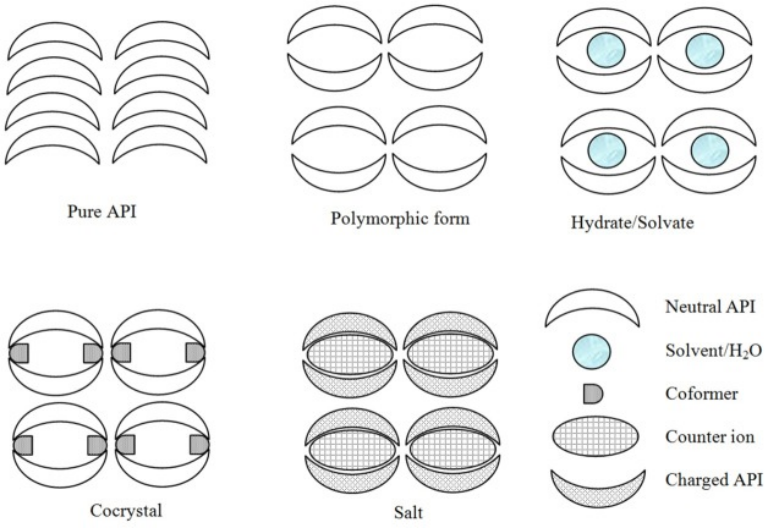
盐、共晶和多晶型物的示意图(doi:10.15171/apb.2016.062)
盐的形成基于经典的酸碱化学反应,其核心在于 API 与反离子之间发生了明确的质子转移。这种离子间的静电相互作用不仅极大地改变了分子的极性,更是解决可离子化 API 溶解度低下和生物利用度瓶颈的常规武器。同时,成盐还可以优化药物的熔点、纯度、化学稳定性及吸湿性等关键物理参数。
相比之下,对于那些不具备电离中心,或者受限于 pKa 无法有效成盐的弱酸弱碱类 API,共晶技术提供了一种极具潜力的替代途径。共晶并不涉及质子的转移,而是依赖于组分间(API 与共晶配体)强大的非共价相互作用,主要是氢键的定向自组装。此外,晶体工程学领域还衍生出了第三种更为复杂的固态系统——共晶盐(Salt Cocrystal),即在一个晶格网络中,同时包含了质子转移事件与组分间的氢键组装,为那些难以被传统方法驾驭的 API 提供了额外的调控空间。
1.2 工业界的前沿应用实践
在当今的制药行业,虽然游离酸、游离碱和各类盐型药物已占据了市售药品的主导地位,但共晶技术的崛起正为新药研发注入强劲动力。多家跨国制药巨头已在临床阶段积极推进共晶项目。例如,辉瑞(Pfizer)与默克(Merck)联合研发的 SGLT2 抑制剂埃格列净(Ertugliflozin),其采用的是与焦谷氨酸形成的 1:1 共晶体。
在心血管疾病领域,诺华(Novartis)的重磅炸弹药物诺欣妥(Entresto®)则是一个极为经典的案例,它是一种含有沙库比曲(Sacubitril)和缬沙坦(Valsartan)半水三钠的共晶复合物。
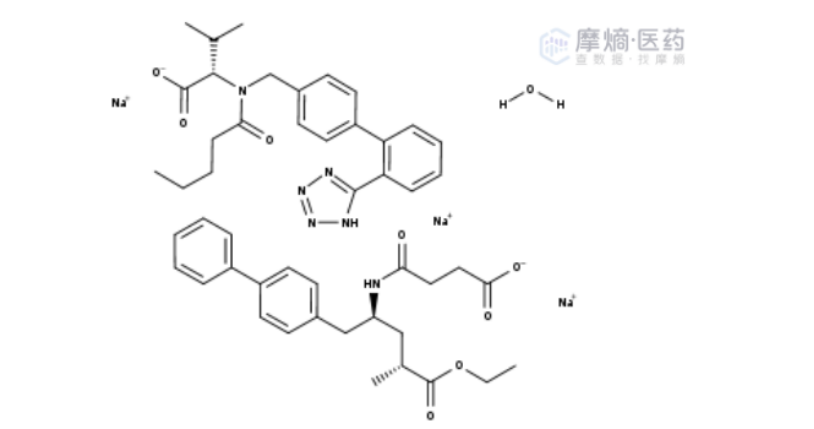
诺欣妥化学结构
在日本,安斯泰来开发的依普列净 L-脯氨酸(Ipragliflozin L-proline)共晶体(Suglat®)已获批用于治疗 2 型糖尿病。这些成功案例无可辩驳地证明了盐与共晶在突破 API 理化性质瓶颈、提升成药性方面的巨大商业价值与临床意义。
2. 探寻最优晶型的路径:多维度的筛选策略
在确认候选药物分子并将其推向深入评价之前,获取具备优异理化特性的盐或共晶形式是不可逾越的步骤。药物开发的阶段不同,其筛选的核心诉求与规模也存在显著差异。
2.1 早期与后期筛选的目标分野
在早期药物开发阶段,主要矛盾在于时间紧迫且物料极度匮乏。此时的目标是快速锁定一种具有“可接受”或“较优”理化性质(如令人满意的结晶度、较低的吸湿性、以及能够支撑早期动物试验的溶解度和生物利用度)的固态形式。研究人员通常会在有目的性的小规模实验中展开探索:例如使用 3~5g 的原料药进行约 100 次筛选实验;若物料更为受限(不足 500mg),则必须依靠高通量筛选(High-Throughput Screening, HTS)平台,该平台能在 <1~5mg 的微量级别下运作。对于只追求最稳定、最难溶形式以评估毒理极限的情况,甚至可以使用 1g 原料药仅开展 25 次精简实验。
当项目步入后期开发,筛选的维度和深度急剧增加。这一阶段不仅需要综合运用手动实验与 HTS 进行 300~400 次的大规模排查,还必须将制剂工艺的应力因素(如微粉化、高剪切共混、湿法或干法制粒)以及长期存储过程中的转晶风险纳入考量。此外,为了最大化药品的生命周期价值,围绕 API 反离子或共晶的多晶型进行全面的知识产权(IP)布局,是后期筛选中极具战略意义的一环。
2.2 反离子与共晶配体的科学选择
无论是成盐还是共晶,配体的选择直接决定了最终晶体的命运。盐的反离子必须是能够供给或接受质子的酸性或碱性实体。共晶配体可以是与成盐所用相同的化合物(前提是环境阻断了质子交换),也可以是依靠氢键、π-π 堆积等非共价力结合的中性分子。
为了确保最终药物的安全性,配体的来源必须受到严格监管。研究人员高度依赖于“公认安全物质”(GRAS)清单以及美国食品中的可添加物质(EAFUS)数据库。从毒理学管理的角度,这些配体通常被分为三大类:
- 第一类:具有极高安全性、可不受限制使用的物质,它们通常是生理代谢网络中普遍存在的离子或中间产物,是首选的成盐配体。
- 第二类:非天然存在但毒性极低、人体耐受性良好的物质。
- 第三类:具有自身微弱药理活性,仅在特定场景下谨慎使用的物质。使用此类配体时,必须严密复查最新的毒理学文献与安全红线,并密切关注预期剂型的长期累积毒性。如反离子的最大日剂量(MDD)限制,例如对于口服途径,苯磺酸根的最大日剂量约为 160mg,而柠檬酸根则可高达 5250mg。
在物理化学预判上, pKa 差异(ΔpKa = pKa (碱) - pKa (酸))是一个核心经验法则。当 ΔpKa < 0 时,质子转移的能量壁垒极高,体系最有可能形成共晶;当 ΔpKa > 3 时,热力学驱动力足以引发完全的质子转移,从而稳定形成盐。若该值介于 0 至 3 之间,则体系处于“连续体”的灰色地带,可能生成具有部分质子转移特征的复合物或共晶体。
在共晶设计中,超分子化学中的“合成子”概念被广泛应用。同源合成子(如羧酸形成的二聚体环状结构)与异源合成子(如磺酰胺与羧酰胺的互补配对)构成了晶格中强有力的结构节点。分子间的几何形状契合度与极性互补性极大地提高了共晶的命中率。
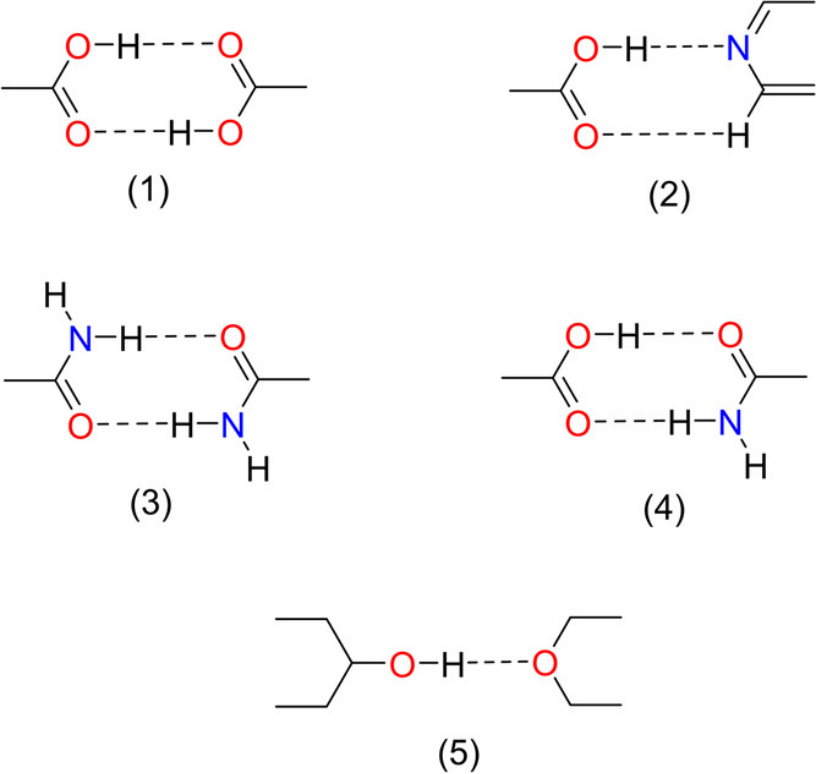
共晶形成中常用的典型超分子合成子(doi:10.1021/acsmedchemlett.1c00478)
2.3 手动、自动化高通量与计算预测的交响
结晶过程受限于众多热力学与动力学变量,包括溶剂极性、混合比例、系统温度、降温或升温的梯度速率、过饱和度的演变等。著名晶体学家 Walter McCrone 曾断言,一个化合物能够被发现的多晶型数量,与其上投入的研究时间、经费及实验频次成正比。
高通量筛选(HTS)通过机械臂、自动移液与多孔板(如 96 孔板),突破了人工筛选的通量极限,仅用毫克级样品便可穷尽极其复杂的溶剂配比与孵育条件。HTS 尽管受限于某些极端工艺条件(如受限的蒸发控制或极高温模块),但若辅以精密的实验设计(DOE),仍可覆盖数百次结晶尝试,有效揭示多晶型、水合物、溶剂化物等潜在形式。
同时,计算辅助手段作为一种“预筛选”利器正崭露头角。基于晶格能量的计算、剑桥结构数据库(CSD)的大数据挖掘以及表面静电势的氢键倾向性预测,可以帮助研究人员从成百上千种候选配体中锁定“苗头(Hit)”分子。计算不仅能预测热力学稳定性,甚至能勾勒出药物在特定 pH 值水溶液中的溶解度轮廓线。尽管对盐型进行结构预测因电荷转移和远程静电相互作用更为复杂,但在某些结构已知的前提下,现代算法已经成功预测了诸如盐酸特拉唑嗪(Terazosin Hydrochloride)的无水多晶型物。
2.4 工作流程与表征手段
一个严谨的筛选工作流程应具备闭环的验证逻辑:
① 配体选择:严格基于 GRAS 清单与 pKa 导向选择目标分子。
② 实验矩阵设计:覆盖宽广的 pH 范围与溶剂极性梯度,探寻任何潜在的降解风险。
③ 多维度表征:任何疑似的新晶型均需经历 X 射线粉末衍射(XRPD)的指纹图谱确认,热重分析(TGA)与差示扫描量热法(DSC)揭示其热力学事件与溶剂挥发特性,以及核磁共振(NMR)与离子色谱(IC)测定其化学计量比。特别是针对水合物,卡尔·费舍尔(KF)滴定法与动态水分吸附/解吸(DVS)研究至关重要。单晶 X 射线衍射虽为“金标准”,但受限于氢原子散射能力弱,常需结合固态核磁共振(ssNMR)、红外(IR)或拉曼光谱,通过键长及特征官能团振动频率的位移来佐证质子是否发生了真正的转移。
此外,在成功获得首选的盐或共晶后,启动针对该形式的衍生“多晶型物筛选”是防范后期开发风险的关键。这旨在探索其是否存在无水合物、水合物变体,并评估在制剂加工(如高湿环境)下发生歧化变回游离酸碱的风险。
3. 从众多候选者中突围:晶型的综合评估与甄选
获得一系列具有不同化学计量比或结构的盐/共晶后,必须建立科学的决策漏斗或评估矩阵,以确定推向临床的最终先导形式。理想晶型的画像因开发策略而异,但通常需满足以下基准要求:
- 物理化学稳定性与结晶度:优异的结晶度赋予分子更高的化学惰性。目标形式的熔点应足够高(通常 >100°C)以耐受制剂过程中的热应力,并且在环境相对湿度(60%~75% RH)下不可发生潮解,保证储运安全。
- 溶解行为与溶出动力学:溶解度和溶出速率是 BCSI、II 类药物逆袭的命门。对于口服固体制剂,目标水溶性通常设定在 0.1~10 mg/mL 区间;若为静脉注射剂,则需大于 10mg/mL。值得注意的是,溶解性并非越高越好,若是缓控释制剂,则可能特意追求具有缓慢溶解速率的晶型。
- 形态学特征:优选呈板状或规则块状的晶体,尽量避免极细的针状或易断裂的棱镜状晶体,这直接关系到粉体粉碎、流动性、可压片性等下游制剂工艺顺应性。
在评估含有可电离基团的盐型时,必须深度考量其 pH-溶解度曲线。盐型的总溶解度是质子化形态与游离碱(或游离酸)饱和浓度的总和。在这个动态平衡中,随着环境 pH 跨越关键阈值(如 pHmax),占主导地位的固相会从盐型突变为游离形态,导致溶解度呈现断崖式下降或上升。
4. 跨越放大的鸿沟:结晶工艺的工业化转化
当小试规模(克级)的最优晶型被敲定,随之而来的便是工艺放大。将烧瓶中的沉淀转化为反应釜中吨级的纯粹晶体,需要跨越动力学与热力学的多重鸿沟。
首要原则是溶剂体系的工业友好性。依据 ICH Q3C 指南,应尽量采用低毒性的 3 类溶剂,并确保 API 在预设的操作温度范围内具备可接受的浓度梯度变化。结晶的核心在于控制过饱和度的释放。工业上常用的起晶策略包括梯度降温、反溶剂滴加及减压蒸发等。为了防止不可控的爆发性成核(可能导致生成包裹杂质或形成亚稳态多晶型),通常在介稳区内精准引入目标晶型的“晶种”(添加量一般小于 5%)。这不仅有效引导了宏观形貌的演变,更能严格控制最终产品的粒径分布(PSD)。此外,还需警惕化学反应杂质,例如醇类溶剂与甲磺酸结合极易生成具有极高遗传毒性的甲磺酸酯类杂质,其残留量必须被严酷压制在 10ppm 以下。
在探讨共晶的大规模结晶时,三元相图(Ternary Phase Diagram, TPD) 是不可或缺的导航图。以 API、共晶配体(CCF)与溶剂组成的三元体系,在特定温度下描绘出各类固相(纯 API、纯 CCF、共晶体及各自混合区)与液相的平衡边界。
在咖啡因-戊二酸共晶体系的经典案例中,研究者通过构建不同温度区间的相图,精准地勾勒出了共晶的稳定操作窗口。在结晶设计空间内,不仅要确保产物的化学纯度,还要避免多晶型转化风险(例如咖啡因-戊二酸共晶中的亚稳态晶型 I 向热力学稳定态晶型 II 的相变)。通过过程分析技术(Process Analytical Technology, PAT)在线监测溶液浓度与粒子生长,研究证明采用缓慢的降温速率(0.1°C/min)辅以足够负载量的晶种,可以成功抑制亚稳态晶型的成核,并获得均一饱满的颗粒。除传统溶液结晶外,热熔挤出(HME)、喷雾干燥及高剪切制粒技术也正在成为实现共晶工业化放大的新型工程手段。
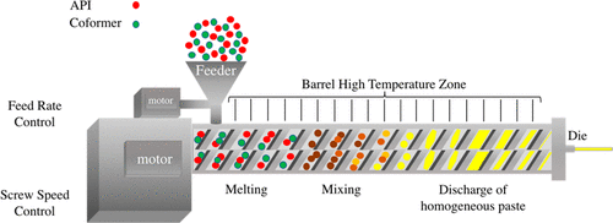
典型 HME 仪器的示意图
5. 制剂转化中的动态演变与处方考量
在药物产品的生命周期中,纯净的原料药晶体并不能直接交予患者,必须经过复杂的单元操作(如粉碎、制粒、干燥、压片或冷冻干燥)转化为剂型。而在这些充满机械应力、热应力及湿度波动的过程中,API 的固态形式极其脆弱,常发生工艺诱导的形态转变(Process-Induced Transformations, PIT)。
5.1 机械力与湿热环境的冲击
微粉化或研磨会引入大量机械能,不仅可能导致结晶骨架塌陷生成无定形物质,其产生的高比表面积更容易从环境中吸附水分。例如,硫酸沙丁胺醇(Albuterol Sulfate)在研磨后产生的无定形区域暴露于湿度下会迅速吸水并重新结晶,直接导致粉体结块与颗粒聚集,破坏流动性。
在湿法制粒环节,水或醇类润湿剂的加入是诱发多晶型相变或水合物形成的高危因素。苯磺酸氨氯地平(Amlodipine Besylate)在湿法制粒过程中,其无水物便会部分转化为二水合物。反之,在后续的流化床高温干燥步骤中,原本的水合物可能会失去结晶水,但在后续吸湿平衡时再度水化,导致片剂体积膨胀甚至开裂(如利塞膦酸钠的异常膨胀现象)。
5.2 辅料相容性与微环境 pH 扰动
赋形剂绝非化学惰性的占位符。若辅料具有较强的碱性或酸性,其可能改变局部微环境的 pH 值,从而“夺取”或“捐赠”质子,导致盐型药物发生致命的歧化反应。例如,含有碱性赋形剂的处方在吸收微量水分后,会直接促使甲磺酸苯佐卡因(Benzocaine Mesylate)和甲磺酸咪康唑(Miconazole Mesylate)解离出游离碱,不仅大幅降低了药物的溶出度,还可能引发色泽变化与化学降解。
对于共晶,辅料的干预有时则是正向的。卡马西平-烟酰胺共晶体在水介质中本极易解离转化为卡马西平二水合物,但若在处方中引入微量的高分子聚合物如羟丙基甲基纤维素(HPMC),便能有效抑制晶核的异相形核,维持共晶态的高溶解优势。
5.3 溶出测试中的沉淀风险
即便药品完好无损地被服用,在进入胃肠道或生物模拟流体(如 FaSSIF)后,过饱和度的瞬间释放也可能诱发沉淀。例如,在针对 AMG517 多种共晶体的溶解度测试中,药物一旦溶出便迅速解离,析出了溶解度极低的游离碱水合物。类似地,盐酸氟西汀-富马酸共晶在特定溶出度测试中亦会发生解离并沉淀出盐酸氟西汀,虽然在体内药代动力学(PK)研究中该共晶体依然表现出了更高的生物利用度。这警示我们在设计处方时,必须充分利用沉淀抑制剂来维系过饱和状态。
6. 法规监管差异与知识产权博弈
在这个高度监管的行业中,监管机构对于盐与共晶的定义和分类,直接决定了药品注册申报的路径与耗费。
6.1 FDA 与 EMA 的监管分歧
美国食品药品监督管理局(FDA)在现行法规体系下(21 CFR 314.108),将同一活性分子的不同盐型严格视作“不同的 API”。这意味着若要更换盐型,必须补充详尽的临床试验数据以证实其有效性和安全性。然而,针对共晶,FDA 的最新指南做出了关键性调整:共晶不再被视为一种独立的活性物质变体,而是被归类为与多晶型物相似的管理范畴,并被视作一种特殊形式的“溶剂化物”(其中溶剂成分是不可挥发的中性配体)。因此,不同配体的共晶(前提是配体安全可控)仅需通过生物等效性研究证明其具备可接受的吸收性能即可。
与之不同,欧洲药品管理局(EMA)则采取了更为宽泛和统一的立场。EMA 将同一分子的多晶型物、水合物、溶剂化物、盐以及共晶一视同仁,均不视为“新活性物质(New Active Substance, NAS)”。只要提供充分的交叉引用支持性安全数据及生物等效性结果,即可推进申请注册。ICH Q11 指南进一步明确,如果共晶形成物属于常见化学品,可按试剂对待;若使用了新颖且复杂的配体,则必须呈递全面的生产、表征及质控论证资料。

美国和欧洲药物共晶体的监管状况
6.2 橙皮书与哈奇-瓦克斯曼法案的刀光剑影
为盐、共晶及其多晶型物申请专利,是创新药企构筑知识产权(IP)护城河、延长产品生命周期的核心战略。FDA 发布的《具有等效性评估的获批药品清单》(即著名的“橙皮书”,Orange Book)记录了原研药物的所有有效专利(涵盖化合物组成、制备工艺、特定盐型及多晶型)及排他期。
基于《哈奇-瓦克斯曼法案》(Hatch-Waxman Act),仿制药企业在提交简略新药申请(ANDA)以挑战原研药(上市对照药物,RLD)时,必须做出四项认证声明之一。其中最为激烈的便是“第四段认证(Paragraph IV)”:仿制药企主张橙皮书中列出的某项晶型或盐型专利无效、不可执行,或其仿制工艺使用了全然不同的避专利晶型(未构成侵权)。这往往会引发旷日持久的专利诉讼,制药史上的诸多著名战役,如围绕盐酸雷尼替丁(Ranitidine Hydrochloride)、盐酸帕罗西汀(Paroxetine Hydrochloride)等多晶型与盐型的法律对决,无一不在印证固态化学专利的巨大商业杠杆力。
7. 穿越周期的经典工业案例解析
为了更为具象地阐释上述理论与策略在真实工业环境中的应用,我们回顾两项极具代表性的新药研发案例。
7.1 茚地那韦(Indinavir):早期盐型切换力挽狂澜
由默克(Merck)公司开发的硫酸茚地那韦(Indinavir Sulfate),是一款被批准用于治疗成人 HIV-1 感染与艾滋病(AIDS)的关键蛋白酶抑制剂。
查数据,找摩熵!图源:摩熵医药数据库
在研发初期,原计划使用的是茚地那韦的游离碱水合物。然而,该游离碱呈现出极其严重的 pH 依赖性:在胃肠道天然生理 pH(7~7.5)环境下,其水溶解度仅为微乎其微的 0.02 mg/mL,导致口服吸收率极差。
研究人员果断决定进行盐型筛选。分子的解离常数( pKa)表明,唯有强酸性的反离子才能诱导完全的质子转移并攻克溶解度难关。但棘手的是,茚地那韦在酸性溶液中化学稳定性极差,容易发生水解降解。经过严密筛选,研究团队最终锁定了一种结晶态的硫酸乙醇溶剂化物。该盐型的水溶性飙升至 >500 mg/mL,且水溶液呈酸性(pH < 3)。但该盐型又带来了极强的吸湿性与高湿转晶风险。为了保护这一脆弱但具有救命疗效的晶型,制剂团队量身定制了极为严苛的“干法制粒”工艺,并控制环境相对湿度维持在 <30%,最终实现了长达 2 年以上的保质期。后续临床数据显示,该硫酸盐形式在空腹状态下的血药暴露量显著优于游离碱,成功推向市场。
7.2 阿托伐他汀(Atorvastatin):后期临床的华丽转身
辉瑞公司(原华纳-兰伯特公司)研发的降脂神药阿托伐他汀钙(Atorvastatin Calcium),属于典型的 BCS II 类分子(高渗透性、低溶解度)。
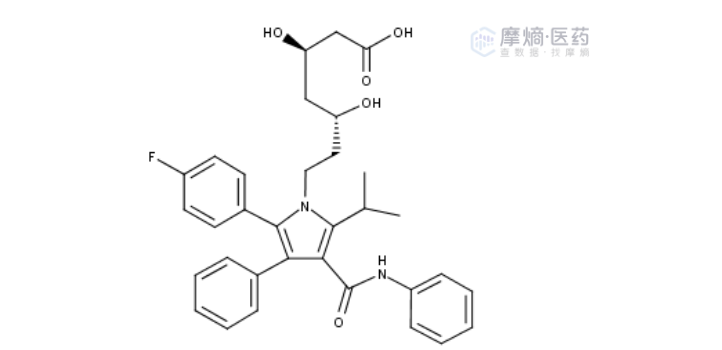
阿托伐他汀钙化学结构
在 I 期与 II 期临床试验中,药企使用的是其半钙盐对映体的“无定形”粉末。无定形结构以其高能态赋予了药物极佳的溶解度和早期优异的药效表现。
然而,当项目进入需要大规模生产的阶段时,无定形物质的工艺灾难显现:极差的粉末流动性、无法顺利过滤与干燥、以及对热、光照、氧气与水分的极度敏感,使其在大生产中步履维艰。面对这一困局,辉瑞在 III 期临床试验期间进行了战略性转向,成功分离出并转而放大生产了一种结晶体的“三水合物”结构(即著名的晶型 I)。
晶型 I 展现出了压倒性的工业制造优势:更高的化学纯度、无与伦比的固态化学稳定性、优良的干燥过滤性能以及狭窄的粒度分布。尽管理论上无定形和结晶三水合物在吸收率上存在差异,但严格的生物等效性人体试验证明,二者的吸收程度高度一致。这一华丽的晶型切换不仅拯救了产品的工艺链,更为辉瑞赢得了极其强大的专利保护网。辉瑞相继为晶型 I、II、IV 等多达数十种晶型申请了涵盖物质组成及晶型专利的《橙皮书》列名,其中某关键多晶型专利的保护期一直延续至 2016 年 7 月。凭借精准的晶型生命周期管理与专利策略,阿托伐他汀一举成为制药史上最畅销的重磅炸弹药物之一,年销售额连续7年超过100亿美元。
立普妥历年销售额
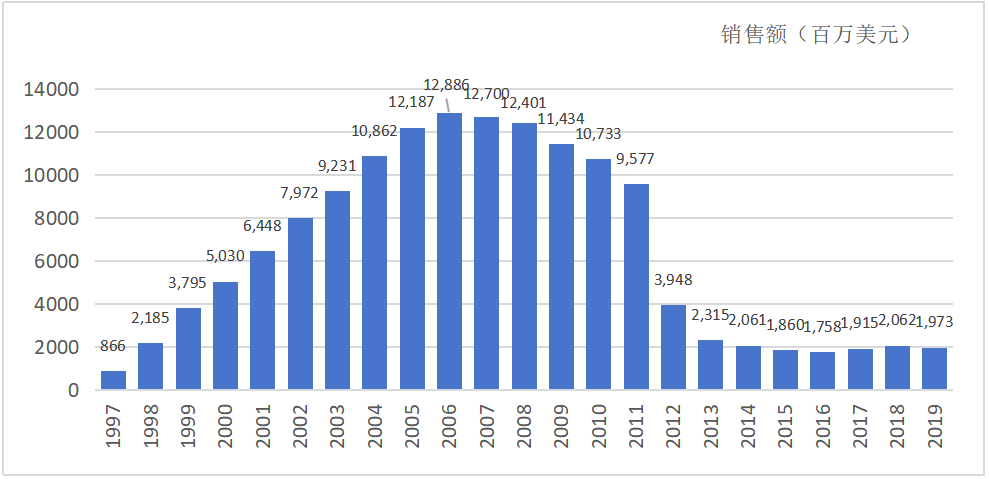
查数据,找摩熵!图源:摩熵医药数据库
结语
从小试管内配体的氢键组装与质子夺取,到巨型反应釜中晶核的生长与析出;从微观晶格的粉碎研磨,再到法规与专利权杖下的市场角逐——盐与共晶的开发是一项融合了化学热力学、物理药剂学、化学工程学以及法规科学的系统性跨界工程。
在药物生命周期的管理中,通过不断的筛选验证、精密的相图指导放大以及严密的剂型保护,不仅可以化解早期药物因水溶性低下而夭折的风险,更能在产品上市后迭代出更优良的疗效、更低的副作用与更高的患者依从性。盐与共晶作为晶体工程学中最锋利的长矛,将继续在现代药用固体材料的探索之路上开疆拓土。
扩展阅读:
2. 深度解析生物利用度:从Cmax/AUC到FDA监管,揭秘制剂工艺与临床疗效的核心纽带
3. 地高辛之殇到BCS豁免:一部生物等效性(BE)研究演进史,如何为仿制药安全性与可及性保驾护航
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论