
在生物医药行业的深度投研与管线分析中,无论是评估创新药企的全球化市场拓展,还是审查仿制药的合规与商业化潜力,生物等效性(BE)试验都是不可或缺的核心枢纽。我们在日常利用摩熵医药等相关专业数据库追踪企业研发管线,或通过 FDA 辅料数据库(IIG)逆向拆解制剂处方时,最终都要回归到一个根本问题:该制剂在人体内的药代动力学(PK)表现是否真正等效。
基于对国内及国际主流监管体系的深度梳理,本文将系统性重构并全景解析以药代动力学为终点的生物等效性试验的底层逻辑与实操架构。
一、 核心准则:以药代动力学(PK)为终点的评价逻辑
对于绝大多数口服及常规给药制剂,BE 研究的核心目标是精准捕捉药物从制剂中释放并进入体循环的动态过程,这需要将受试药品(Test)与参比药品(Reference)在机体内的全身暴露量进行严格的比对。
从学术和监管的严谨定义来看,以 PK 参数为终点的 BE 研究,其本质是通过精密仪器测定可获取的生物基质(如全血、血浆或血清)中的药物浓度,从而推导出核心的药代动力学参数作为终点评价指标。这一过程能够直观且量化地反映出药物活性成分被吸收进入循环系统的速率与程度。在评价体系中,峰浓度(Cmax)和药时曲线下面积(AUC)是两大基石指标。在极少数情况下,若血液基质中的目标分析物极难准确定量,也可退而求其次,通过测定尿液中的药物排泄浓度来开展等效性评价。
监管层面对此亦有着严密的历史演进。早在2005年3月,国家药品审评中心(CDE)便出台了针对化学药物制剂的人体 BE 研究技术指导原则。随着仿制药一致性评价的推进,NMPA 在2016年3月发布了更为详尽的《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则》。此后,2020版《中国药典》第四部更是以国家药典的高度,对 BE 试验提出了极具指导性的规范。当前高水平的 BE 设计,必须在融合这些国内标准的同时,深度对标美国 FDA、欧洲 EMA 以及日本 PMDA 的指导意见,从受试者筛选、样本量博弈到统计学边界,进行全方位、系统性的考量。
二、 临床研究模式的精准定位
在启动一项 BE 研究之前,首要任务是确定恰当的给药与进食条件模型。这直接关系到试验的敏感度与最终结果的可靠性。
1. 单次给药 vs. 多次给药的敏感度博弈
在评价制剂释放速度与程度的敏感性方面,单次给药生物等效性研究(Single-dose BE Study)具备天然且无法替代的优势,通常被各国监管机构作为评价口服固体制剂等效性的首选与推荐标准。其底层逻辑在于:单次给药在捕捉药物释放速率和吸收程度的微小差异方面,远比多次给药达到稳态后的研究模型更为敏感。稳态水平往往会掩盖制剂间由于释药行为不同而产生的早期血药浓度波动。
然而,科学研究必须兼顾伦理与受试者安全。若受试药物存在显著的安全隐患,必须在正在接受该药物治疗且不可停药的患者群体中开展试验时,则妥协方案是进行多次给药达稳态后的 BE 研究。
2. 空腹与餐后状态的双重验证
食物的摄入会改变胃肠道 pH 值、排空速率及胆汁分泌,从而显著干扰药物的生物利用度(BA)。因此,通过餐后 BE 研究来评估进食对受试制剂与参比制剂 BA 影响的差异,是常规制剂不可省略的一环。
- 口服常释制剂:标准操作是同时开展空腹和餐后双相 BE 研究。但存在豁免特例:若参比药品的官方说明书中严禁与食物同服(明确规定需饭前1小时或饭后2小时服用),则可合理免除餐后试验。反之,若药物仅能与食物同服,原则上也建议开展双相试验,除非有确凿的安全性数据表明空腹给药存在严重风险,此时方可仅保留餐后 BE 研究。
- 口服调释制剂:对于控释、缓释等复杂制剂,由于其释药机制易受胃肠道生理环境(尤其是高脂饮食引发的“突释”效应)影响,必须全面开展空腹与餐后 BE 研究。
三、试验设计的架构与统计学策略
试验设计不仅受制于药物自身的理化性质,更受其药代动力学特征的深刻影响。科学的试验设计是剥离噪音、揭示制剂真实差异的唯一途径。通常有三种经典架构:交叉设计、平行设计与重复设计。
1. 交叉试验设计:行业的“黄金标准”
在绝大多数生物等效性试验中,交叉试验设计是目前应用最多、也是最为经典的统计学方法。由于人体在药物吸收与代谢上存在巨大的个体差异,且个体间变异系数通常远超个体内变异系数,因此 BE 试验极度依赖于“自身对照”的逻辑。
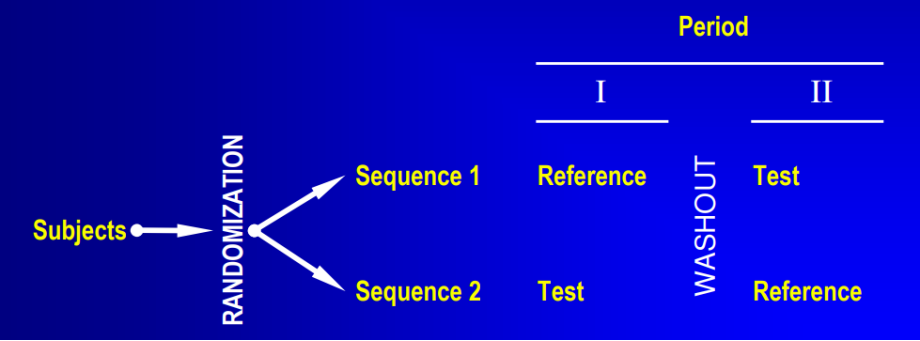
交叉设计能够极其有效地剔除个体间变异对等效性评价造成的统计偏倚。在同等样本规模下,交叉设计的统计检验效能远超平行设计。最经典的模型是“两制剂、两周期、两序列(2×2)”交叉设计。受试者被随机分入序列1(先 T 后 R)或序列2(先 R 后 T)。关键在于两次给药间必须设置充分的“清洗期”,以彻底阻断残留药物对下一周期的干扰,该清洗期通常要求长达7个以上的药物消除半衰期。
2. 平行试验设计:长半衰期药物的妥协之选
当药物或其活性代谢物的半衰期极长时,交叉设计便面临落地的困境。极长的半衰期意味着受试者需要经历长达数周甚至数月的清洗期(超过5个半衰期方可将浓度降至检测限以下),这不仅会带来极高的受试者脱落率,在患者中开展时更可能引发严重的伦理危机(如长时间停药)。
此时,平行试验设计成为备选。受试者被随机分为两组,每组仅接受一种制剂(T 或 R)。由于无法区分个体内与个体间变异,平行设计受个体间变异的冲击极大。因此,两组受试者在年龄、性别、体重、种族、甚至代谢酶基因型(快/慢代谢者)等人口学与生理特征上必须高度均衡。此外,为达到与交叉设计等同的统计效力,平行设计需要庞大得多的样本量。FDA 指南明确指出,对于半衰期 ≥30h 的药物,采用平行设计时,截取 60~96h 的血药浓度数据对证明等效性最有价值,而超过 120h 的数据采集往往缺乏实际意义。
3. 重复试验设计:破解高变异药物(HVD)的利器
部分药物的个体内变异极大(变异系数 CV≥30%),按常规 2×2 设计极难达到等效标准,此时需引入重复试验设计。其核心逻辑是将同一制剂在不同周期重复给予同一受试者,从而精准估算该制剂真实的个体内变异。
重复设计分为两类:
- 部分重复设计:通常为三周期(如单制剂重复,TRR/RTR/RRT)。
- 完全重复设计:通常为四周期、两序列(如 TRTR/RTRT)或四序列(如 TRRT/RTTR/TTRR/RRTT)。
在评价高变异药物时,参比药品标度平均生物等效性(RSABE)方法被广泛采用。通过重复设计精确测定参比药品的个体内变异后,可以在严密科学论证且不影响临床安全有效的前提下,将 80.00%~125.00% 的严苛等效限度作适当比例的拓宽。这有效避免了为追求极窄置信区间而招募海量受试者所带来的不必要的人群暴露风险。需要注意的是,Balaam 设计(TR/RT/TT/RR)在个体生物等效性(IBE)评价中因部分序列无法提供制剂间相互作用信息而应当避免。
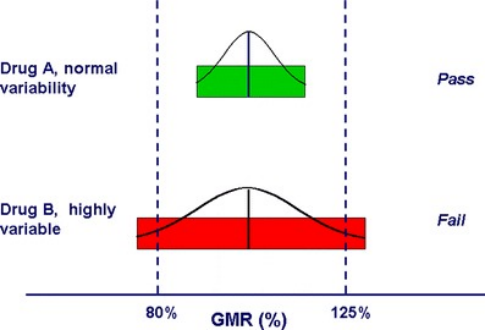
80%–125% 的生物等效性 (BE) 限值以两个“目标点”沿 x 轴表示。该 BE 限值与正常变异性药物(药物 A)和高变异性药物(药物 B)的试验/参考 BE 测量几何平均比值 (GMR) 的假设 90% 置信区间进行比较。如果使用更多受试者,高变异性药物 B 很可能达到 BE 限值。来源:Davit, BM, Chen, ML., Conner, DP 等。美国食品药品监督管理局实施高变异性仿制药产品变异性图表的参考标度平均生物等效性方法。AAPS J 14, 915–924 (2012)。https://doi.org/10.1208/s12248-012-9406-x
四、受试者群体的科学筛选与队列构建
为了最大程度剥离与药品制剂差异无关的混杂因素(如疾病状态造成的吸收/代谢改变),BE 试验的默认人群是健康志愿者。FDA 和 EMA 的指导原则均强调了这一点,要求受试者的健康状况必须通过详尽的病史询问、全面的体格检查和实验室检验予以确认。
然而,绝对的安全底线不可逾越。若目标药物(如抗肿瘤细胞毒性药物)对健康人群具有不可接受的药理毒性或潜在危害,则必须打破常规,在严格的临床监护下将试验受众替换为目标适应证的患者群体,并确保患者在试验期间病情处于稳定期。
在常规健康受试者的入组标准上,必须遵循以下队列分布原则:
- 基础特征:年龄需 ≥18 周岁,体重指数(BMI)严格控制在 19 ~ 26kg/m2 的标准区间内。
- 人口学代表性:受试队列必须涵盖目标人群的普遍特征。若药物拟用于全人群,受试者必须保持合理的男女比例配置。若药物定位为老年专属用药,则应尽可能提高60岁以上高龄受试者的入组比例。
- 生活方式与基因型管控:为排除外源性代谢诱导或抑制,受试者最好无吸烟习惯,严禁酗酒及药物滥用。对于特定靶向或强代谢依赖型药物,必须提前对受试者的代谢酶表型或基因组学特征进行分层考量。同时,在针对特定仿制药的研究中,女性受试者常被要求处于非孕期及非哺乳期状态。
五、统计学效能与样本量估算
BE 试验不是简单的数值比较,而是一场严密的统计学检验。样本量的多寡不仅牵涉巨大的财务与时间成本,更关乎伦理与科学结论的确定性。各主要监管区对最小样本量存在差异化底线:美国要求 24~36 例,欧盟要求至少 12 例,日本为 20~30 例,中国通常为 18~24 例。
在基于平均生物等效性(ABE)的方法论下,样本量估算受制于以下核心变量:
(1)显著性水平(α)与检验效能(1-β):通常 α 设定为 0.05(即控制一类错误发生率,防止“伪等效”),检验效能则绝不能低于 80%(确保有足够概率发现真实的等效性)。
(2)变异系数(CV):这是最棘手的变量。在经典的 2×2 交叉设计中,此参数来源于对数转化后方差分析得出的均方差根(RMSE),即个体内变异系数(CVW)。其数值多依赖于预试验或既往高质量文献的提取;若文献缺失,亦可依据已知参比制剂几何均值比(GMR)的 90% 置信区间(CI)宽度进行逆向粗估。
(3)几何均值比(GMR,θ=μT/μR):基于预期中受试药品与参比药品的真实差距,通常设定为 0.95(或 1.05);若预期工艺差距较大,则按 0.9(或 1.1)预估。
特殊药物的接受限度差异
一般情况下,判定等效的铁律是受试药品与参比药品的 Cmax 和 AUC 的 GMR 的 90%CI 必须完全落入 80.00% ~ 125.00% 的区间内。但这并非放之四海而皆准。
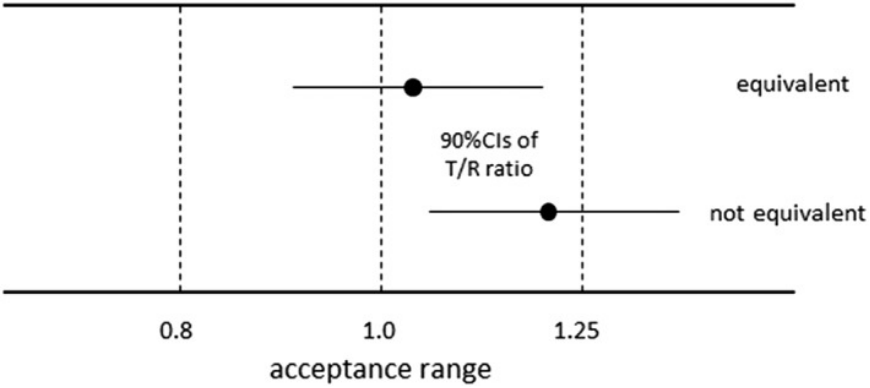
生物等效性试验的接受范围。CI,置信区间
- 窄治疗指数(NTI)药物:这类药物(如地高辛、华法林、环孢素)有效血药浓度与中毒浓度极度接近,极其微小的波动即可引发致命毒性或治疗失败。为此,监管机构对 NTI 药物实行严酷的限度收缩。中国药典、NMPA、FDA 以及 EMA 均倾向于将其 AUC 的可接受等效区间大幅缩窄至 90.00% ~ 111.11%。FDA 更是要求必须采用四周期完全重复交叉设计,并严控总体标准差比值。
- 高变异药物(HVD):与 NTI 药物相反,HVD 的个体内变异 CV ≥ 30%,但往往具有极宽的安全窗。若固守 80-125% 的界限,将迫使企业招募成百上千名受试者,这在临床实操与伦理上均不可接受。因此,在基于临床充分理由的前提下,全球监管体系均允许基于 RSABE 方法对其界限进行适度扩增。例如,NMPA 允许 Cmax 的接受范围最宽放宽至 69.84% ~ 143.19%,但通常出于保守原则,AUC 的接受限度依然死守在 80.00% ~ 125.00% 不变。
六、参比制剂(RLD)的严苛遴选机制
参比制剂是整个仿制药评价体系的“基准锚点”,选错参比,满盘皆输。CDE 与 NMPA 对此制定了极端严格的选用层级,其核心防线在于:坚决杜绝误差的代际传递与叠加放大。
举个简单的例子:如果原研药(A)绝对吸收率为 100%,仿制药(B)达到 A 的 85%,判定为等效;后续仿制药(C)若以 B 为参比且达到 B 的 85%,同样能获得针对 B 的等效结论。但此时,C 相较于原研锚点 A 的吸收率仅剩 72.25%,已经实质性跌出等效区间。因此,参比药品必须具备完整的安全性与有效性循证依据,是临床上不可替代的基石。
口服固体制剂的遴选铁律:
(1)原研首位顺位:永远将国内获批上市的原研药品置于第一顺位。若原研已实现本土化代工生产,在证明与海外原研质量一致后,亦可作为合法参比。
(2)国际同种与主流市场外推:若原研未进入国内市场,或证明其质量已不符合现代要求,可退而求选在国内上市的“国际公认同种药物”。若此路依然不通,则直接跨境放眼欧美日三大主流法制市场,选取当地上市并被明确登记为 RLD(Reference Listed Drug)的制剂。
需要特别警惕的两大注册陷阱:
(1)单纯改剂型申请:若将原研片剂改良为胶囊剂,BE 试验的对标物绝不能是市面上其他企业已经做出的胶囊剂,而必须回头去死磕原研发企业的“原剂型片剂”,改盐基品种同样适用此道。
(2)工艺变更与补充申请:仿制药一旦获批,若后续发生重大工艺与处方变更触发 BE 研究,其比对目标不能是自己变更前的老工艺产品,而必须再次向原研产品发起挑战。
七、采样时间矩阵与给药剂量界定
1. 采样矩阵:捕捉完整的动态全貌
药代动力学参数的真实性建立在高密度、高精度的生物样本采样之上。常规建议是,每个受试者在单一试验周期内必须采集 12~18 个包含给药前空白对照的血样。
时间轴的排布堪称一门艺术,必须完美覆盖吸收相、分布相与消除相。为精确锁定并消除速率常数(λz),采样点分布应当呈阶梯状前密后疏。
- 吸收相:安排 2~3 个时间点追踪药物浓度爬升。
- 峰值附近:这是兵家必争之地,在预期 Cmax 发生时间前后,需密集部署至少 3 个采样点,以防“漏峰”现象(预试验对于排雷首个采样点即为最高浓度的尴尬局面至关重要)。
- 消除相:需设置 3~5 个点,采样动作需持续推进直至覆盖受试药及其活性代谢产物 3~5 个完整的末端消除半衰期,或一直追踪到血药浓度跌落至 Cmax 的 1/20 ~ 1/10 处。无论如何,AUC0-t 必须能够覆盖外推至无穷大的 AUC0-∞ 总量的 80% 以上(长半衰期药物允许采用 AUC0-72h 截断线作为替代)。若存在因临床依从性导致的采血时间偏差,参数计算必须以实际采血时间戳为准,严禁造假套用计划时间。
2. 给药剂量的博弈:探索治疗边界
临床给药剂量通常直奔该制剂在市面上流通的最大单次给药规格而去,但绝对不得逾越说明书中标识的安全红线。T 制剂与 R 制剂必须严格执行等剂量对决。
- 线性 PK 体系:若药物在治疗窗内具备优良的线性药代动力学特征(即剂量的增加与 AUC 的扩增呈完美的比例线性关系),且该药物拥有多个上市规格。在最高规格存在受试者耐受性瓶颈或因强水溶性极易释药时,申请人可向下兼容,选择较低规格完成等效论证。只要各规格处方比例(辅料构成)具备高度相似性,且体外溶出曲线对比验证通过,即可实现规格间的等效豁免。
- 非线性 PK 体系:情况则复杂得多。若随着剂量爬升,AUC 发生超比例的非线性暴增,则必须咬紧牙关在最高规格下进行试验。反之,若 AUC 的增量被生理吸收饱和所压制(低于剂量增量比例),则往往被强制要求在“最高规格”与“最低规格”两极同时拉开防线,开展两组相互独立的 BE 试验。
八、临床合规基石:药品的抽样与封样留存
在监管日益严苛的当下,试验样品的真实可追溯性是防止学术造假与数据倒置的防弹衣。CDE 专门在《生物利用度和生物等效性试验用药品的处理和保存要求技术指导原则》中筑起了这道防火墙。

试验机构的随机抽样必须从申办方提供的同一批号产品中提取。无论是面对单一硕大容器、分散的多个容器,还是独立塑封的单位剂量包装,机构均需按既定比例抽取使用量与留存量。对于盲法试验,必须备足带有盲态编码的冗余样本组与救命的紧急揭盲信封。
留存数量的监管底线毫不退让:必须具备能够支持按国家法定质量标准进行5次全检的物质余量。以最常见的片剂或胶囊为例,受试制剂与参比制剂往往分别需要留底至少 300 个制剂单位。对于临用前临时配制的液态混悬制剂,留存的必须是其未接触溶剂的原始干燥状态。更为严厉的是,这批肩负着审计重任的留存样本,必须在试验基地静默冷藏至少至药品获批上市后的2周年;机构亦可将其移交至符合资质的独立第三方保管,但绝对禁止私自返还给存在直接利益冲突的申办方企业。
结语
综上所述,一份能够经得起监管穿透式审查与市场检验的 BE 报告,绝不仅是冷冰冰的 PK 参数堆砌。它凝结了对受试药物深度理化特性的拆解、精准的受试者队列分层、严谨的统计边界博弈以及对伦理与合规红线的绝对敬畏。在医药研发的浩瀚长征中,BE 试验如同那把丈量真理的卡尺,刻画着每一粒药片背后对患者生命质量的庄严承诺。
扩展阅读:
1. 深度解析生物利用度:从Cmax/AUC到FDA监管,揭秘制剂工艺与临床疗效的核心纽带
2. 解锁口服药物吸收密码:溶解性、渗透性及S-P矛盾全解析
3. 创新药降本增效的核心密码:深度解析现代工艺开发新技术,合成生物化学等三大工艺成核心驱动力!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论