2026年作为“十五五”开局之年,中国生物医药产业迎来战略定位的历史性跃升。全国两会政府工作报告首次将生物医药明确列为国家层面新兴支柱产业,与集成电路、航空航天、低空经济等核心战略产业并列。同期,国家药监局明确,自2026年3月31日起新实施的药物临床试验全面适用ICHE6(R3)标准,推动我国临床试验质量管理与国际全面接轨。
在政策红利释放与全球产业转移的双重驱动下,中国已从临床试验“承接地”升级为全球医药创新策源地。临床试验是衔接基础研究与产业转化的关键枢纽,其申办方格局、机构分布及阶段特征,深刻映射着中国医药创新生态的结构与演进方向。本文内容摘编自摩熵咨询《2025年中国临床试验数据洞察》报告,依托摩熵医药数据库对全国临床试验登记信息的全量追踪与深度治理,从申办方属性、头部企业竞争格局、试验阶段布局及临床机构地域分布四大维度,系统解析2025年中国临床试验的核心格局与发展态势。
一、内资企业领跑临床试验申报,创新研发活力持续高位
2025年临床试验登记中,内资企业占比达93.4%,外资企业仅占6.6%,本土药企在临床申报中占据核心地位。
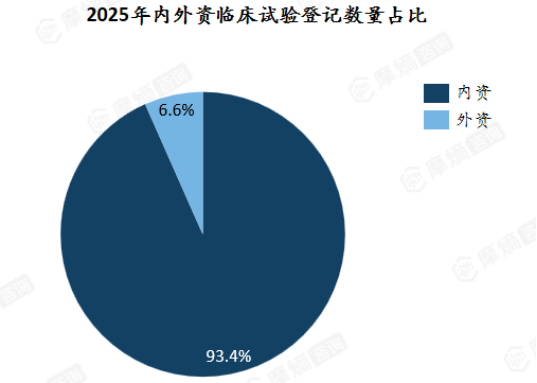
数据来源:摩熵医药-中国临床试验数据库
从季度趋势看,内资企业临床试验登记量呈现“先升后降”态势,Q3达到峰值1329项,Q1-Q4均维持在1100项以上,显示创新研发活跃度持续高位。
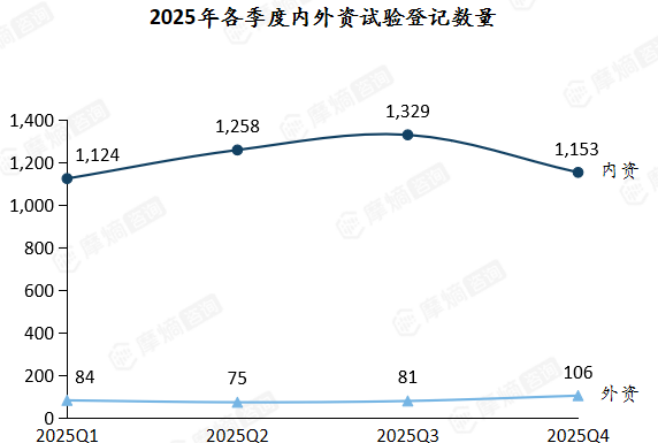
数据来源:摩熵医药-中国临床试验数据库
外资企业方面,季度登记量稳定在100项左右,第四季度小幅增长至106项,在华临床布局稳步推进。整体来看,内资企业依然是中国临床试验申报的绝对主力,内外资企业的格局保持稳定:内资企业主导,外资企业稳步参与。
二、恒瑞领跑TOP20榜单,头部药企临床活跃度凸显
在2025年临床试验申办方TOP20榜单中,恒瑞医药以绝对优势领跑,石药集团、正大天晴等本土龙头紧随其后,形成第一梯队,以创新药与仿制药双轮驱动的发展模式,持续深化在临床试验领域的布局。
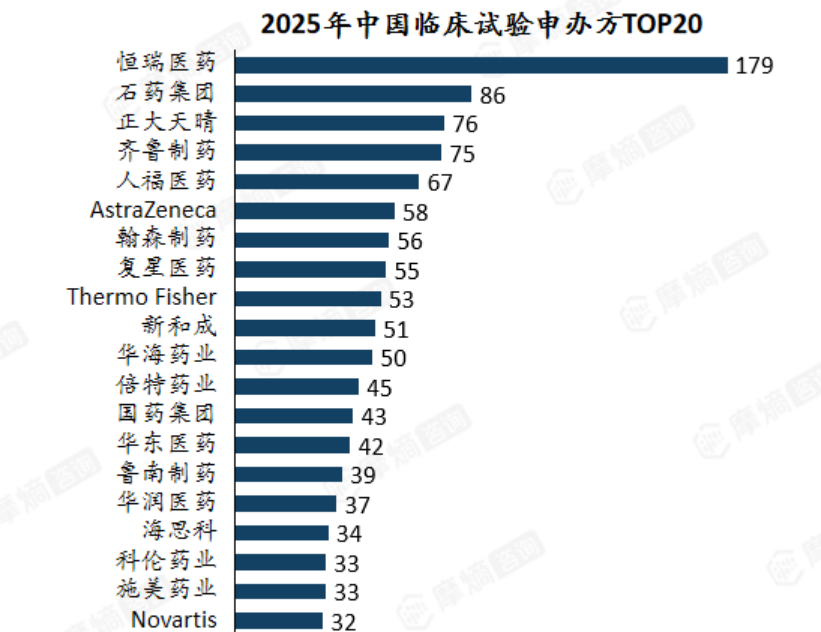
数据来源:摩熵医药-中国临床试验数据库
在内资阵营中,恒瑞医药的领跑态势并非偶然。根据其2025年年报,公司全年研发投入达87.24亿元,占营收比例27.58%,创新药销售收入同比增长26.09%至163.42亿元,贡献总药品销售的58.34%。报告期内,28项临床推进至III期,61项进入II期,28项创新产品首次进入I期,100多个自主创新产品处于临床开发阶段,同时在国内外推进400余项临床试验。这一“创新药一哥”的临床申报密度,正是中国本土药企研发实力跃升的缩影。
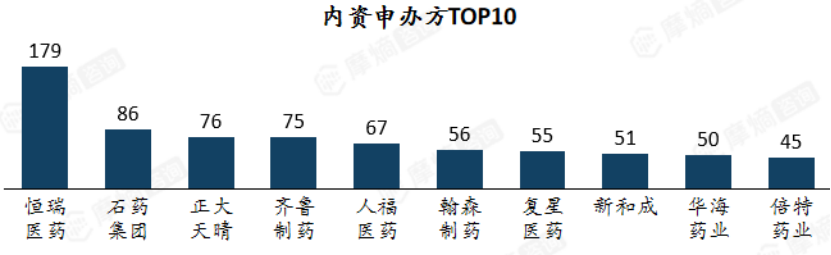
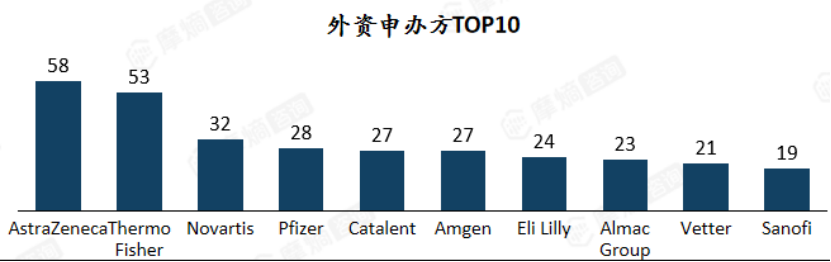
外资阵营中,阿斯利康、赛默飞等企业位列前茅,CDMO与创新药企业并重,聚焦前沿疗法布局。阿斯利康凭借其全球研发网络与中国本地化策略,持续推进肿瘤、呼吸、心血管等领域的临床试验;赛默飞则依托其CDMO平台优势,为全球药企提供临床试验外包服务,聚焦创新疗法与精准医疗领域。
三、内资聚焦创新探索,外资重后期商业化布局
摩熵咨询的报告进一步揭示了一个关键的结构性差异:内外资企业在临床试验阶段的布局上形成了鲜明的战略分野。
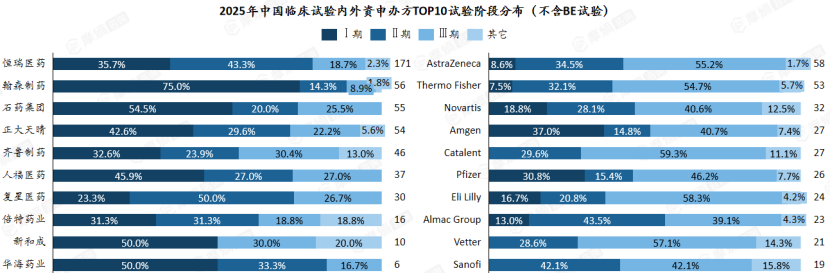
数据来源:摩熵医药-中国临床试验数据库
内资企业以早期临床为核心,侧重本土创新与管线拓展。大量Ⅰ期、Ⅱ期试验的密集开展,体现了本土药企“从0到1”的源头创新能力正在加速释放。
外资企业则以后期临床为核心,III期及注册性临床试验占比更高,侧重全球管线在中国市场的落地与转化。Ⅲ期试验及上市后研究的持续推进,体现了“从1到N”的商业化导向与上市潜力。
整体来看,内资驱动创新探索,外资主导后期验证,二者形成优势互补、协同发展的良性生态。这种分工格局共同推动中国医药创新生态的繁荣发展,为中国患者提供更加丰富的治疗选择与临床获益。
四、头部临床机构地域分布集中,中东部省份活跃度领先
一场成功的临床试验,除了强有力的申办方,更离不开高效运转的临床研究机构。2025年TOP20临床机构的省域分布数据揭示:头部临床机构的地域分布呈现高度集中特征,中东部省份在临床试验活跃度上呈压倒性领先态势。
2025年TOP20临床机构省份活跃度分布(以试验登记数量计)
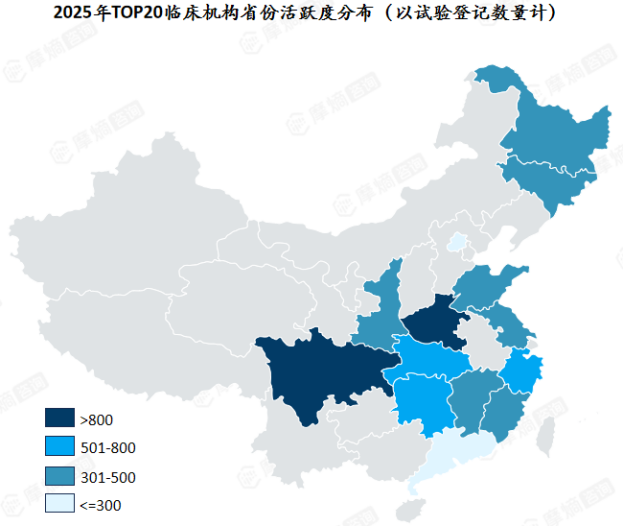
从地域分布来看,TOP20的临床机构几乎被中东部经济活跃省份“包揽”。无论是长三角的上海、江苏,还是山东、福建、江西,亦或是珠三角的广东,这些地区的临床中心不仅拥有顶尖的医疗硬件,更具备高效的患者招募能力与国际化合规意识。中东部省份在医药研发端的活跃度,无疑走在了全国前列。
数据来源:摩熵医药-中国临床试验数据库
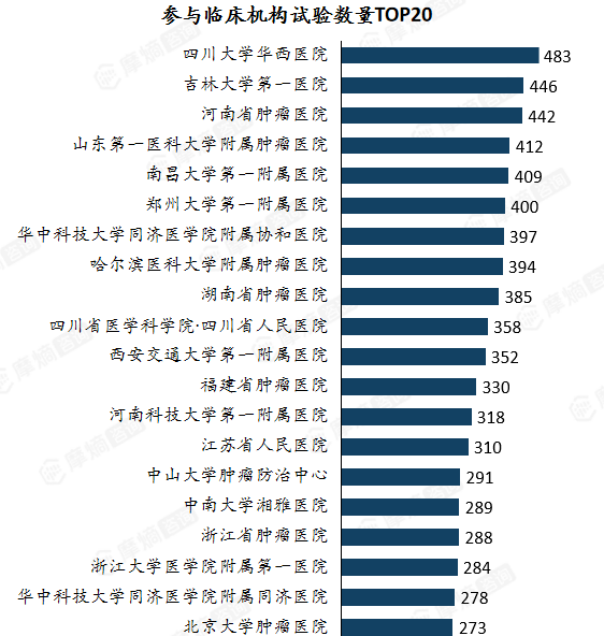
在TOP20临床机构名单中,综合性三甲医院和专科龙头医院占据了主导地位。其中,四川大学华西医院以483项试验高居榜首,吉林大学第一医院(446 项)、河南省肿瘤医院(442 项)分列二、三位。
结语:
纵观2025年,中国临床试验在申办方格局与机构分布上展现出强大的韧性与清晰的演进逻辑。内资企业的蓬勃活力与外资企业的稳健深耕交相辉映,共同构筑起富有中国特色的医药创新生态。在这场研发竞逐中,数据不仅是结果的记录,更是战略的指南。摩熵医药数据库以全面、精准、实时的数据能力,剥离市场噪音,还原行业基本面;而摩熵咨询《2025年中国临床试验数据洞察》报告,则是对海量数据的深度提炼。这不仅是审视过往的“成绩单”,更是预判未来的“导航仪”,为从业者、投资者及监管层提供关键决策坐标,助力中国医药创新穿越周期,行稳致远。
相关拓展阅读:
1. 2025年中国临床试验数据洞察报告:新药占比近六成,BE试验增速亮眼!
2. 2025年中国临床试验数据洞察:药品类型与治疗领域全景分析
以上内容均来自摩熵咨询《2025年中国临床试验数据洞察》,如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论