
4月20日,石药集团发布公告,宣布其自主开发的注射用西罗莫司(白蛋白结合型)(HB1901)用于治疗晚期恶性血管周围上皮样细胞瘤的Ib/III期临床研究已顺利达成预设主要疗效终点。研究结果兼具显著的统计学差异与明确的临床获益,该药有望填补国内相关治疗空白,成为晚期恶性PEComa的首款标准治疗方案。

截图来源:企业公告
一、改良新药破局递送难题,国内首款静脉剂型填补空白
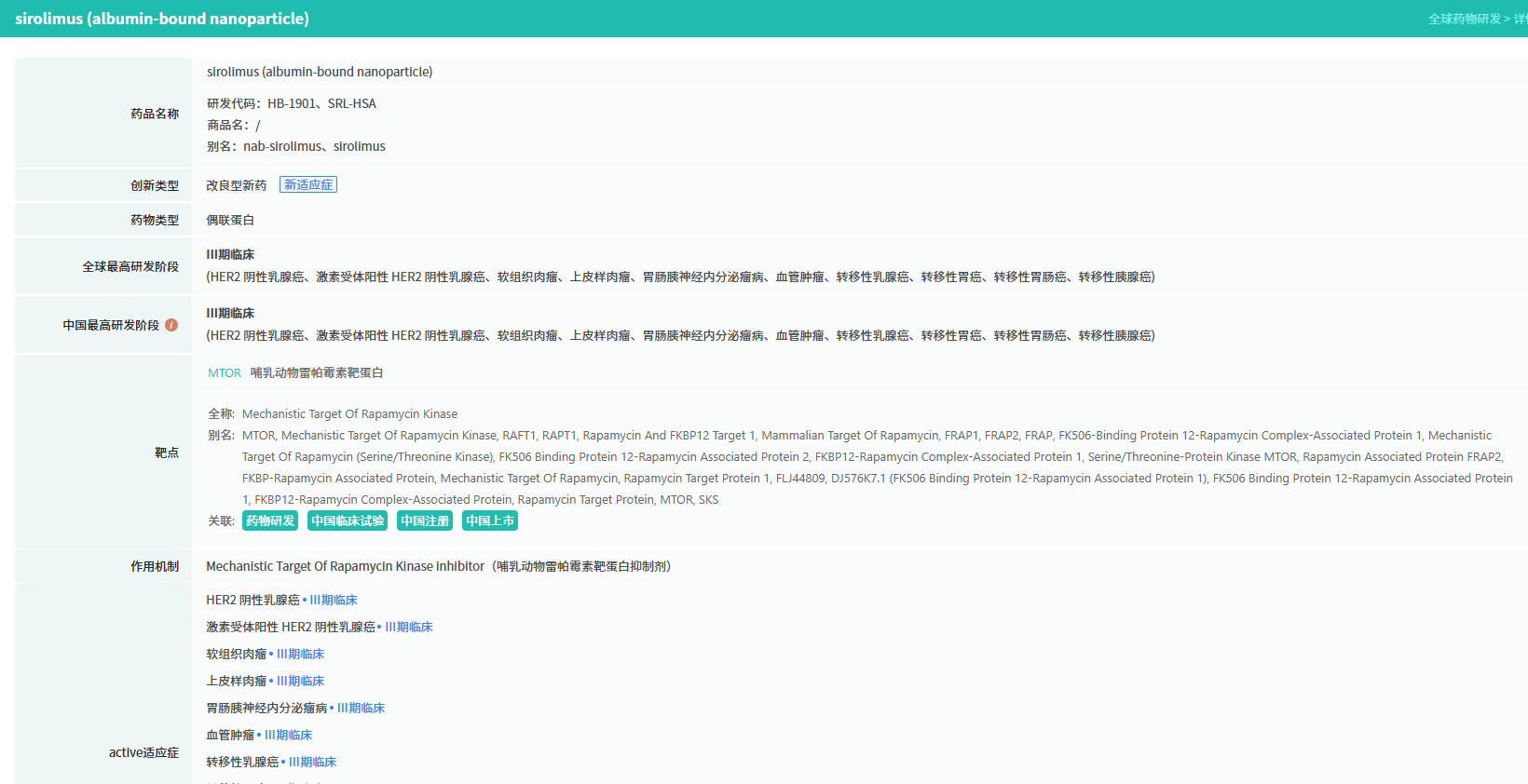
HB1901为西罗莫司白蛋白结合型纳米颗粒注射用混悬液,其活性药物成分为西罗莫司,依据《药品注册管理办法》属于化学药品注册分类2.2类改良型新药。
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
西罗莫司水溶性差,难以有效递送,限制了其在抗肿瘤领域的应用。HB1901采用创新技术将西罗莫司包裹于人血白蛋白中,是国内首个获得临床许可的静脉给药西罗莫司制剂。该剂型有效克服了传统口服制剂生物利用度低、靶部位递送不足的缺点,有望显著提高生物利用度并降低消化系统毒性。
2025年2月,HB1901已获得国家药监局授予的突破性治疗药物认定,其临床潜力获得认可。
二、直面巨大未满足需求,III期头对头研究验证临床价值
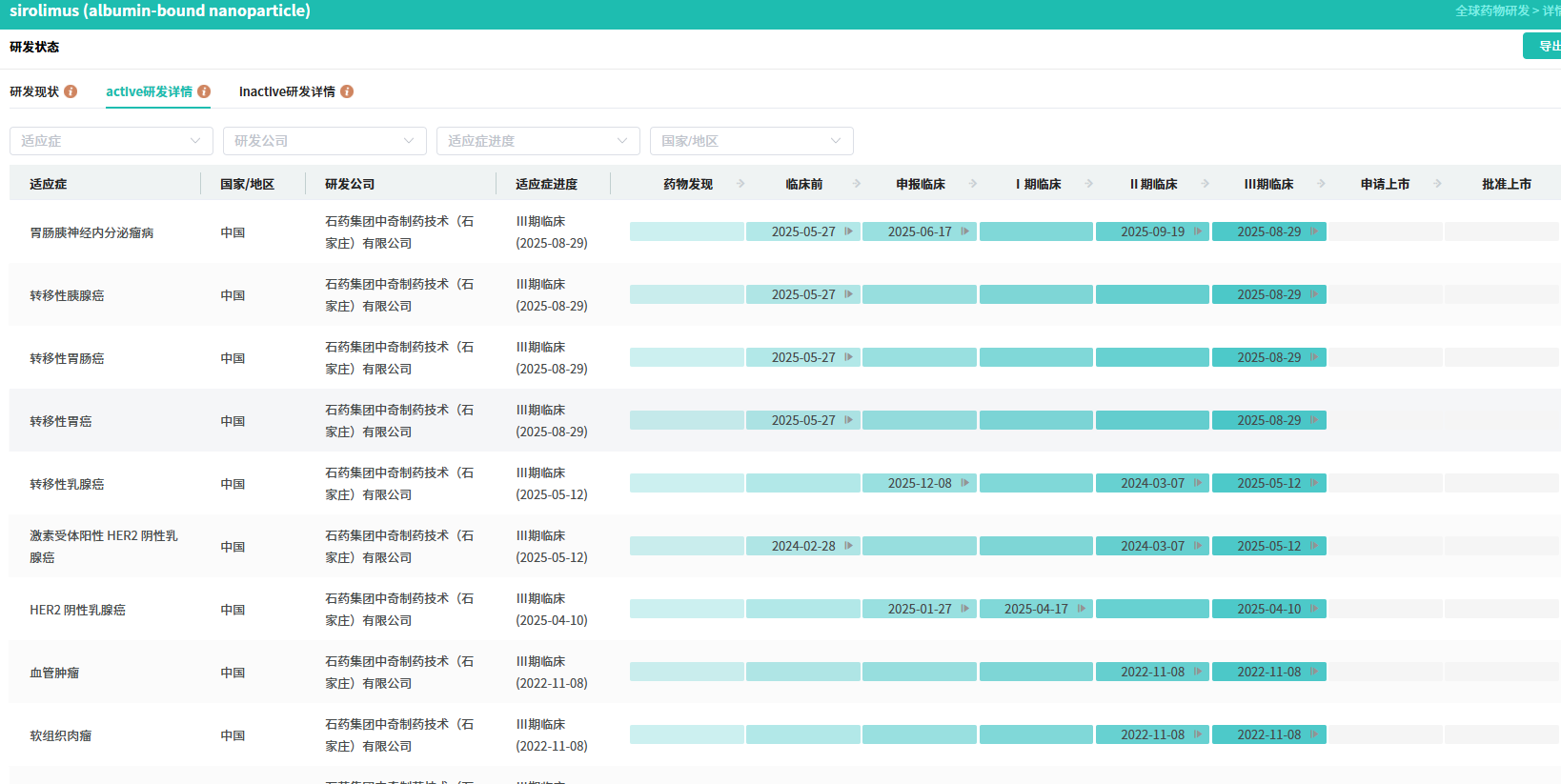
HB1901-004研究的核心III期部分采用头对头设计,对照研究者优选方案,全面评估了HB1901在晚期恶性PEComa患者中的抗肿瘤疗效、临床获益及安全性。其成功达终点,为该罕见难治肿瘤提供了新的高效治疗选择。
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
恶性PEComa是一种罕见的侵袭性间叶源性肿瘤。约半数患者在确诊时已属晚期,常伴有转移,预后较差。对于无法手术、术后复发或转移的晚期患者,国内目前缺乏公认的标准治疗方案,临床存在迫切的未满足需求。HB1901有望填补这一空白,成为国内该适应症的首款标准治疗。
三、研发管线梯队渐成,多领域创新药步入收获期
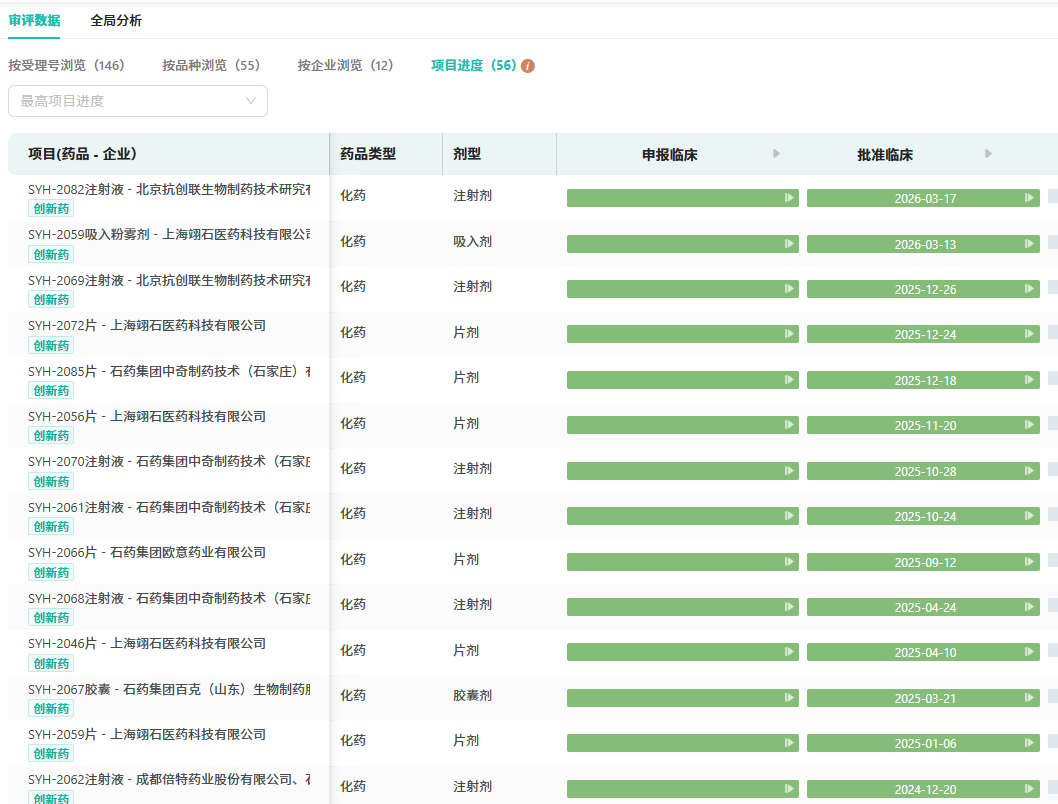
HB1901仅是石药集团创新研发的缩影。摩熵医药数据显示,在化学新药领域,石药集团目前已有超50款1类新药进入临床及以上阶段。
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论