
4月22日,国家药监局药品审评中心(CDE)官网显示,信达生物两款1类新药获批临床试验。其中 IBI3031是一款靶向IGF-1R/TSHR的双特异性抗体,拟用于治疗甲状腺眼病;IBI115 则为靶向DLL3/CD3的双抗,拟开发用于晚期小细胞肺癌。两款新药的同步获批,进一步丰富了信达生物在双特异性抗体领域的管线布局。
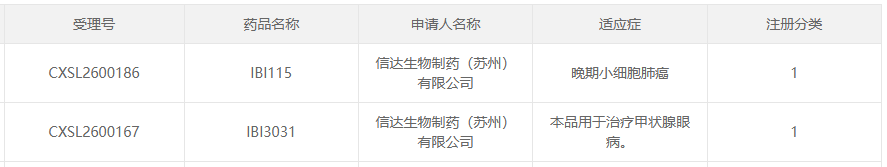
截图来源:CDE官网
一、核心管线登陆ASCO,公布全球首创IBI363关键临床数据
同日,信达生物对外宣布,其核心产品 IBI363(PD-1/IL-2α-biased 双特异性抗体融合蛋白)与 信迪利单抗(达伯舒®)的多项临床研究结果,将在2026年美国临床肿瘤学会(ASCO)年会上公布。本届年会定于2026年5月29日至6月2日在美国芝加哥举办。

截图来源:企业官微
在ASCO上,信达生物将公布 IBI363 在非小细胞肺癌免疫耐药及一线治疗方面的概念验证数据。基于在免疫耐药NSCLC患者中取得的成熟结果,IBI363 已快速进入全球多中心关键注册临床阶段。
据摩熵医药数据库显示,信达生物目前已有14款双抗创新药进入临床阶段,形成梯队化输出。除 IBI363(已进入III期临床)外,全球首个进入临床的IL-4Rα/TSLP双抗IBI-3002也正处于II期研究,用于中重度特应性皮炎。
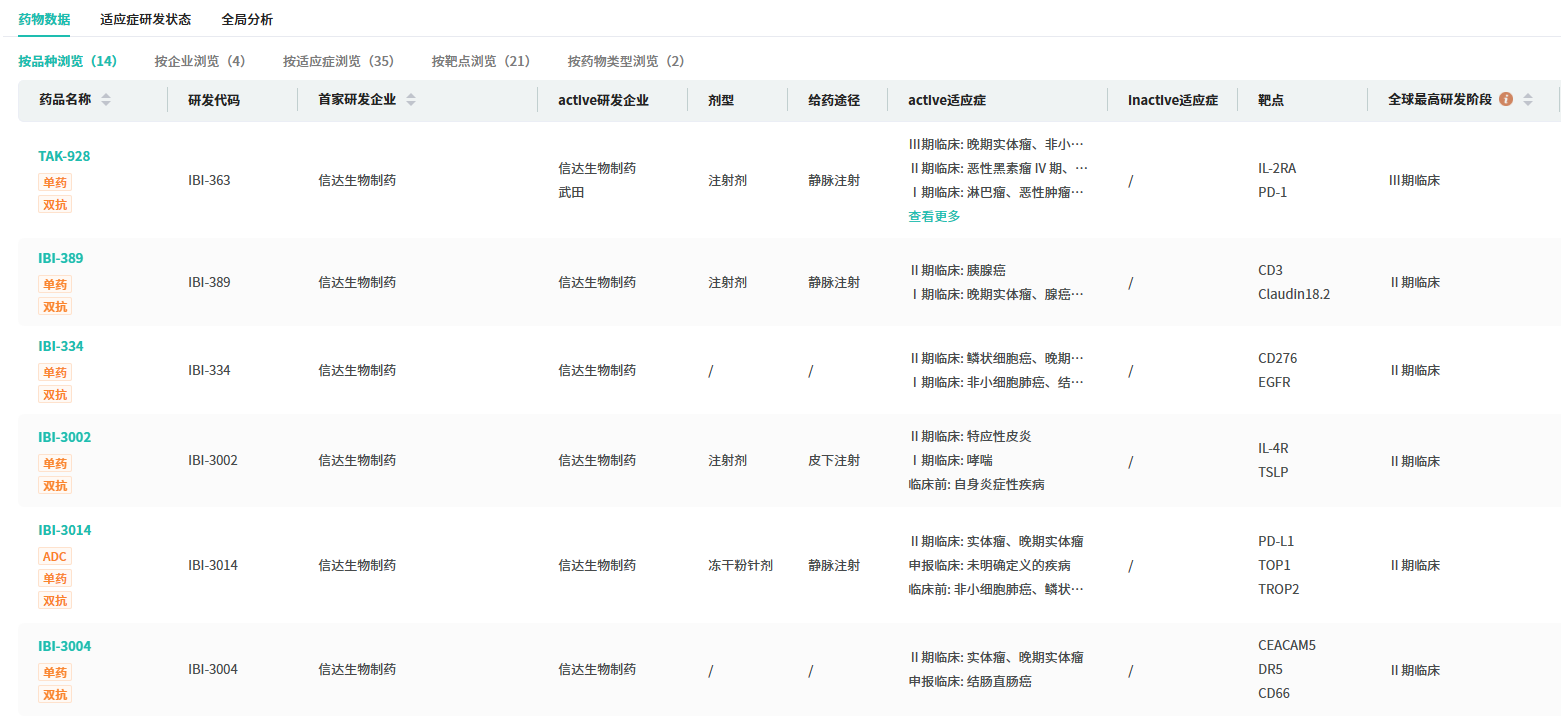
查数据,找摩熵!图源:摩熵医药-中国药品审评数据库
二、百亿营收、首次全年盈利,商业化“反哺”创新管线加速
核心管线的积极进展离不开公司强大的商业化支持,近年来信达生物在商业化方面也取得了显著成果。两款新药快速获批的背后,是信达生物已构建起的强大自我“造血”体系。
2025年全年业绩报告显示,公司实现总收入130.42亿元,同比增长38.4%;产品收入达118.96亿元,同比增长44.6%,首次突破百亿元大关。增长引擎不仅来自其在肿瘤领域的领先优势,也得益于心血管、代谢等综合产品线的快速放量。
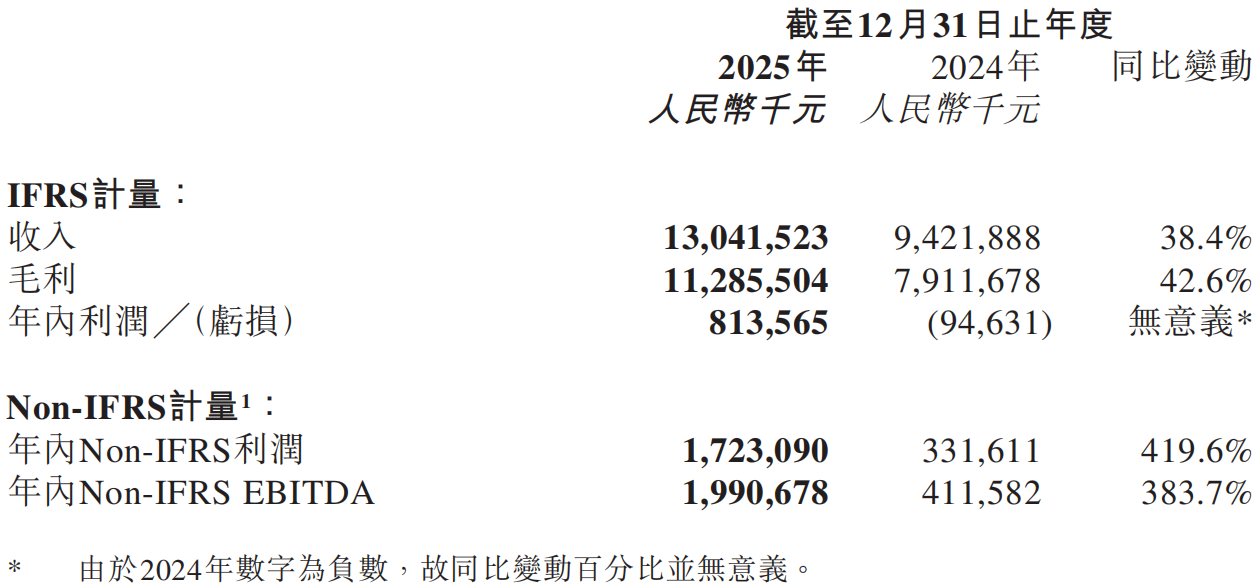
截图来源:企业年报
更具里程碑意义的是,公司首次实现IFRS准则下的全年盈利,净利润达8.14亿元,成功扭转2024年的亏损局面。
Non-IFRS净利润高达17.23亿元,同比激增 419.6%。与此同时,公司前瞻性布局的“IO+ADC”战略已进入价值收获期。其中,IBI363(PD-1/IL-2α-bias)和 IBI343(CLDN18.2 ADC)等三项资产已推进至全球注册性临床,其潜在目标市场规模合计超过600亿美元。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论