1.4.1 本周全球TOP10创新药研发进展
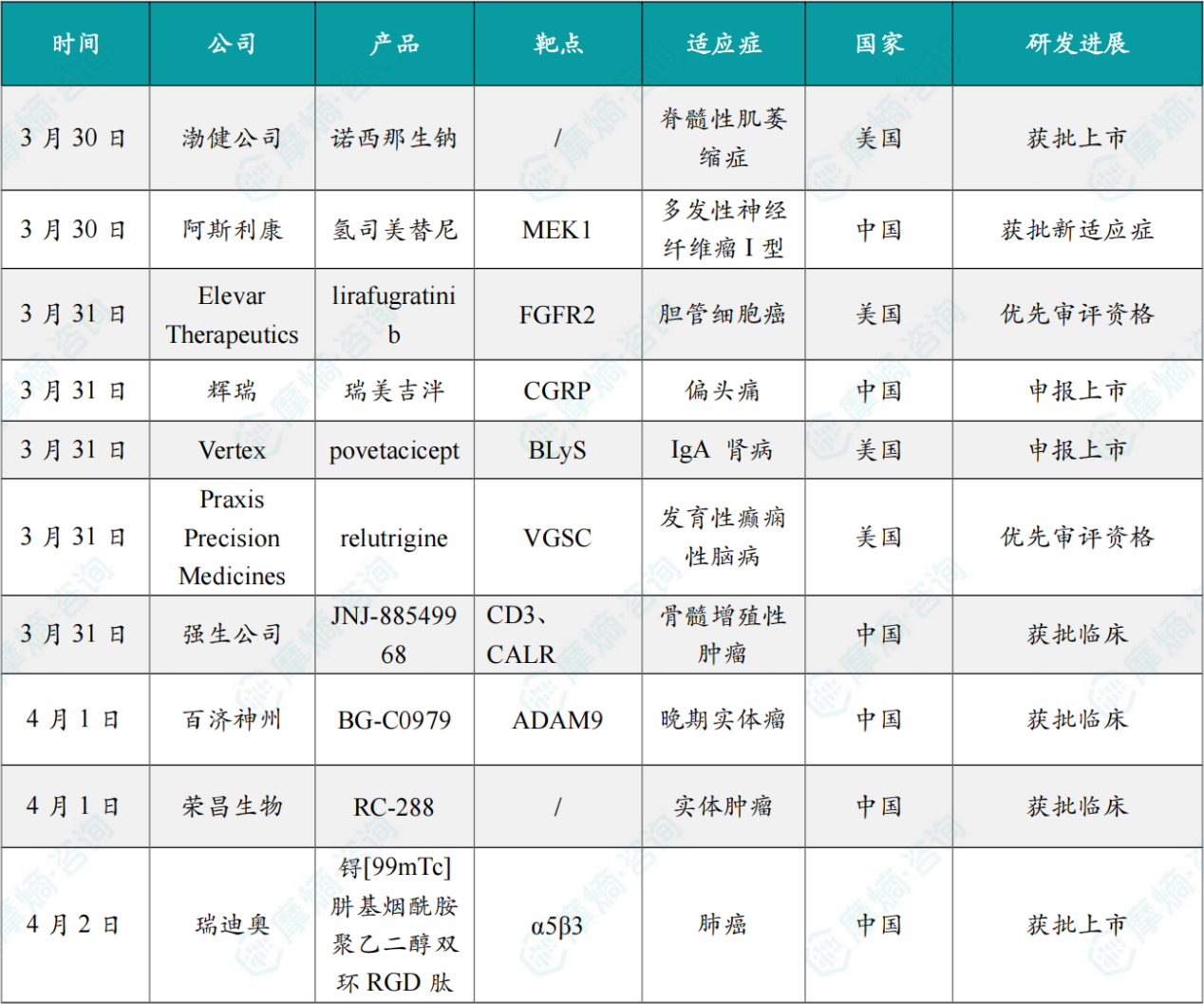
(1)渤健高剂量治疗脊髓性肌萎缩症新药获批上市
3月30日,美国FDA正式批准了渤健公司(Biogen)旗下药物SPINRAZA®(nusinersen)的全新高剂量治疗方案。
SPINRAZA®作为一种处方药,专门用于治疗儿童和成人脊髓性肌萎缩症患者,需要在拥有腰椎穿刺经验的医疗专业人员的指导下进行鞘内注射。
此次获批的高剂量方案正是在过去十年低剂量(12毫克)方案积累的临床数据基础上研发的。高剂量SPINRAZA®旨在通过负荷和维持给药阶段提供更高浓度的药物,从而为满足患者群体不断变化的需求提供新的选择。
(2)阿斯利康宣布MEK抑制剂司美替尼在华获批新适应症
3月30日,阿斯利康(AstraZeneca)宣布,中国国家药品监督管理局(NMPA)已正式批准硫酸氢司美替尼胶囊,一种选择性、口服MEK抑制剂,用于3岁及3岁以上伴有症状、无法手术的丛状神经纤维瘤(PN)的1型神经纤维瘤病(NF1)儿童及成人患者的治疗。
司美替尼在儿科患者中的真实世界使用经验已充分证实其在儿童NF1-PN患者中的疗效;而作为针对伴有症状且无法手术的NF1‑PN成人患者开展的3期临床试验,KOMET研究进一步验证了司美替尼能够显著控制肿瘤进展、改善患者临床症状,并展现了良好的安全性,有望实现对儿童到成人NF1-PN 患者的全生命周期守护。
(3)FDA授予Elevar Therapeutics抗癌小分子优先审评资格
3月31日,Elevar Therapeutics今日宣布,美国FDA已受理其在研疗法lirafugratinib的新药申请(NDA),用于治疗既往接受过治疗、且携带FGFR2融合或重排的胆管癌(CCA)患者。FDA并授予该申请优先审评资格,并预计将于2026年9月27日前作出审评决定。
此次优先审评主要基于1/2期ReFocus临床试验的积极数据。结果显示,lirafugratinib实现了46.5%的确认客观缓解率(ORR),且总体安全性表现可预测,并可通过剂量调整进行管理。
(4)辉瑞偏头痛口服预防药物在华申报上市
3月31日,CDE网站显示,辉瑞的硫酸瑞美吉泮口崩片在华申报新适应症,用于预防性治疗成人阵发性偏头痛。
瑞美吉泮是全球首个且唯一个采用专利口崩片技术的降钙素基因相关肽(CGRP)受体拮抗剂,于2020年2月首次获FDA批准上市,用于急性治疗成人急性偏头痛。2021年5月,瑞美吉泮在美国扩展新适应症,用于预防成人发作性偏头痛。2024年1月,该药物首次在中国获批上市。据辉瑞财报,瑞美吉泮在2025年的全球销售额为14.24亿美元。
(5)Vertex的Povetacicept在美国完成申报上市
3月31日,Vertex宣布已在美国完成Povetacicept的滚动生物制品许可申请(BLA)工作,并使用了一张优先审评券,以寻求FDA加速批准Povetacicept用于治疗IgA肾病。
Povetacicept是一种靶向B细胞激活因子(BAFF)和增殖性诱导配体(APRIL)的双重抑制剂,以此抑制B细胞激活、分化和/或存活,从而治疗多种自身免疫性疾病。
此次滚动BLA是基于III期RAINIER研究的积极结果。中期分析结果显示,第36周时,Povetacicept(80mg,每4周1次,皮下注射)组患者的24h尿蛋白肌酐比(24h-UPCR)较安慰剂组下降了49.8%(-52.0% vs -4.2%,P<0.0001),差异具有显著的统计学意义和临床意义。在所有预先指定的亚组中,蛋白尿也呈现出一致的下降趋势。
(6)Praxis Precision Medicines宣布在美国获优先审评资格,治疗癫痫性脑病
3月31日,Praxis Precision Medicines宣布,美国FDA已受理其候选药物relutrigine的新药申请(NDA),用于治疗由SCN2A和SCN8A基因突变引起的发育性和癫痫性脑病(DEEs),并授予该申请优先审评资格,FDA预计将在2026年9月27日之前作出审评决定。
此次NDA申请主要基于EMBOLD研究的积极结果。该研究在中期分析后,经数据监测委员会建议,因疗效显著而提前终止。目前,relutrigine也正在EMERALD临床试验中评估其在更广泛DEEs患者群体中的疗效,该研究预计将于2026年底完成。
根据新闻稿,若最终获批,该药物有望成为首个获FDA批准用于治疗SCN2A/SCN8A相关DEEs的疗法。
(7)强生1类新药在中国获批临床,针对骨髓增殖性肿瘤
3月31日,中国国家药监局药品审评中心(CDE)官网公示显示,强生公司(Johnson & Johnson)申报的1类新药JNJ-88549968注射液获批临床,拟开发治疗骨髓增殖性肿瘤。
公开资料显示,这是强生在研的一款靶向CALRmut×CD3的双特异性T细胞重定向抗体。
(8)百济神州新型ADC在国内获批临床
4月1日,CDE官网显示,百济神州注射用BG-C0979获批临床,用于治疗晚期实体瘤。这是国内第二款获批临床的ADAM9 ADC。
此前2026年2月,百济神州已经在Clinicaltrial网站上登记了一项评估BG-C0979单药治疗或与替雷利珠单抗联合治疗晚期实体瘤患者的安全性、耐受性、药代动力学和初步抗肿瘤活性的I期临床(NCT07414836)。
目前全球在研的ADAM9 ADC中进入临床阶段的有3款,分别是MacroGenics的MGC028、映恩生物的DB-1317和百济神州的BG-C0979。
(9)荣昌生物双抗ADC癌症1类新药获批临床
4月1日,荣昌生物宣布,公司自主研发的双抗ADC药物RC288,正式获得中国国家药品监督管理局药品审评中心(CDE)批准,将开展单药治疗局部晚期不可切除或转移性恶性实体肿瘤的1/2a期临床试验。
RC288是一款同时靶向PSMA和B7H3的双特异性ADC,是荣昌生物采用新一代偶联及毒素技术开发的创新药物分子。PSMA全称前列腺特异性膜抗原,是一种Ⅱ型跨膜糖蛋白,其支持肿瘤生长和血管生成;B7H3是一种免疫检查点分子,当其在肿瘤中过表达时,会促进免疫逃逸和肿瘤进展。PSMA及B7H3均是极具潜力的治疗靶点,在多种恶性肿瘤组织及肿瘤新增生血管中高表达,并参与肿瘤增殖、侵袭、耐药等相关信号通路。
(10)瑞迪奥锝[99mTc]佩昔瑞特加肽药盒获批上市
4月2日,国家药监局(NMPA)官网显示,瑞迪奥的1类放射性创新药锝[99mTc]佩昔瑞特加肽注射液及制备该药品的注射用锝[99mTc]佩昔瑞特加肽药盒通过优先审评审批程序获批上市,用于可疑肺癌患者区域淋巴结转移的辅助检查。
该药物是国内药企在FIC靶点上推出的核医学放射诊断1类新药,也是全球第一个用于SPECT显像的广谱肿瘤显像剂。
1.4.2 本周全球TOP10积极/失败临床结果
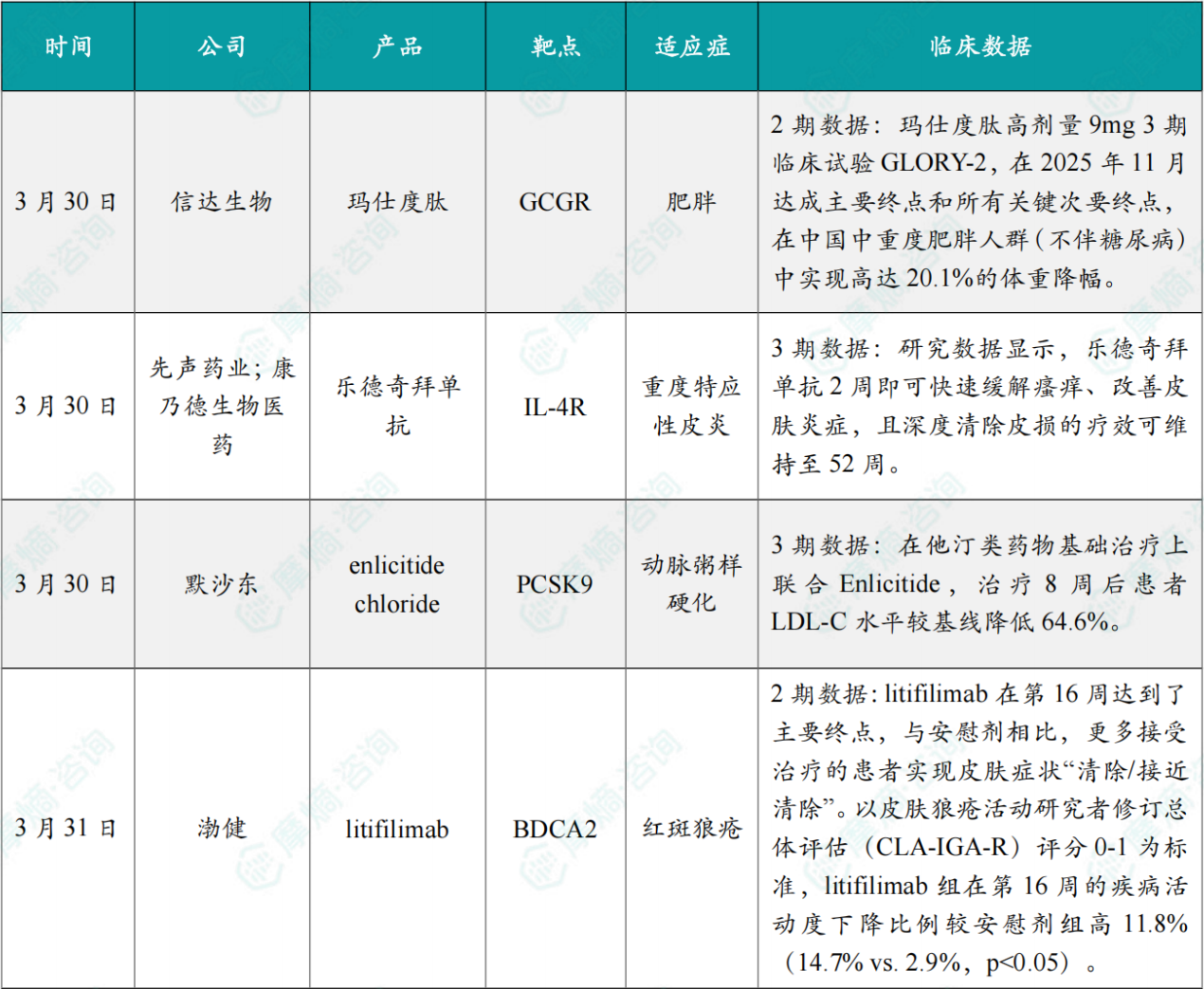

(1)信达生物减重新药玛仕度肽2期临床结果发表
3月30日,信达生物宣布:胰高血糖素(GCG)/胰高血糖素样肽-1(GLP-1)双受体激动剂玛仕度肽注射液,在中国肥胖受试者中开展的2期9mg剂量的临床研究结果近日在Cell子刊MED全文在线发表。
玛仕度肽高剂量9mg 3期临床试验GLORY-2,在2025年11月达成主要终点和所有关键次要终点,在中国中重度肥胖人群(不伴糖尿病)中实现高达20.1%的体重降幅。基于该研究,玛仕度肽注射液高剂量9mg用于成人中重度肥胖患者长期体重控制的上市申请已于2025年11月获中国国家药品监督管理局(NMPA)药品审评中心(CDE)受理。
(2)先声药业/康乃德公布IL-4Rα单抗Ⅲ期研究数据
3月30日,先声药业宣布,与康乃德生物医药合作的创新抗体药物乐德奇拜单抗针对成人、青少年中重度特应性皮炎患者的Ⅲ期临床研究入选第84届美国皮肤科学会年会最新突破性研究摘要(Late-Breaking Abstract, LBA)并进行口头报告。
研究数据显示,乐德奇拜单抗2周即可快速缓解瘙痒、改善皮肤炎症,且深度清除皮损的疗效可维持至52周。乐德奇拜单抗是靶向IL-4R的全人源单抗。临床前研究显示,其与受体的亲和力高于度普利尤单抗。2025年7月,乐德奇拜单抗的新药上市申请已获NMPA受理。
(3)默沙东口服PCSK9抑制剂III期临床成功
3月30日,默沙东公布了其口服PCSK9抑制剂Enlicitide(MK-0616)治疗高胆固醇血症的CORALreef AddOn III期详细数据。
CORALreef AddOn(NCT06450366)研究是一项多中心、随机、双盲临床试验,旨在评估Enlicitide(20mg,每日1次)对比依折麦布单药(10mg,每日1次)、贝派度酸单药(180mg,每日1次)、依折麦布联用贝派度酸,治疗有主要ASCVD事件病史或有主要ASCVD事件风险并接受他汀类药物治疗的高胆固醇血症患者的疗效和安全性。主要终点方面,试验结果显示,在他汀类药物基础治疗上联合Enlicitide,治疗8周后患者LDL-C水平较基线降低64.6%。与对照药物相比,Enlicitide的降脂优势显著。
(4)渤健公布其AMETHYST 2/3期研究(A部分)中2期试验的积极结果
3月31日,渤健公布其AMETHYST 2/3期研究(A部分)中2期试验的积极结果,该研究评估在研单抗litifilimab用于治疗皮肤红斑狼疮(CLE)患者的疗效与安全性。
AMETHYST研究A部分评估了该药物至第24周的疗效与安全性,结果显示在多个指标上均观察到皮肤疾病活动度的下降。这一结果与此前发表在《新英格兰医学杂志》的2期LILAC研究结果一致,两项研究结果也支持该疗法近期所获美国FDA授予的突破性疗法认定。
在AMETHYST研究的2期部分中,litifilimab在第16周达到了主要终点,与安慰剂相比,更多接受治疗的患者实现皮肤症状“清除/接近清除”。以皮肤狼疮活动研究者修订总体评估(CLA-IGA-R)评分0-1为标准,litifilimab组在第16周的疾病活动度下降比例较安慰剂组高11.8%(14.7% vs. 2.9%,p<0.05)。此外,治疗组在多个次要指标中也显示出持续改善:以红斑性疾病面积和严重程度指数活动度-50(CLASI-50,即较基线改善50%)为指标,litifilimab组在第4周即与安慰剂出现分离,并持续至第24周(40.8% vs. 21%);在CLASI-70指标上,第24周治疗组应答率为21.7%,高于安慰剂组的5.8%。同时,约六分之一接受litifilimab治疗的患者在第24周达到CLASI 0-3评分,即无或极轻疾病活动度。总体而言,该药物在AMETHYST研究A部分中耐受性良好,其安全性表现与既往研究(包括LILAC研究)一致。
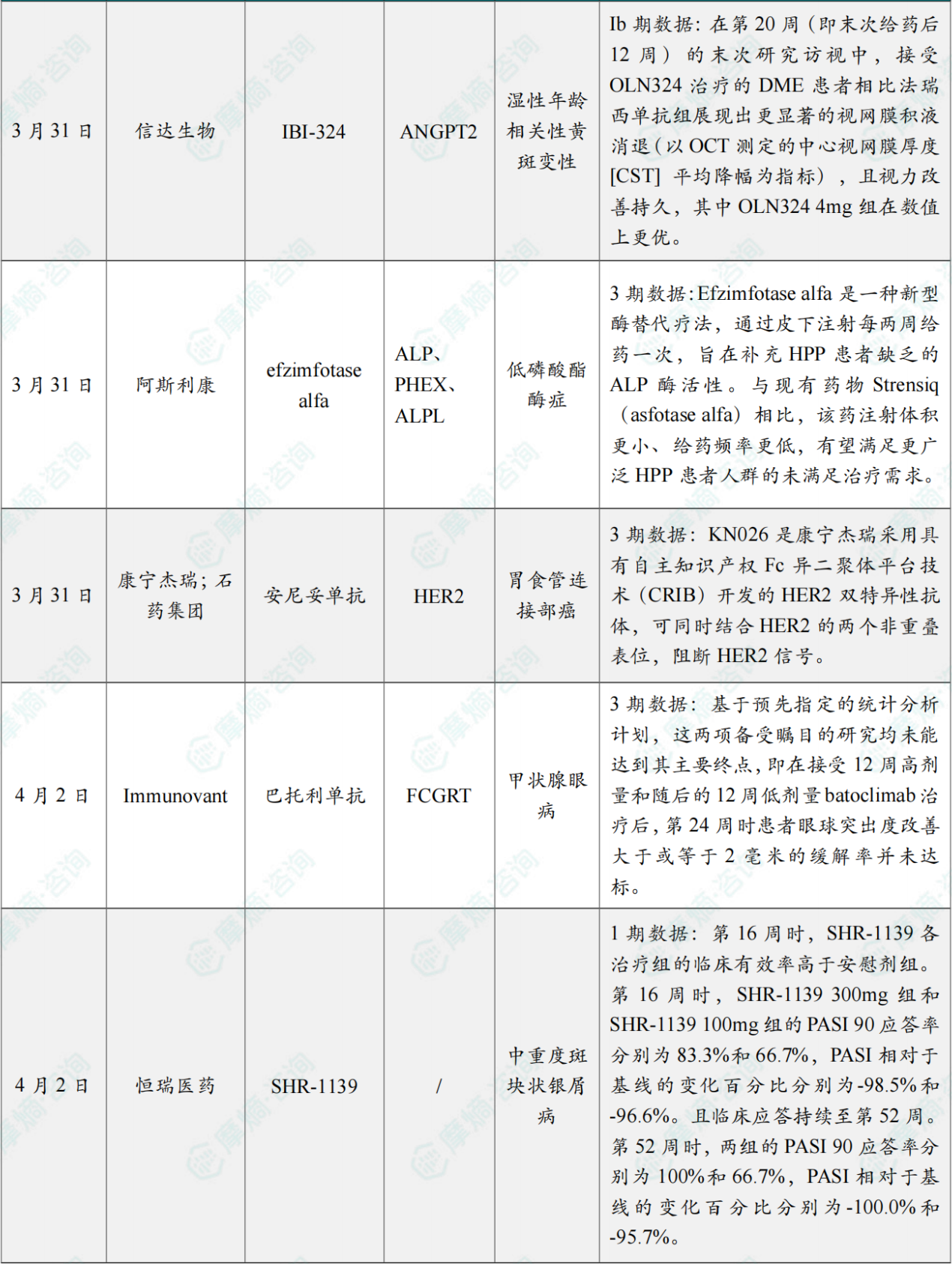
(5)信达生物眼科双抗临床Ib期结果公布
3月31日,信达生物宣布,其合作伙伴Ollin Biosciences公布了IBI324对比法瑞西单抗临床Ib期研究JADE的最终数据。
IBI324(Ollin研发代号OLN324)是一款更高效价、更高摩尔剂量的血管内皮生长因子(VEGF)/血管生成素-2(Ang2)双特异性抗体。
本次公布结果的一项随机、头对头研究,共持续20周,旨在对比了IBI324与法瑞西单抗在糖尿病性黄斑水肿(DME)或湿性(新生血管性)年龄相关性黄斑变性(wAMD)患者中的疗效与安全性。在第20周(即末次给药后12周)的末次研究访视中,接受OLN324治疗的DME患者相比法瑞西单抗组展现出更显著的视网膜积液消退(以OCT测定的中心视网膜厚度[CST]平均降幅为指标),且视力改善持久,其中OLN324 4mg组在数值上更优。
(6)阿斯利康新型酶替代疗法III期研究成功
3月31日,阿斯利康宣布酶替代疗法efzimfotase alfa(ALXN1850)治疗低磷酸酯酶症(HPP)患者的III期临床项目取得积极结果。
Efzimfotase alfa是一种新型酶替代疗法,通过皮下注射每两周给药一次,旨在补充HPP患者缺乏的ALP酶活性。与现有药物Strensiq(asfotase alfa)相比,该药注射体积更小、给药频率更低,有望满足更广泛HPP患者人群的未满足治疗需求。
该全球临床项目包括两项随机、安慰剂对照试验和一项随机、开放标签、阳性对照的儿科转换试验,共纳入196名患者,涵盖儿童、青少年和成人,包括儿童期发病或成人期发病HPP患者,分布于22个国家。这些数据将在即将举行的医学会议上展示,并与全球监管机构分享。
(7)康宁杰瑞/石药集团HER2双抗新辅助治疗乳腺癌III期研究成功
3月31日,康宁杰瑞和石药集团共同宣布KN026联合注射用多西他赛(白蛋白结合型)(HB1801)新辅助治疗HER2阳性乳腺癌的III期临床研究(KN026-004)达到主要终点,即总体病理完全缓解率(tpCR)的改善结果具有显著的统计学意义和临床意义。
KN026是康宁杰瑞采用具有自主知识产权Fc异二聚体平台技术(CRIB)开发的HER2双特异性抗体,可同时结合HER2的两个非重叠表位,阻断HER2信号。KN026的新药上市申请于2025年9月获NMPA受理,目前处于上市申请审评中。2021年8月,康宁杰瑞与石药集团旗下子公司津曼特生物达成授权合作,后者获得KN026在中国内地(不包括香港、澳门及台湾地区)关于乳腺癌及胃癌适应症的排他性开发与独占性商业化许可权。
(8)Immunovant宣布甲状腺眼病临床III期失败
4月2日,Immunovant宣布了评估batoclimab作为治疗活动性中重度甲状腺眼病(TED)成人患者的两项第3期(GO)临床研究的顶线结果。遗憾的是,基于预先指定的统计分析计划,这两项备受瞩目的研究均未能达到其主要终点,即在接受12周高剂量和随后的12周低剂量batoclimab治疗后,第24周时患者眼球突出度改善大于或等于2毫米的缓解率并未达标。尽管主要疗效终点未能如期实现,但该药物的安全性能依然保持稳定,安全性结果与以往的发现保持一致,并且在研究过程中没有发现任何新的安全信号。
(9)恒瑞医药公布双靶点新药治疗银屑病1期临床数据
4月2日,恒瑞医药宣布,在2026年美国皮肤病学会(AAD)年会上,该公司在研的双靶点IL-23p19和IL-36R的抗体新药SHR-1139用于中重度斑块状银屑病患者1期研究数据发布。
本研究入组的16例患者均完成第0周和第4周的共2次给药(SHR-1139 100mg组和SHR-1139 300mg组各6例、安慰剂组4例),各组的人口学和基线特征基本均衡,基线时银屑病面积与严重程度指数(PASI)评分分别为31.4、32.1、36.7,体表受累面积(BSA)分别为48.0%、52.3%、55.8%,静态医师全面评估(sPGA)>3分的患者比例分别为83.3%、66.7%、100%。
皮损清除效果:第16周时,SHR-1139各治疗组的临床有效率高于安慰剂组。第16周时,SHR-1139 300mg组和SHR-1139 100mg组的PASI 90应答率分别为83.3%和66.7%,PASI相对于基线的变化百分比分别为-98.5%和-96.6%。且临床应答持续至第52周。第52周时,两组的PASI 90应答率分别为100%和66.7%,PASI相对于基线的变化百分比分别为-100.0%和-95.7%。
(10)Enveda公司公布ENV-294的1b期临床试验的积极结果
4月6日,Enveda公司公布了其潜在“first-in-class”、每日一次口服在研疗法ENV-294,在中重度特应性皮炎(AD)患者中进行的1b期临床试验的积极结果。这项开放标签研究纳入了9名曾接受过系统性治疗的成人患者,所有患者均接受了为期28天的每日一次800 mg ENV-294口服给药,随后进行了14天的停药观察。
该研究显示出快速且深度的临床缓解,第42天时湿疹面积和严重程度指数(EASI)平均降低了85%,最早在第8天就观察到了疗效。所有患者(100%)均达到了EASI-50,78%达到EASI-75,56%达到EASI-90,并且在停药后仍有持续改善。在安全性方面,该药物表现出良好的耐受性,未发生严重不良事件,也没有患者因此停药。
同期事件:
1. 2026年第14周03.30-04.05国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第14周03.30-04.05国内仿制药/生物类似物申报/审批数据分析
3. 2026年第14周03.30-04.05国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.03.30-2026.04.05) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论