【2月全球在研新药】月报内容亮点
2月国内新药获批临床情况
- 2月共有145款新药获批临床(共计234个受理号),较上个月减少了27款;
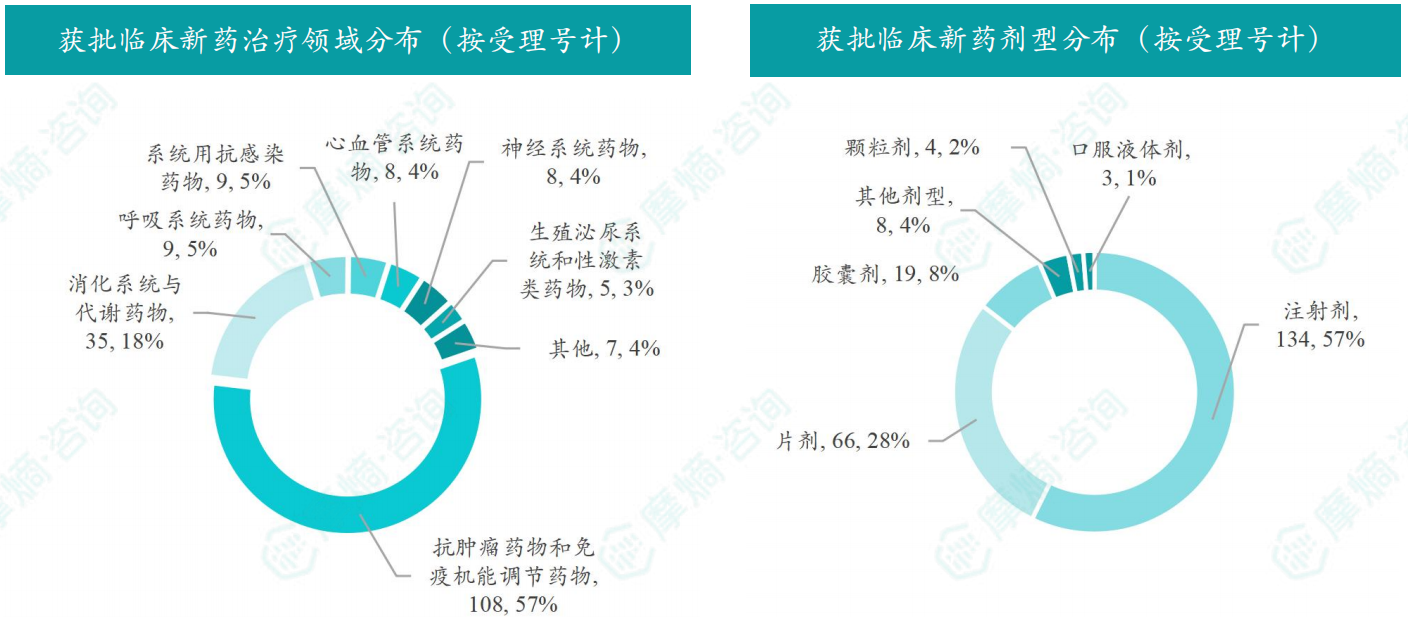
- 2月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有108个,占比57%;
- 2月获批剂型主要为注射剂与片剂,分别有134个,66个。
全球获孤儿药/突破性/快速通道资格认定品种盘点
- 2月共有41款药物获孤儿药/突破性/快速通道资格认定。
全球在研创新药积极/失败临床结果最新动态速递
- 勃林格殷格翰宣布肾病新药2期临床研究积极结果;
- 安进自身免疫单抗疗法2期临床积极结果公布;
- 恒瑞医药口服GLP-1R/GIPR激动剂II期研究成功;
- 阿斯利康口服GLP-1减肥药2b期临床达主要终点。
每月相关创新药最新政策速递、国内新药注册申报、全球获孤儿药/突破性/快速通道资格认定品种盘点、全球在研创新药积极/失败临床结果TOP20、全球创新药研发进展TOP20等,摩熵咨询团队基于真实可溯源的全球医药数据,将每月推出「全球在研新药月报」,以期帮助业内人士通盘把握每月全球范围内的新药开发情况,全面而深入的了解全球新药开发动态。
一、2月国内新药获批临床/上市情况
根据摩熵医药数据库统计,2026年2月共有145款新药获批临床(共计234个受理号),较上个月减少了27款,其中包括63款化药,77款生物制品,5款中药。

截图来源:摩熵咨询月报
本月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有108个,占比57%,消化系统与代谢药物获批数量也比较多,有35个。获批剂型主要为注射剂与片剂,分别有134个,66个。
截图来源:摩熵咨询月报
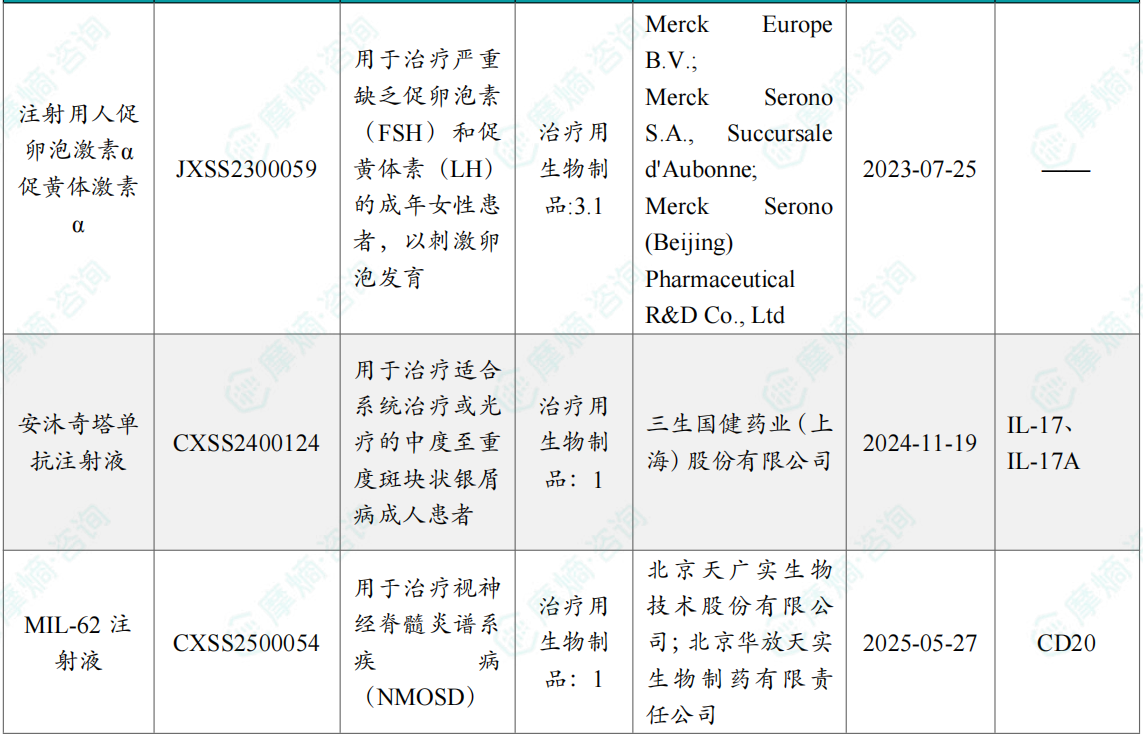
2026年2月,国内医药市场迎来了5款创新药物的获批上市,涉及三生国健药业的 安沐奇塔单抗注射液,该药是公司自主研发的1类生物创新药,提供两种灵活的用药选择,维持期患者可实现每4周或每8周一次的给药频率。安沐奇塔单抗 维持期每8周一次的给药方案仍可维持疗效强效应答,相较于现有同靶点抑制剂的治疗方案,给药间隔更长。在不影响疗效和安全性的基础上,安沐奇塔单抗 每8周一次的简化给药方案有望降低患者年度用药频率,有效降低长期治疗带来的时间成本与心理压力。
2026 年2月国内获批上市的新药

截图来源:摩熵咨询月报
二、全球获孤儿药/突破性/快速通道资格认定品种盘点
2月共有41款药物获孤儿药/突破性/快速通道资格认定。2026年2月9日赛诺菲宣布,美国FDA授予 rilzabrutinib(瑞扎布鲁替尼)突破性疗法认定,用于治疗温型自身免疫性溶血性贫血(wAIHA)。该药为口服可逆性BTK抑制剂,BTK在多种免疫细胞中表达,对免疫疾病进程和炎症通路作用关键,rilzabrutinib 有望通过调节免疫恢复平衡,治疗多种罕见免疫或炎症性疾病。据新闻稿公示,rilzabrutinib 是首个也是目前唯一获FDA此认定、用于治疗该罕见自身免疫性疾病的在研BTKi类药物。
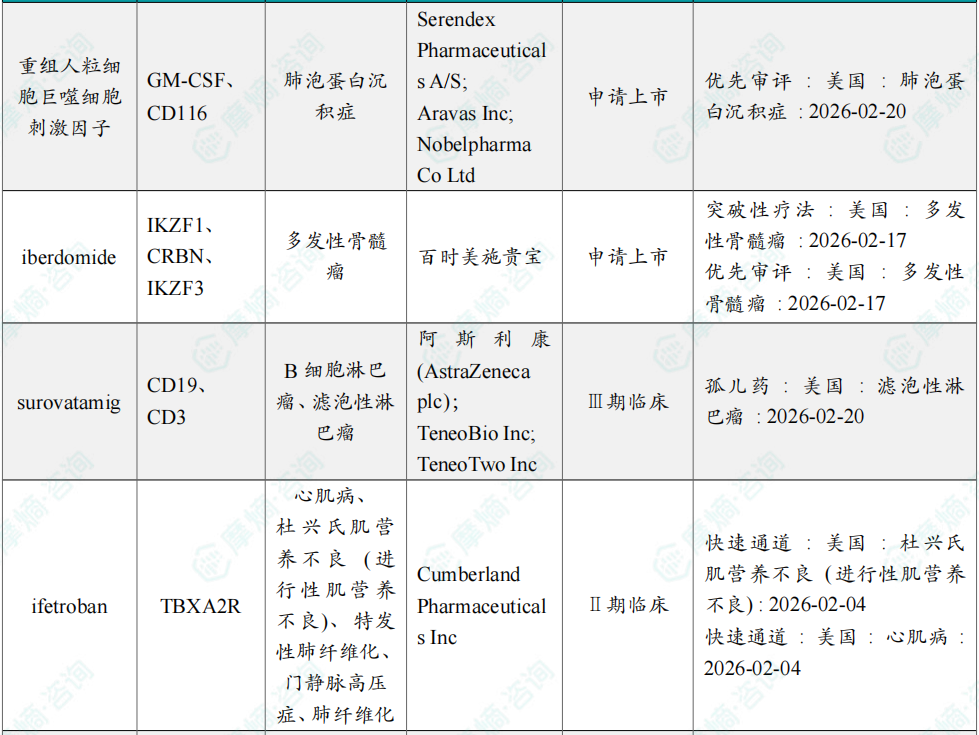
2月全球孤儿药/突破性/快速通道资格认定品种一览表(部分)



截图来源:摩熵咨询月报
三、全球在研创新药积极/失败临床结果TOP20
2月2日,赛诺菲公布了 Venglustat 的两项III期研究进展:针对III型戈谢病(GD3)的III期LEAP2MONO研究达到了主要终点,针对法布瑞氏症的III期PERIDOT研究未达到主要终点。基于这些进展,赛诺菲将率先推进 Venglustat 用于治疗GD3的申报上市工作。

查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
Venglustat 是一种新型的口服葡萄糖神经酰胺合成酶抑制剂(GCSi),能够强效抑制N端甲基转移酶1(NTMT1),并且能够穿越血脑屏障,有潜力通过抑制异常鞘糖脂(GSLs)积累及其生理病理后果,延缓相关疾病的进展。
在LEAP2MONO研究中,治疗第52周,Venglustat 组GD3患者的共济失调评估与评级量表(SARA)总分和重复性神经心理状态评估测验(RBANS)评分相较酶替代疗法(伊米苷酶)组显著改善(p=0.007),说明患者的神经症状显著改善。此外,在体现非神经系统结局的四个关键次要终点中,该研究达到了其中三个终点,即 Venglustat 组在脾脏容量、肝容量和血红蛋白水平方面显著改善。在该研究中,Venglustat 总体耐受性良好,与既往研究相比无新的安全性信号。Venglustat 组最常报告的不良事件包括头痛(14.3%)、恶心(14.3%)、脾脏肿大(14.3%)和腹泻(14.3%)。
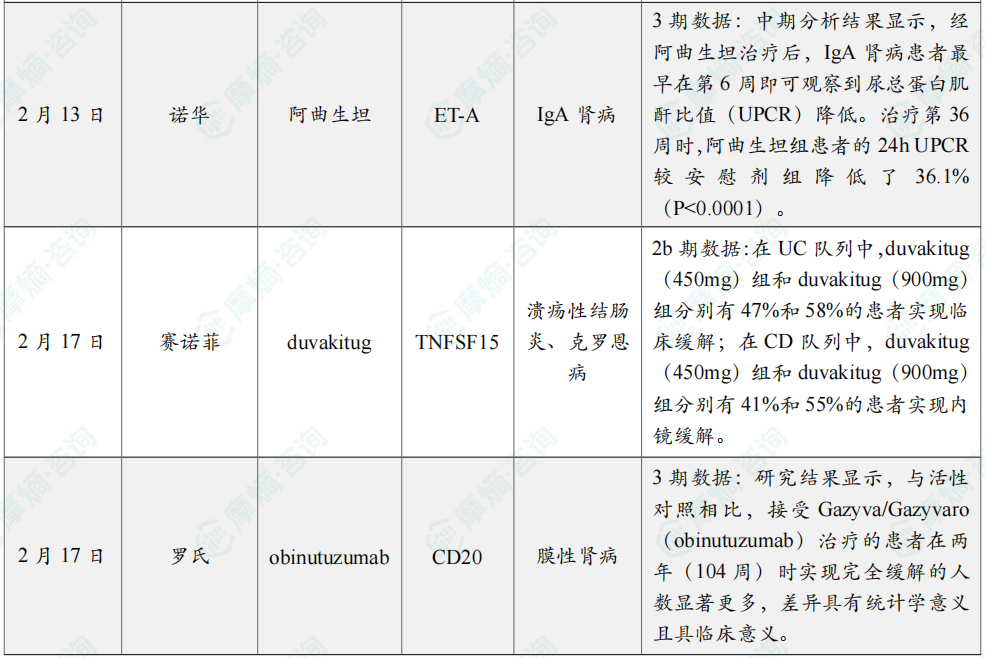
全球在研创新药积极/失败临床结果TOP20




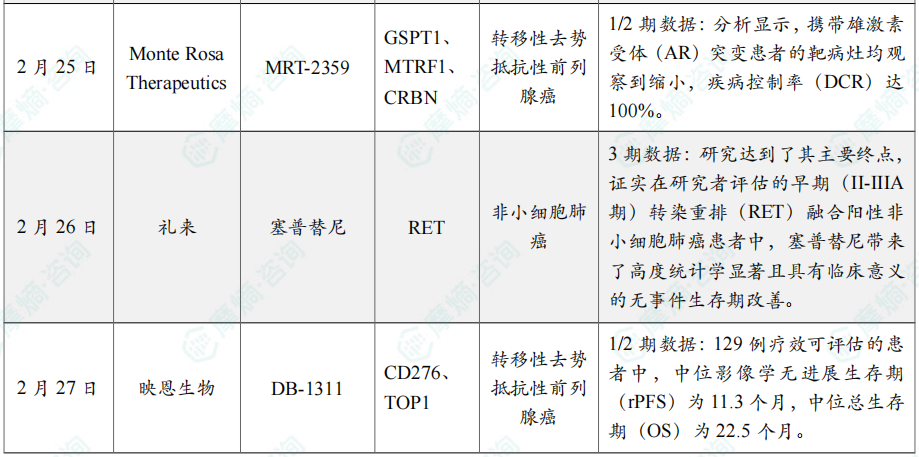
截图来源:摩熵咨询月报
四、全球创新药研发进展TOP20
2月3日,诺华公司(Novartis)宣布,其创新生物制剂 司库奇尤单抗 新适应症获得中国国家药品监督管理局(NMPA)批准,适用于治疗对非甾体类抗炎药(NSAID)应答不佳的活动性放射学阴性中轴型脊柱关节炎(nr-axSpA)成人患者(其客观征象表现为C反应蛋白[CRP]升高和/或磁共振成像[MRI]证据)。

查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
此次nr-axSpA适应症的获批,是继 司库奇尤单抗 成人和儿童中重度斑块状银屑病、强直性脊柱炎、银屑病关节炎和化脓性汗腺炎后,在中国获批的第六个适应症。中轴型脊柱关节炎(axSpA)是一种慢性炎症性疾病。axSpA疾病谱包括强直性脊柱炎(AS)和nr-axSpA。nr-axSpA患者的疾病负担与AS患者相似,且与AS呈现相同的症状,包括腰背疼痛、疲劳、晨僵和活动受限等。作为一种进展性疾病,若未得到及时干预,可能出现不可逆的结构损伤和功能障碍。研究表明,白介素(IL)-17A是参与axSpA、银屑病、银屑病关节炎病理机制的关键细胞因子。司库奇尤单抗作为一款IL-17A抑制剂,可特异性中和多种来源的IL-17A,抑制其促炎作用,缓解nr-axSpA的症状,持续改善病情,为患者带来长期获益。
全球创新药研发进展 TOP20



截图来源:摩熵咨询《2026年2月全球在研新药月报》
以上内容均来自摩熵咨询{ 2026年2月全球在研新药月报 },如需查看或下载完整版报告,可点击!
扩展阅读:
1. 2026年1月全球新药动态全览:172款新药获批临床!35款纳入特殊审评,涉及默沙东、礼来、诺华…
2. 2025年12月227款新药获批临床!42款纳入特殊审评,涉及安进、默沙东…
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论