
3月16日,阿斯利康宣布,其PD-L1单克隆抗体度伐利尤单抗(商品名:Imfinzi)联合FLOT化疗方案(含氟尿嘧啶、亚叶酸钙、奥沙利铂及多西他赛),已获得欧盟批准上市,用于治疗可切除的早期(II期)及局部晚期(IIIA-IIIB期)胃癌和胃食管交界处癌成人患者。该围手术期治疗方案包括术前(新辅助)及术后(辅助)各三个周期的度伐利尤单抗联合FLOT化疗,随后进行度伐利尤单抗单药维持治疗。
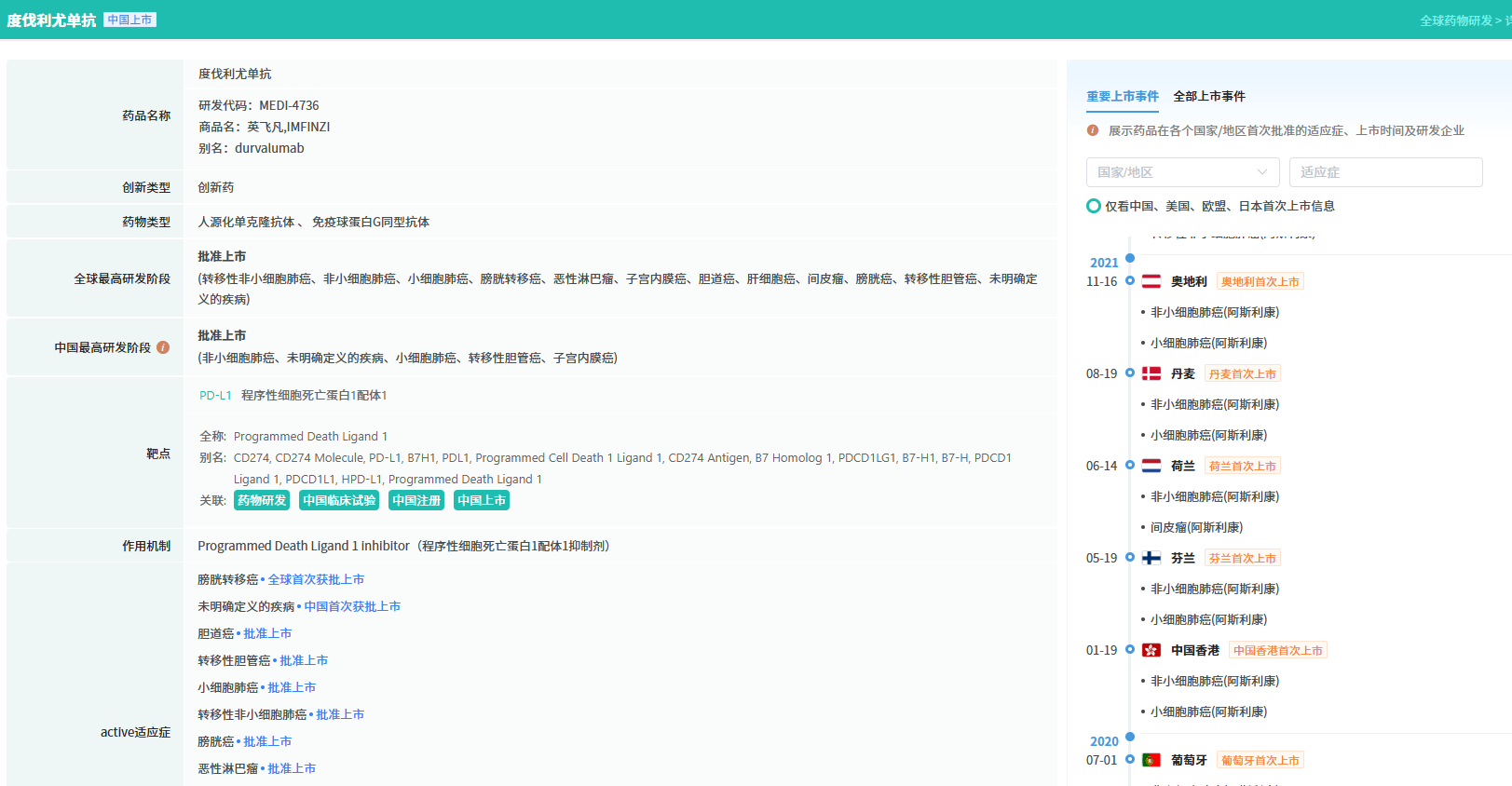
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
此次获批标志着度伐利尤单抗成为欧盟境内首个且目前唯一获批用于胃癌及胃食管癌围手术期治疗的免疫疗法,为此类患者群体提供了全新的治疗选择。
欧盟批准基于关键III期MATTERHORN研究阳性结果
本次批准主要基于全球多中心、随机、双盲、安慰剂对照的III期MATTERHORN临床试验的积极数据。该研究旨在评估在可切除的胃癌及胃食管交界处癌患者中,于FLOT化疗基础上联合度伐利尤单抗作为围手术期治疗的疗效与安全性。试验在全球20个国家的176个中心开展。
研究结果显示,与单纯FLOT化疗相比,度伐利尤单抗联合FLOT的围手术期治疗方案显著改善了患者的无事件生存期与总生存期:
无事件生存期:在预先计划的中期分析中,联合治疗方案将患者的疾病进展、复发或死亡风险显著降低了29%。联合治疗组的预估中位EFS尚未达到,而化疗对照组为32.8个月。联合治疗组患者的12个月和24个月无事件生存率分别为78.2%和67.4%,优于对照组的74.0%和58.5%。
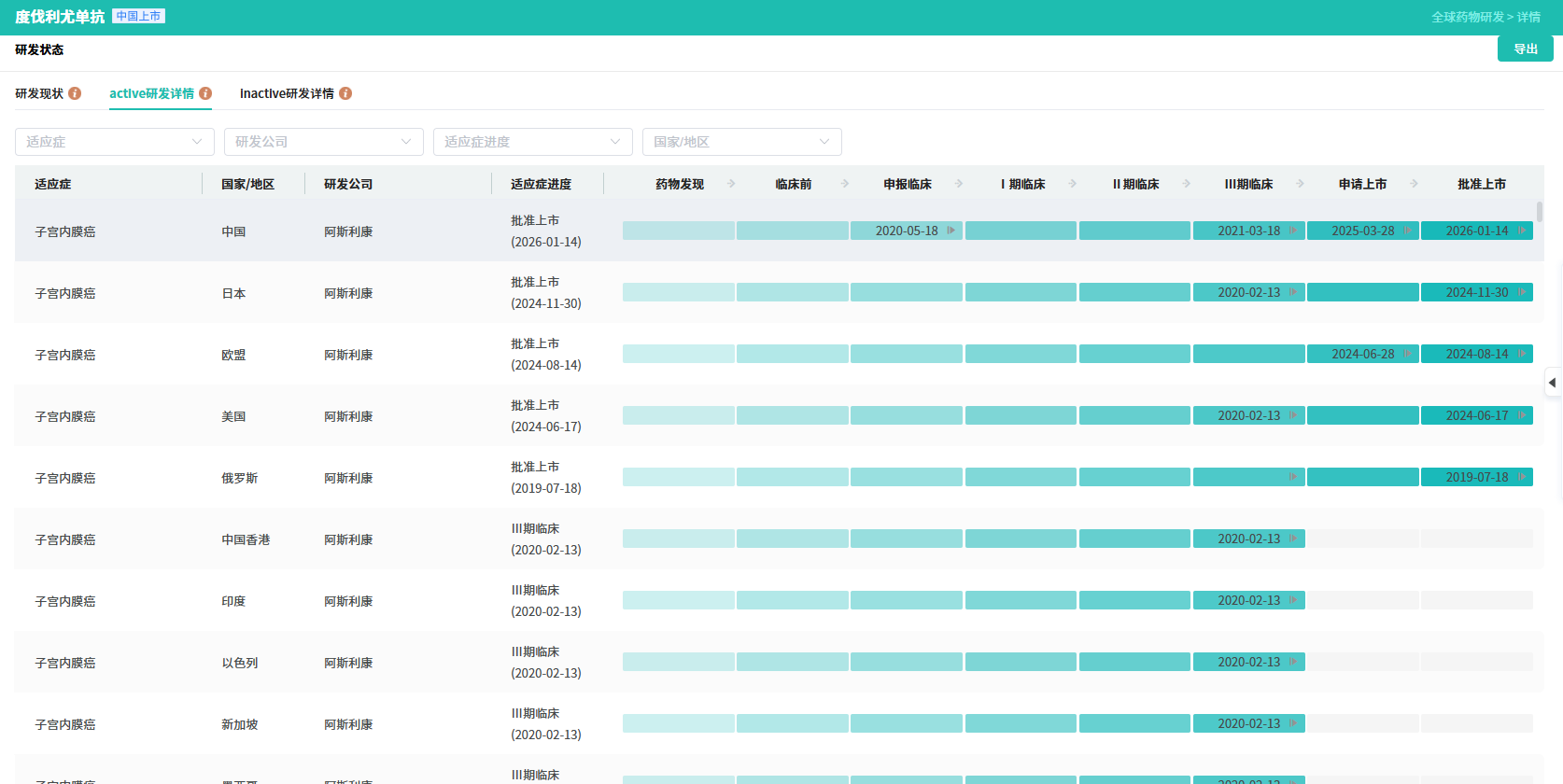
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
总生存期:在最终分析中,联合治疗方案表现出具有统计学显著性和临床意义的总体生存获益,与单纯化疗相比,患者的死亡风险降低了22%。联合治疗组患者的3年总生存率达到69%,高于对照组的62%。生存曲线显示,随着时间的推移,联合治疗组的生存获益优势持续扩大。该OS获益在不同PD-L1表达水平的患者中均被观察到。
安全性方面,度伐利尤单抗联合FLOT方案的安全性与各药物已知的安全性特征一致,未发现新的安全信号。两组中完成手术的患者比例相似,3级或以上不良事件的发生率亦相近。
基于MATTERHORN研究的卓越数据,度伐利尤单抗联合FLOT方案已于先前获得美国FDA批准用于相同适应症。
满足临床未竟需求,有望确立新标准
MATTERHORN试验的主要研究者Josep Tabernero博士表示:“尽管接受了以根治为目的的手术和化疗,可切除的胃癌患者仍面临较高的复发风险,长期生存率亟待提升。MATTERHORN研究证实,接受度伐利尤单抗围手术期治疗的患者,有近70%在三年后依然存活。此次欧盟批准为此类患者带来了首个能够显著延长生存期的围手术期免疫治疗方案,有望成为新的标准治疗。”
度伐利尤单抗是一种人源化PD-L1单克隆抗体,能够阻断肿瘤细胞利用PD-L1通路逃避免疫系统攻击。自2017年5月首次获批以来,全球已有超过41.4万名患者接受了该药物治疗。作为阿斯利康广泛研发计划的核心产品之一,度伐利尤单抗正在多项临床试验中探索其单药或与其它疗法联用,在非小细胞肺癌、膀胱癌、乳腺癌、卵巢癌及多种胃肠道癌症中的治疗潜力。
2025年,度伐利尤单抗全球销售额达60.63亿美元,同比增长28.54%。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论