
11月24日,据NMPA官网显示,阿斯利康的度伐利尤单抗注射液又一新适应症在国内获批上市。根据阿斯利康公开资料及该药本次国内申请的注册分类(2.2 类),本次获批的适应症为局部晚期非小细胞肺癌(NSCLC)。
截图来源:NMPA官网
度伐利尤单抗是一种人源化的 PD-L1 单克隆抗体,能够阻断 PD-L1与PD-1 和CD80的结合,从而阻断肿瘤免疫逃逸并恢复被抑制的免疫反应。本次新适应症的获批是基于 PACIFIC-5 临床研究结果。PACIFIC-5 是一项中国主导的 III 期随机、双盲、安慰剂对照、多中心临床试验,旨在评估度伐利尤单抗作为巩固治疗在局部晚期、不可切除的非小细胞肺癌(III 期 NSCLC)患者中的疗效。
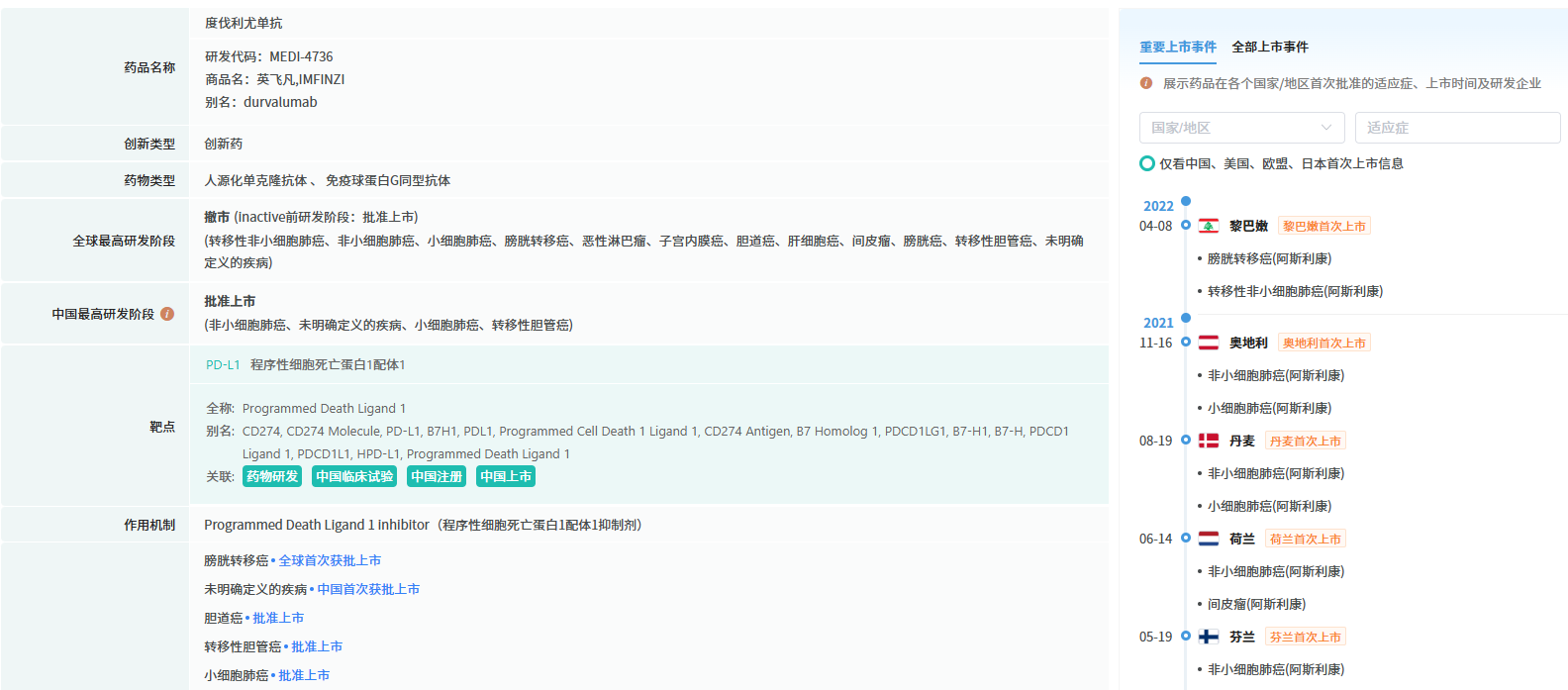
截图来源:摩熵医药数据库-全球药物研发数据库
PACIFIC-5 试验中近 60% 的患者来自中国,其余 40% 来自土耳其、韩国、俄罗斯及其它国家。主要终点是由盲态独立中心审查(BICR)评估的 PFS,关键次要终点是 OS。
2024年12月公布的PACIFIC-5 III期临床试验显示:与安慰剂相比,度伐利尤单抗使患者疾病进展或死亡风险预估降25%(PFS的HR 0.75,95%CI 0.578 - 0.986,p=0.038),亚组分析表明同步或序贯放化疗后接受该药治疗的患者均一致获益。首次中期分析中,关键次要终点OS显示,度伐利尤单抗组患者死亡风险有下降趋势(HR 0.87,95%CI 0.656 - 1.166,p=0.346)。且该药组至少治疗一年(49.1%)和两年(29.9%)的患者比例均高于安慰剂组(33.6%、20.9%)。
参考来源:
[1] NMPA官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 阿斯利康双特异性抗体AZD2936亮相:PD-1与TIGIT双管齐下,探索抗癌新路径
2. RXFP1受体成心血管新药研发焦点,阿斯利康AZD5462片获批临床
3. 阿斯利康/安进全球唯一TSLP单抗特泽利尤单抗在华上市申请获受理,或成2026年重磅新药!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论