
在年销超15亿元且持续增长的抗痛风药市场,天地恒一制药发起关键布局。
2025年12月30日,天地恒一制药提交的多替诺雷片4类仿制药上市申请获CDE受理,成为首个申报该品种仿制的企业。这款去年12月刚在国内获批进口的“痛风新星”,上市仅一年就迎来了首仿争夺战。
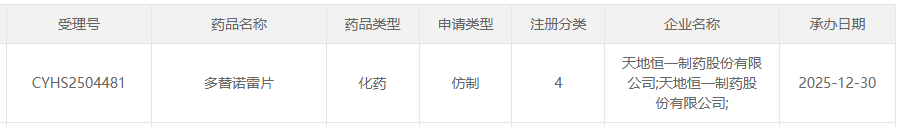
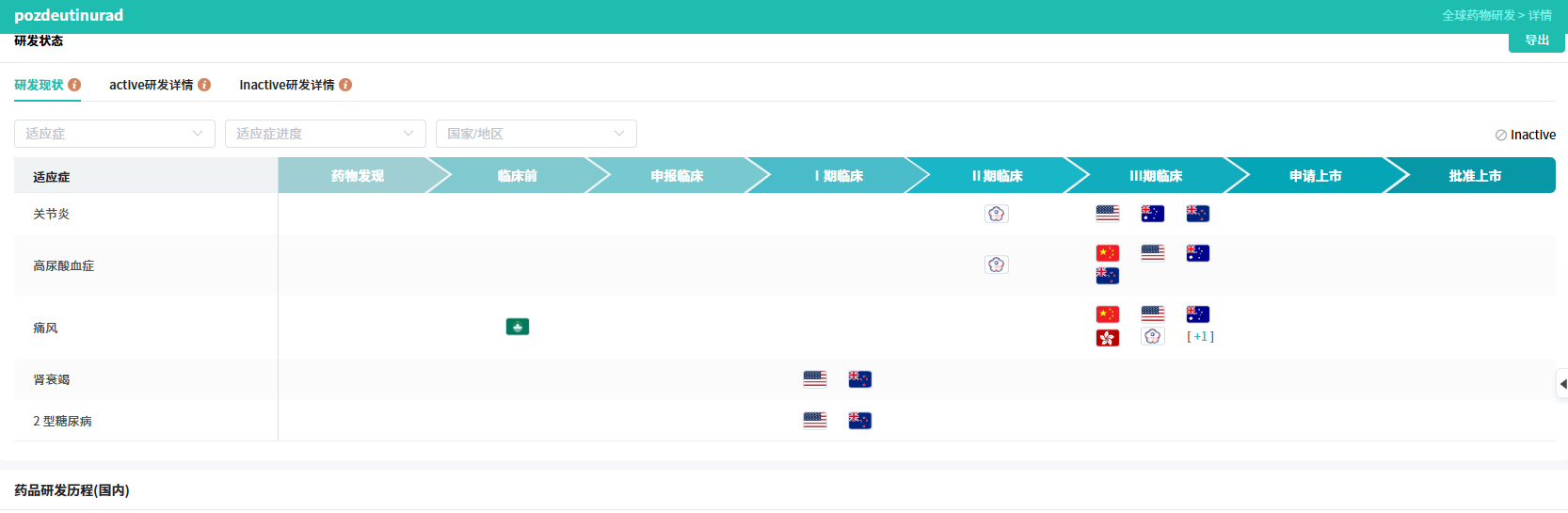
截图来源:CDE官网
15亿抗痛风市场:首仿争夺战打响
多替诺雷由日本富士药品原研,属于高选择性尿酸转运蛋白(URAT1)抑制剂,用于治疗痛风与高尿酸血症。该药于2020年1月在日本率先获批,去年12月在中国获批进口,由卫材独家开发销售,预计2025年7月在中国正式上市。仅隔一年,国内首仿竞争者便纷纷涌现。据摩熵医药数据库显示,2024年抗痛风药全终端医院市场销售额超15亿元,同比增长8.98%,2025年上半年销售额已超7亿元。
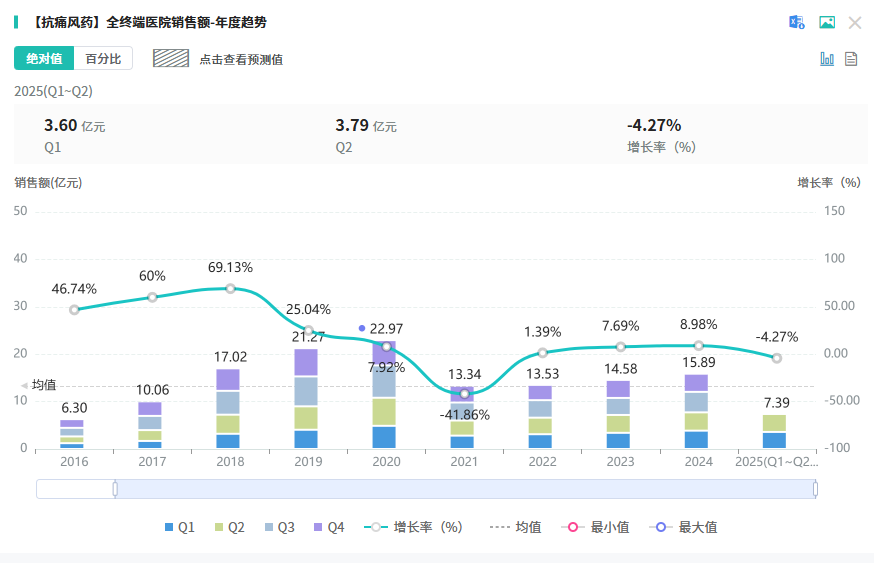
查数据,找摩熵!图源:摩熵医药全终端医院销售数据库
在企业竞争格局上,上海复星高科技集团以29.19%的市场份额位居榜首,杭州朱养心药业以17.61%位列第二。若天地恒一制药的多替诺雷片顺利获批,市场格局有望重塑。
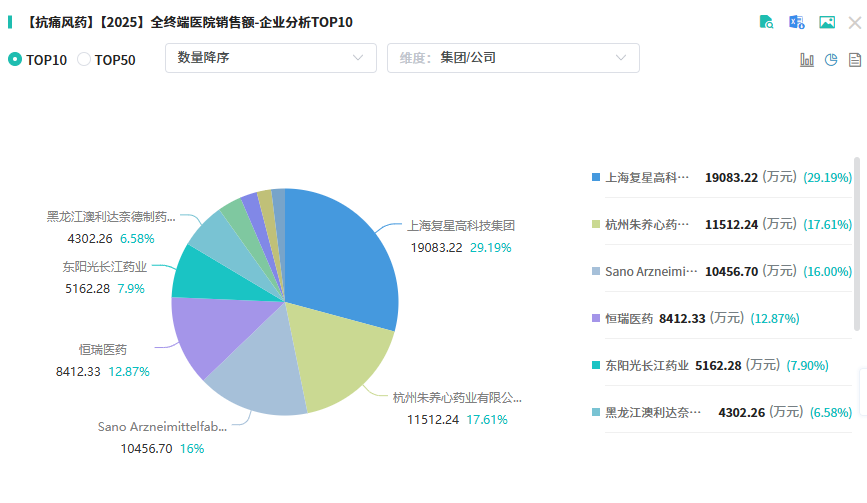
查数据,找摩熵!图源:摩熵医药全终端医院销售数据库
在仿制药领域,除天地恒一制药外,山东朗诺制药也提交了多替诺雷片仿制药上市申请。不过,天地恒一制药若能顺利获批,极有可能斩获首仿。
与此同时,四川国为制药、山西泽辰医药、杭州和康药业等9家药企针对多替诺雷片开展的生物等效性(BE)试验正稳步推进,预计不久后便会提交上市申请,首仿之争愈发激烈。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论