
3月12日,华东医药发布公告称,其全资子公司杭州中美华东制药有限公司(简称“中美华东”)收到美国食品药品监督管理局(FDA)通知,自主研发的注射用HDM2024临床试验申请(IND)正式获批,可在美国开展I期临床试验,适应症为晚期实体瘤。这是华东医药肿瘤创新药管线在国际舞台上的又一关键进展,也是公司全球化研发战略的重要落子。

截图来源:企业公告
据摩熵医药数据库显示,注射用HDM2024是中美华东拥有全球知识产权的1类生物新药,属于靶向EGFR/HER1与人表皮受体3(HER3)的新型双特异性抗体药物偶联物(Bs-ADC)。其结构由三部分组成:可同时识别EGFR/HER1与HER3的双抗分子、可裂解连接子,以及DNA拓扑异构酶1抑制剂类细胞毒性分子。作用机制上,HDM2024既能同步阻断EGFR/HER3信号通路,抑制肿瘤细胞增殖,又能通过连接子精准释放毒素载荷,直击肿瘤组织实现高效杀伤。临床前研究显示,在不同靶点表达水平的多种实体瘤模型中,HDM2024均表现出显著的抗肿瘤活性,且成药性与安全性良好,为其进入临床提供了坚实数据支持。
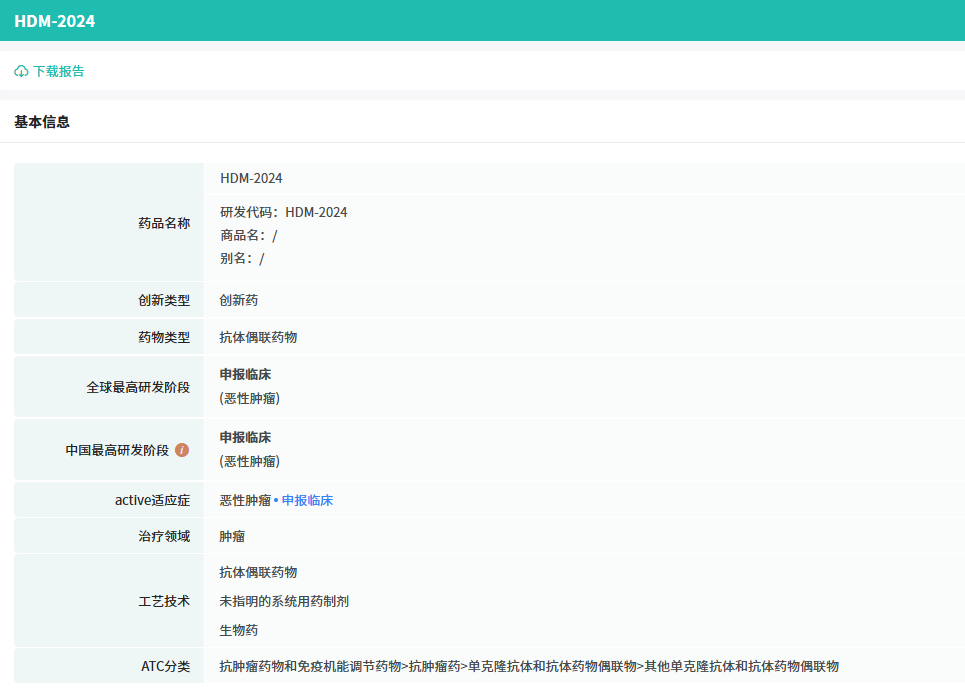
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
从研发进程看,中美华东推进迅速:2026年2月向美国FDA递交IND申请,仅月余即获准启动临床;国内布局亦同步展开——2026年1月已向国家药监局药品审评中心(CDE)提交同适应症的临床试验申请,目前处于审评阶段。这种“中美双报”策略,体现了公司对HDM2024全球化商业前景的信心。
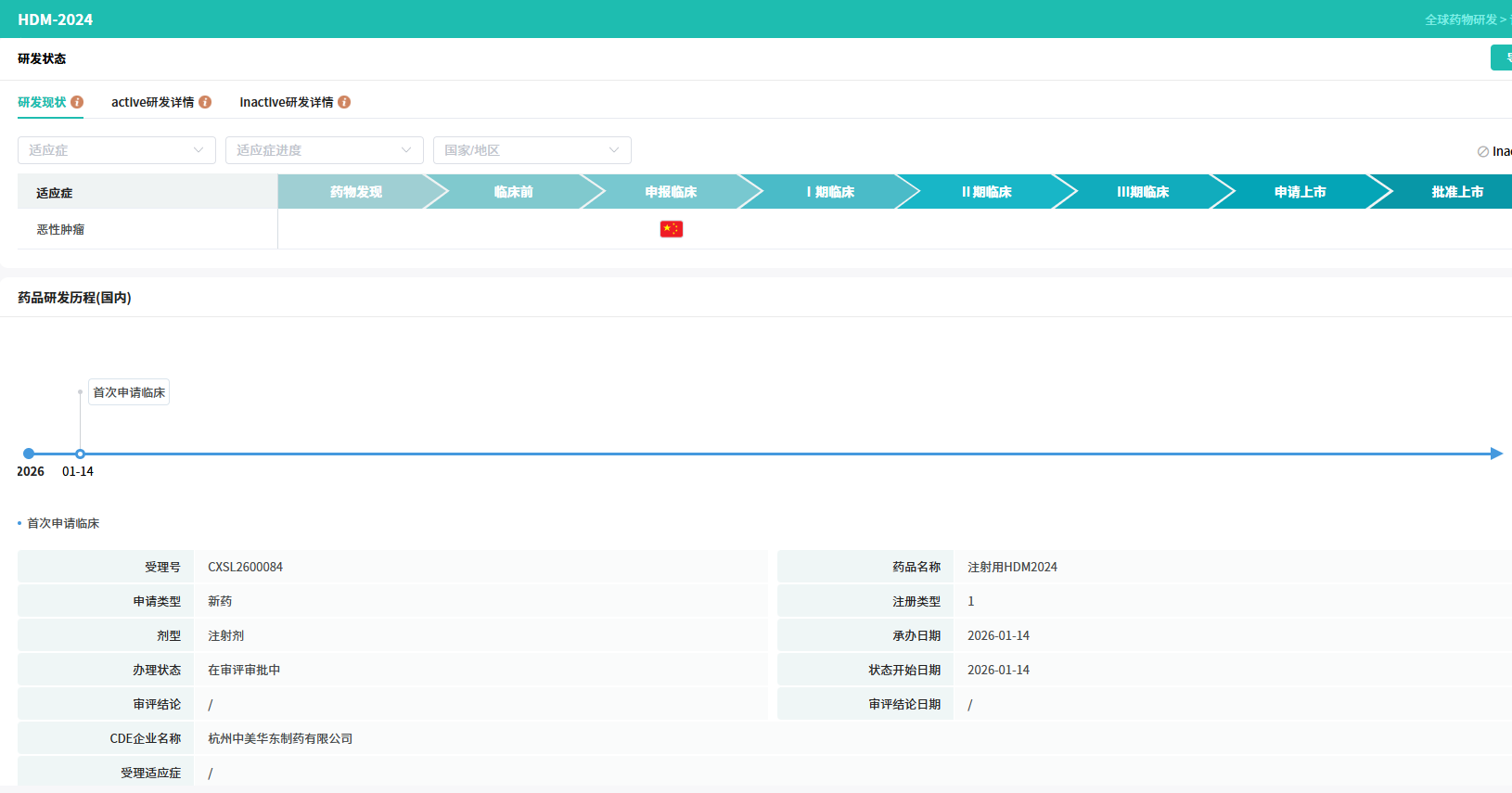
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
作为华东医药肿瘤管线的核心候选药物之一,HDM2024的美国临床获批,不仅意味着其研发进入国际多中心试验阶段,也进一步夯实了公司在ADC(抗体药物偶联物)这一前沿技术领域的全球竞争力。
截至目前,公司已搭建起超30项肿瘤创新药管线,覆盖小分子、单克隆抗体、多特异性抗体、ADC、CAR-T等多种药物形式,技术平台多元且迭代迅速。同时,通过投资、控股、孵化国内多家掌握先进生物技术的公司,并与德国Heidelberg Pharma达成产品与股权合作,引进其ATAC(抗体-鹅膏蕈碱偶联物)专有技术平台,华东医药逐步构建起独具特色的ADC全球研发生态圈,为后续管线拓展与国际化合作奠定坚实基础。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论