
12月25日,第一三共与阿斯利康联合宣布,其重磅抗体偶联药物(ADC)德曲妥珠单抗(商品名:优赫得®/Enhertu)在中国获批一项新适应症,用于治疗HR阳性、HER2低表达(IHC 1+或IHC 2+/ISH-)或HER2超低表达(IHC 0,伴膜染色)的乳腺癌成人患者。这是该药在国内获批的第五项适应症,标志着其在乳腺癌治疗领域的应用边界进一步拓展。

截图来源:企业官微
德曲妥珠单抗是第一三共采用其独有的DXd ADC技术平台开发的一款靶向HER2的创新型疗法。
2019年3月,第一三共与阿斯利康达成总额高达69亿美元的全球合作,共同推进该产品的开发与商业化。此次新适应症的获批,使其在乳腺癌这一核心战场,成功从后线向前线推进,并首次覆盖了“HER2超低表达”这一新的患者群体。
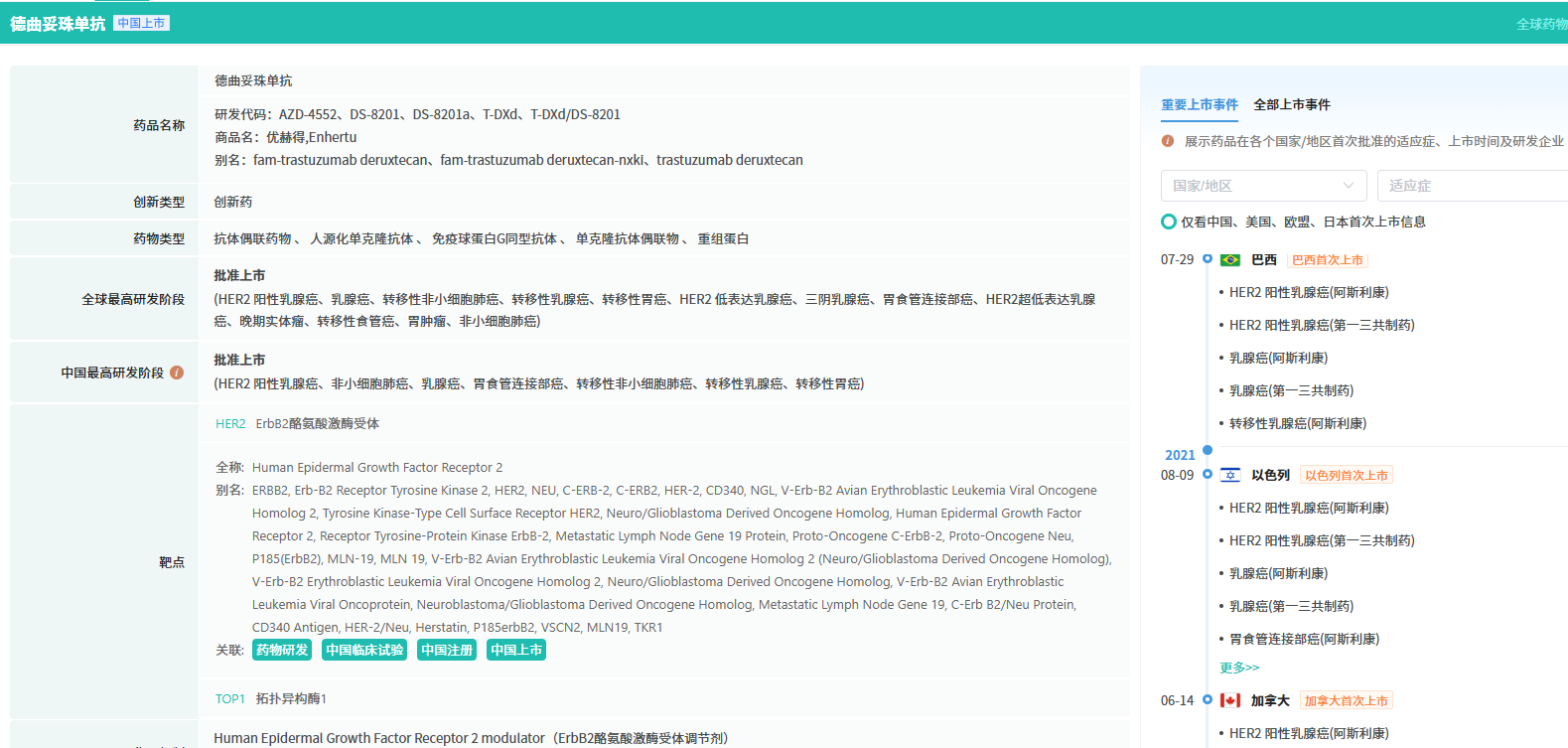
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
本次获批主要基于全球多中心III期临床试验DESTINY-Breast06的积极结果。该研究旨在比较德曲妥珠单抗与研究者选择的化疗,在HR阳性、HER2低表达或超低表达的晚期/转移性乳腺癌患者中的疗效与安全性。
德曲妥珠单抗研发详情
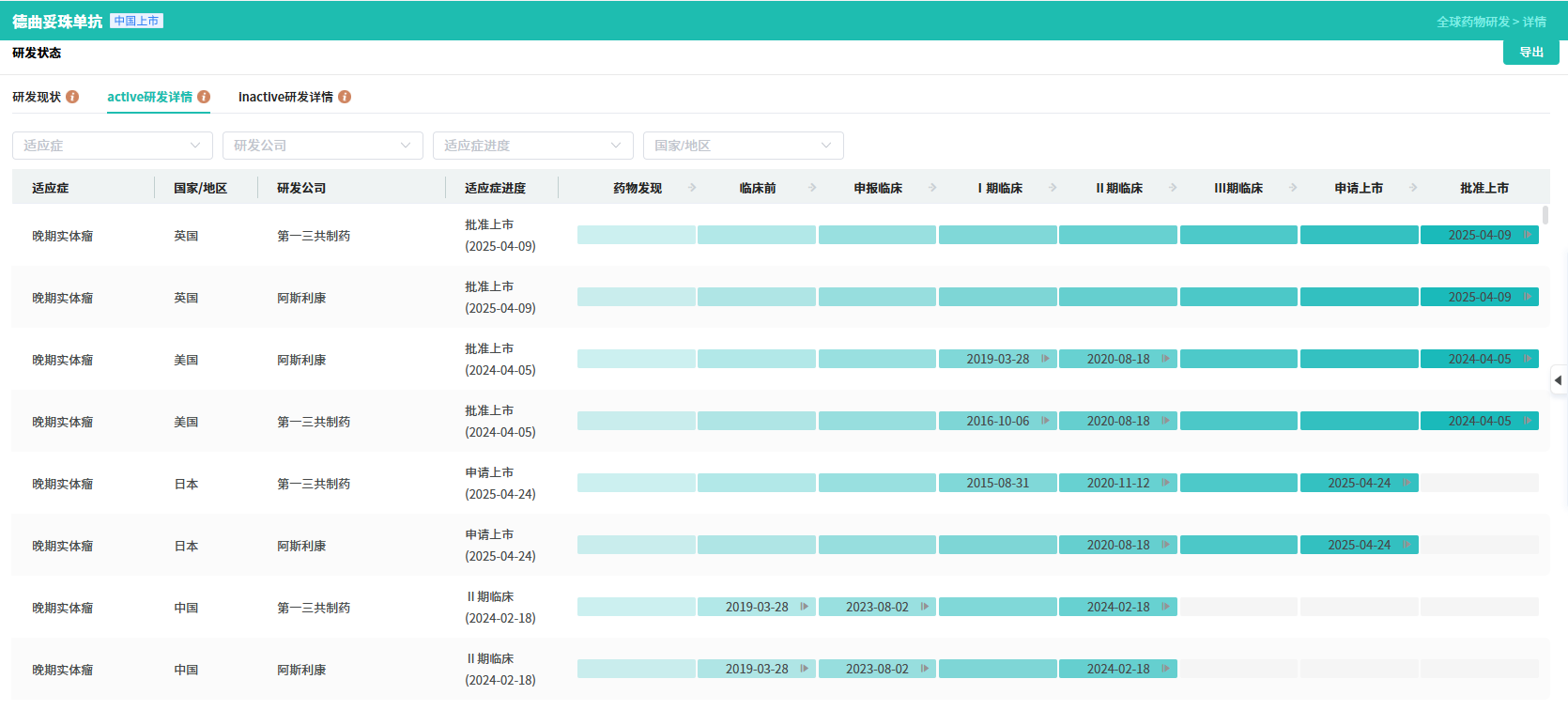
查数据,找摩熵!图源:摩熵医药全球药物研发数据库
研究数据显示出德曲妥珠单抗在多类人群中具有显著疗效优势。在HER2低表达患者中,与化疗相比,其可将疾病进展或死亡风险降低38%,中位无进展生存期(mPFS)达13.2个月,客观缓解率(ORR)为56.5%,缓解持续时间为14.1个月,各指标均显著优于对照组。在HER2超低表达人群中,其客观缓解率达61.8%,中位PFS为13.2个月,也显示出良好的治疗潜力。
至此,德曲妥珠单抗在国内已获批五项适应症,覆盖HER2阳性晚期乳腺癌、HER2低表达晚期乳腺癌、HER2阳性晚期胃癌/胃食管结合部腺癌、HER2突变非小细胞肺癌,以及本次新增的HR阳性、HER2低/超低表达乳腺癌,构建起较为完整的跨癌种治疗矩阵。
德曲妥珠单抗国内药品研发历程

查数据,找摩熵!图源:摩熵医药全球药物研发数据库
德曲妥珠单抗已成为全球ADC领域的领军产品,商业化表现极为亮眼。2024年全球销售额突破34亿美元。2025年前三季度销售额已近36亿美元,同比增长高达31%,显示出强劲的增长势头。
第一三共与阿斯利康仍在持续拓展该药的临床边界,其相关研究已8次登顶顶级医学期刊《新英格兰医学杂志》。目前,该药在国内尚有多个新适应症申报上市,随着适应症的不断拓展,其市场潜力有望进一步释放。
值得注意的是,在第一三共与阿斯利康的肿瘤管线中,另一款靶向TROP2的ADC药物德达博妥单抗也已在中、美、欧、日等多地获批用于HR阳性、HER2阴性乳腺癌的治疗。公司曾指出,德曲妥珠单抗与德达博妥单抗这两款ADC药物有望覆盖约90% 的转移性乳腺癌患者,形成了强大的协同治疗布局,正在重塑晚期乳腺癌的治疗格局。
参考来源:
[1] 企业官微
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 阿斯利康「替格瑞洛分散片」获批进口,莱美药业「艾司奥美拉唑钠」有望迎来首家过评...
2. 阿斯利康奥希替尼联合化疗获FDA批准!业绩最强的小分子肿瘤药物
3. 阿斯利康BTK抑制剂「阿可替尼」新适应症在中国申报上市!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论