
5月12日,CDE官网公示,辉瑞旗下1类新药PF-08653944注射液获得临床试验默示许可。摩熵医药全球药物研发数据库显示,这是 PF-08653944 首次在国内获批临床。
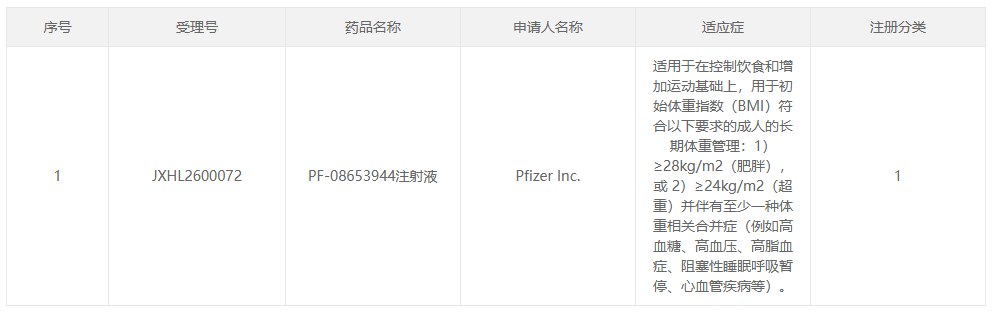
截图来源:CDE官网
一、百亿收购布局!超长效GLP-1具备灵活给药差异化优势
PF-08653944(MET-097i)由Metsera公司研发,是一款全偏向性超长效GLP-1受体激动剂。药物设计支持灵活给药方案,既可作为每周一次单药疗法,也可优化为每月一次给药,同时具备与其他肽类药物联合用药的开发潜力。2025年11月,辉瑞以最高100亿美元总交易额收购Metsera,将这款长效减重管线收入囊中。
据摩熵医药数据库显示,该药在2026年3月4日首次申请临床,5月12日首次批准临床。
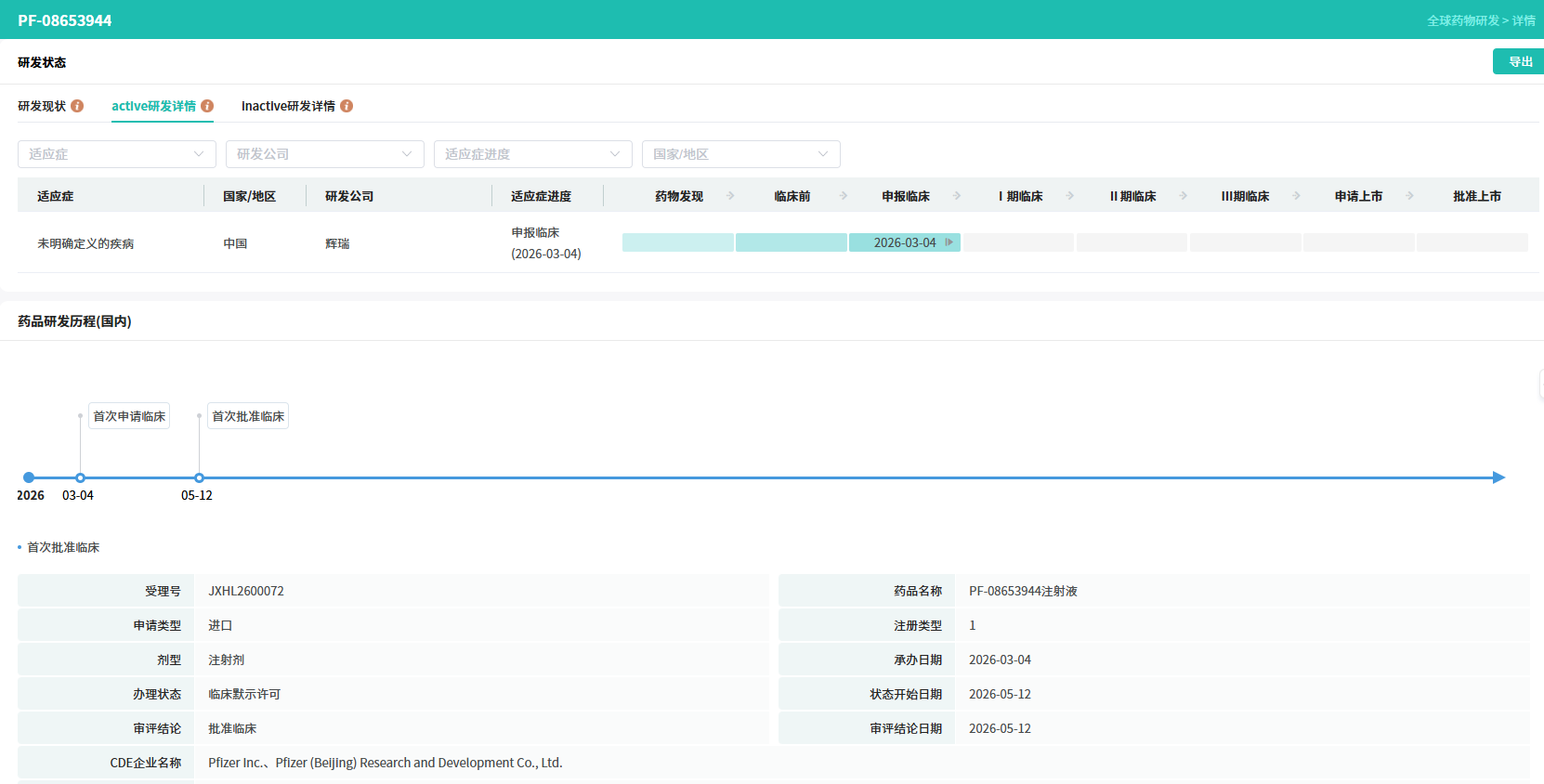
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
本次获批临床的适应症为体重管理,在饮食控制与运动干预的基础上,用于两类成人人群的长期治疗:
一是BMI≥28 kg/m²的肥胖人群;
二是BMI≥24 kg/m²的超重人群,且合并高血糖、高血压、高脂血症、阻塞性睡眠呼吸暂停、心血管疾病等至少一项体重相关合并症。
截至目前,辉瑞已推进PF-08653944针对肥胖、超重合并2型糖尿病人群的III期临床试验,全球化临床布局稳步推进。
二、临床数据亮眼!月度给药实现强效持续减重
2026年2月,辉瑞公布了该药物IIb期VESPER-3研究的积极顶线数据,验证了月度给药方案的减重价值。该研究为为期64周的随机、双盲、安慰剂对照试验,纳入肥胖或超重、无2型糖尿病的受试者,主要评估从每周给药逐步递增过渡至每月维持给药的安全性与有效性。
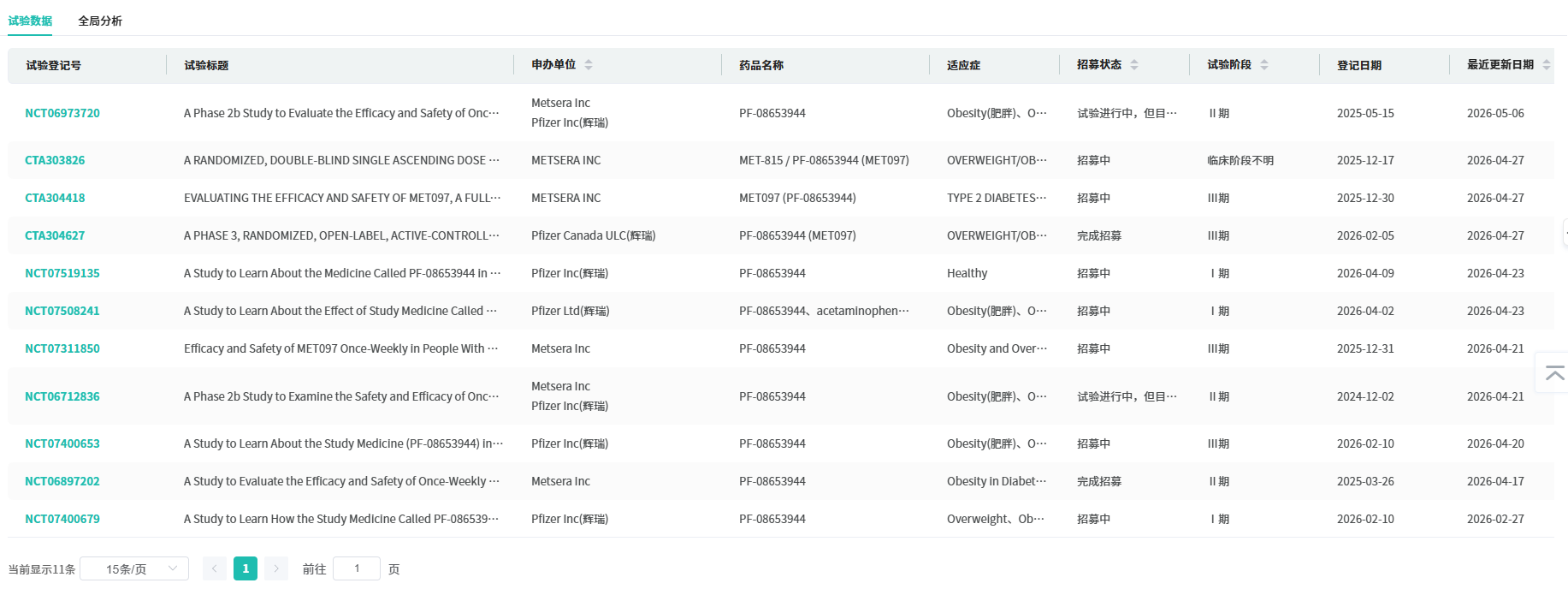
查数据,找摩熵!图源:摩熵医药-全球临床试验数据库
试验共设置四个剂量递增方案组与安慰剂组,各组样本量基本均衡。数据显示,在28周观测节点,适配III期临床的低剂量、中剂量月度维持方案,分别实现10%、12.3%的安慰剂校正体重下降。同时,受试者体重仍保持持续下降趋势,未出现减重平台期,预示64周长期治疗有望获得更优减重效果。
28周随访结果显示,PF-08653944整体耐受性良好,安全特征与现有GLP-1受体激动剂品类一致。试验中出现的胃肠道不良反应以轻、中度为主,各剂量组均未出现重度恶心、呕吐、腹泻等严重胃肠道事件。
整体停药事件发生率可控,每周给药阶段与月度维持阶段各出现5例因不良事件停药案例,安慰剂组无停药情况,整体安全风险符合预期。
三、小结
作为辉瑞重金布局的长效GLP-1管线,PF-08653944凭借周/月灵活给药、长效减重、安全性可控的特点,进一步丰富了肥胖与超重代谢疾病的治疗选择。此次国内临床获批,标志着这款差异化超长效减重疗法正式落地国内临床开发,后续III期数据将持续验证其长期减重疗效与安全性,有望为国内体重管理患者提供更便捷的长效治疗方案。
参考来源:
[1] CDE官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 辉瑞:CGRP拮抗剂硫酸瑞美吉泮口崩片新适应症上市申请获受理,偏头痛治疗“双轮驱动”加速
2. 辉瑞全球首创三抗Tilrekimig临床数据亮眼,中重度特应性皮炎治疗迎来长效强效新选择!
3. 先为达生物与辉瑞达成战略合作:押注新一代偏向型GLP-1受体激动剂埃诺格鲁肽,重塑代谢疾病市场格局
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论