
2026年5月7日,人福医药捷报频传。公司公告显示,控股子公司宜昌人福药业自主研发的化药1类新药RFUS-188注射液获国家药监局核准签发的《药物临床试验批准通知书》,用于急性疼痛治疗的临床试验。同时,宜昌人福药业美国公司申报的产品注射用醋酸西曲瑞克获美国FDA上市批准(ANDA)。

截图来源:企业公告
一、宜昌人福药业1类新药,RFUS-188注射液获批临床
RFUS-188为宜昌人福自主开发的新分子实体,临床上拟用于急性疼痛的治疗。该项目靶向外周κ阿片受体(KOR),不透过血脑屏障,仅在外周组织发挥镇痛作用,避免中枢阿片受体激活带来的成瘾、呼吸抑制、镇静、恶心呕吐等传统阿片类药物副作用。据摩熵医药数据库显示,该新药的临床申请于2026年2月获得承办,并于同年4月首次获得临床试验默示许可。截至目前,宜昌人福在该项目上的累计研发投入约2,500万元人民币。
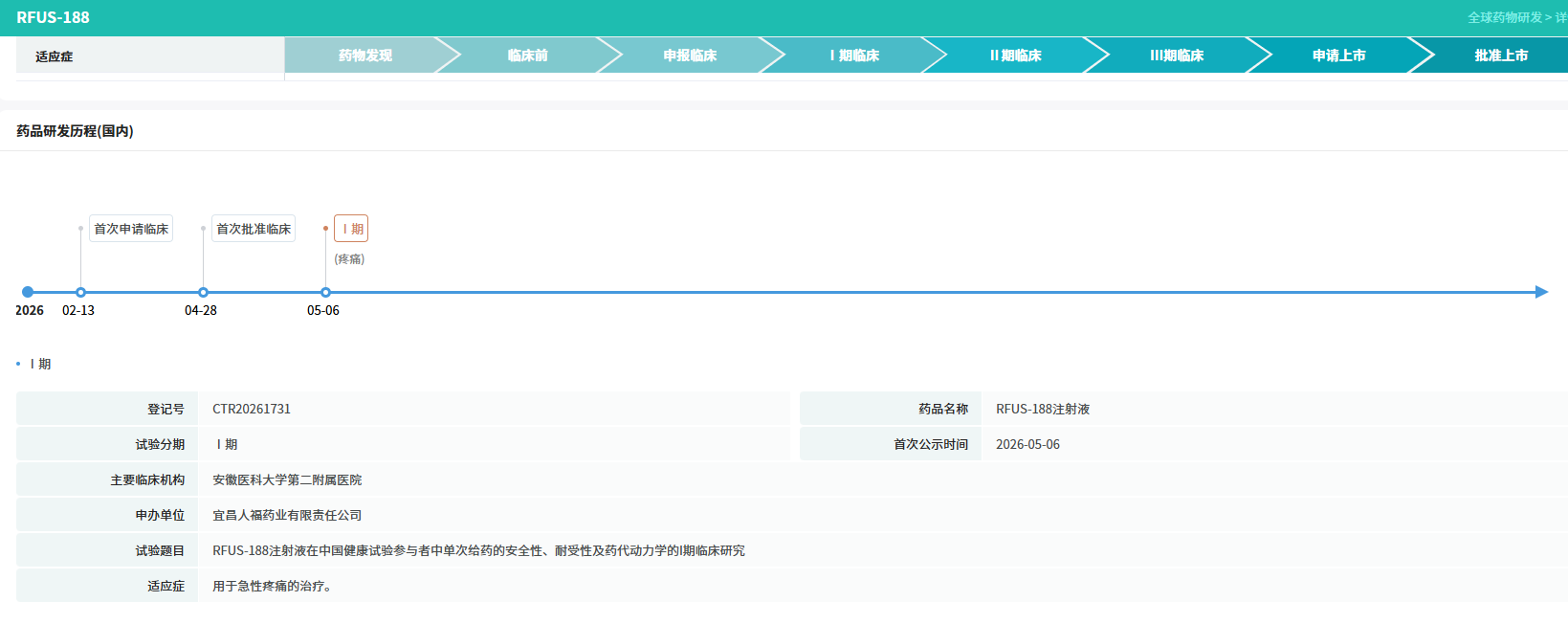
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
人福医药正持续加大研发投入以加快创新转型步伐。2025年年报显示,报告期内公司研发投入合计16.76亿元,同比增长2.84%,占营业收入的6.99%,占制造业主营收入的11.79%。
今年以来,公司已有3款1类新药首次获批临床,除RFUS-188外,拟用于急性疼痛治疗的RFUS-1646片目前已步入Ⅰ期临床;拟用于晚期实体瘤的HW221043片作为新分子实体,目前国内外尚无同类药物获批上市。
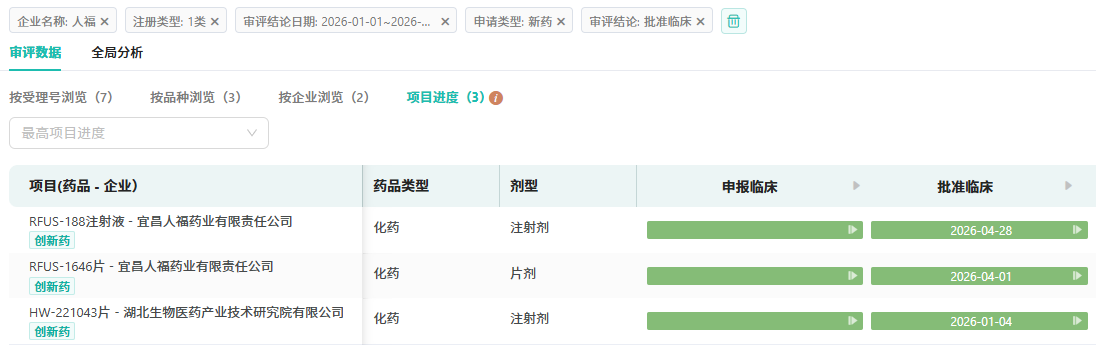
查数据,找摩熵!图源:摩熵医药-中国药品审评数据库
此外,公司在改良型新药(2类)上也密集推进:2.2类新药氨酚羟考酮缓释片报产在审,2.1类新药盐酸右氯胺酮注射液及2.2类新药盐酸艾司氯胺酮口颊粘膜溶液IND申请获受理,均属于神经系统药物。
二、人福药业3亿+品种,获FDA上市批准
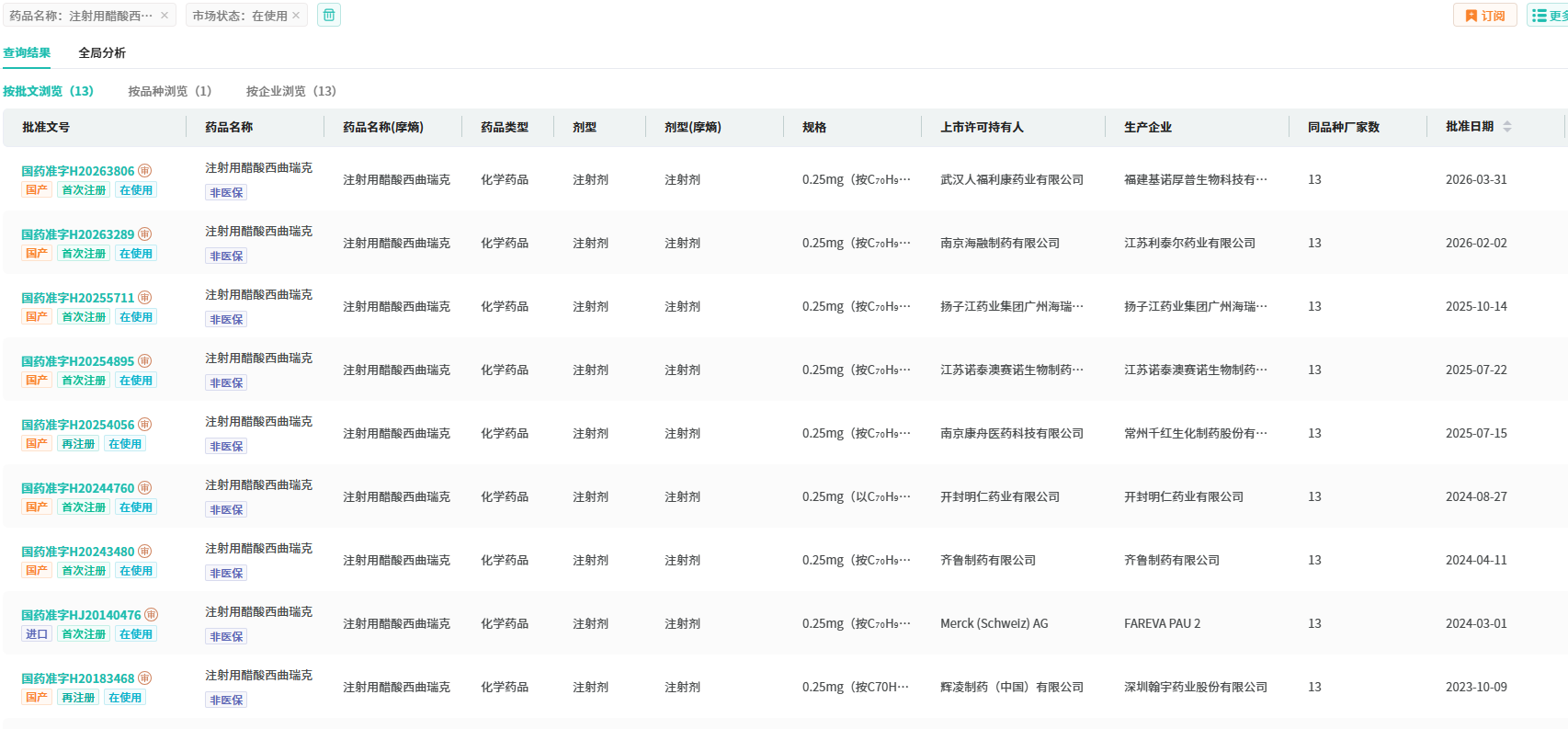
在创新药推进的同时,人福的仿制药国际化业务也迎来实质性兑现。宜昌人福药业美国公司收到美国食品药品监督管理局(FDA)关于注射用醋酸西曲瑞克的批准。注射用醋酸西曲瑞克用于在辅助生殖技术中接受控制性卵巢刺激的女性患者,防止黄体生成素(LH)分泌峰值提前。摩熵医药数据显示,该品种在2025年全终端医院市场的销售额达3.85亿元。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论