
一则上市申请受理公告,让沉寂不久的泌尿领域仿制药赛道泛起涟漪。
2月7日,CDE官网显示,武汉人福药业 按化药注册分类4类申报的 米拉贝隆缓释片 上市申请获受理。
据摩熵医药数据库显示,米拉贝隆 在2024年全球销售额已超11亿美元,成为膀胱过度活动症(OAB)治疗领域当之无愧的重磅品种。
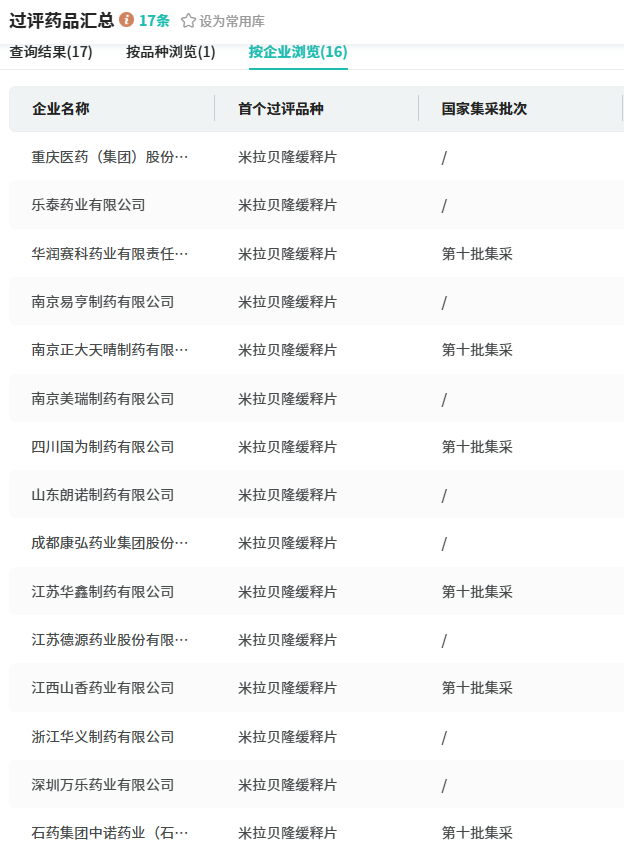
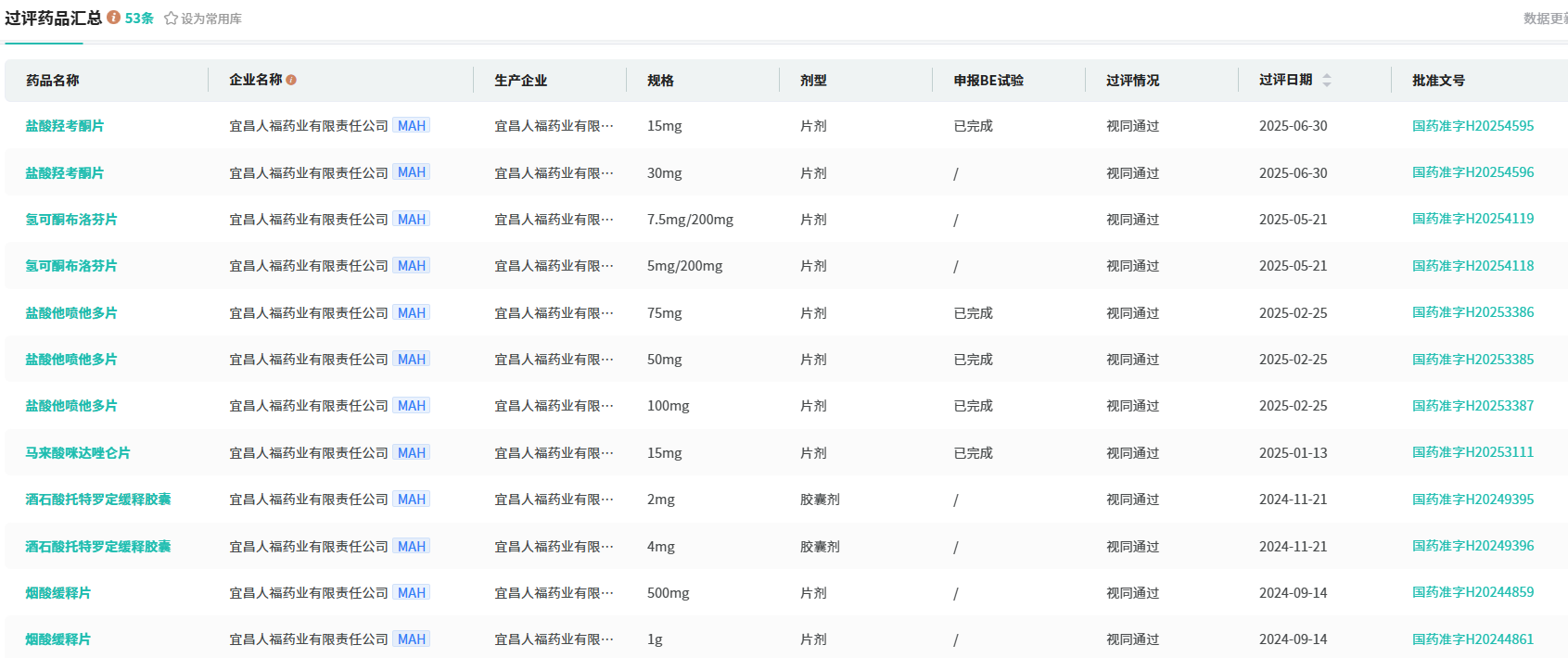
在全球创新药研发风险攀升、普通仿制药利润趋薄的当下,这样一款兼具新机制、高增长、医保覆盖的品种,为何引来多家药企扎堆布局?
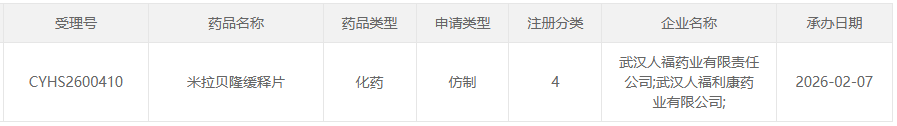
截图来源:CDE官网
2024年院内突破1亿元,同比增长32.51%
米拉贝隆 由日本 安斯泰来(Astellas Pharma Europe B.V.)开发,是全球首个选择性β3-肾上腺素能受体激动剂,用于治疗膀胱过度活动引起的尿急、尿频及尿失禁。它的问世打破了OAB领域近30年缺乏新作用机制药物的局面——既可单用,也可与现有M受体拮抗剂类药物联合使用,显著提升疗效与耐受性。
产品时间轴:
- 2011年9月:日本获批上市;
- 2017年12月:中国获批;
- 2020年:纳入全国医保乙类目录。
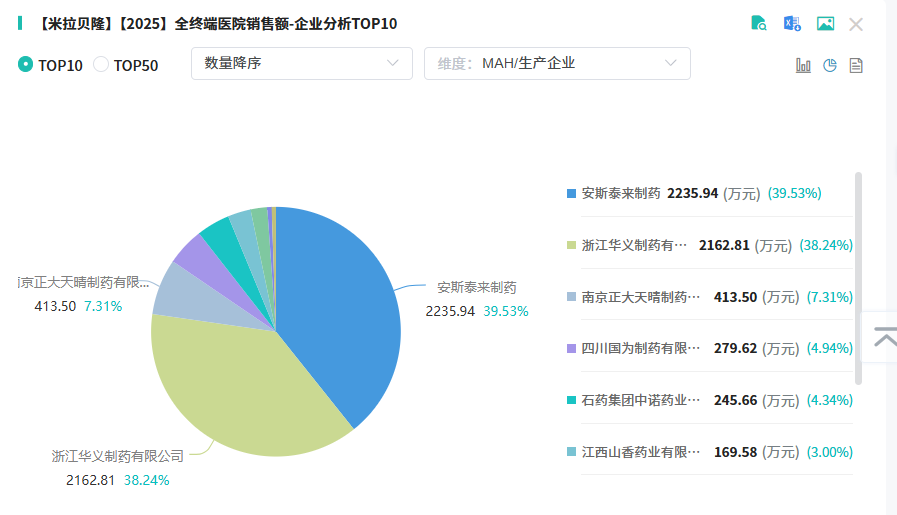
全球市场表现稳健向上,2024年安斯泰来的 米拉贝隆 全球销售额超11亿美元,同比持续增长。国内则处于放量阶段——2022年 米拉贝隆缓释片 在全终端医院的销售额突破5千万元,同比增速高达162.37%;2024年进一步攀升至1亿元,同比增长32.51%。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论