【4月全球在研新药月报】内容亮点
4月国内新药获批临床情况
- 4月共有184款新药获批临床(共计277个受理号),较上个月减少了84款;
- 4月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有106个,占比61%;
- 4月获批剂型主要为注射剂与片剂,分别有156个,79个。
全球获孤儿药/突破性/快速通道资格认定品种盘点
- 4月共有27款药物获孤儿药/突破性/快速通道资格认定。
全球在研创新药积极/失败临床结果最新动态速递
- 艾伯维公布FRα ADC铂敏感卵巢癌II期临床数据;
- 石药突破性疗法Ib/III期研究成功;
- 阿斯利康IL-33单抗又一项III期研究成功;
- 全球首个体内基因编辑疗法III期研究成功。
每月相关创新药最新政策速递、国内新药注册申报、全球获孤儿药/突破性/快速通道资格认定品种盘点、全球在研创新药积极/失败临床结果TOP20、全球创新药研发进展TOP20等,摩熵咨询团队基于真实可溯源的全球医药数据,将每月推出「全球在研新药月报」,以期帮助业内人士通盘把握每月全球范围内的新药开发情况,全面而深入的了解全球新药开发动态。
一、4月国内新药获批临床/上市情况
根据摩熵医药数据库统计,2026年4月共有184款新药获批临床(共计277个受理号),较上个月减少了84款,其中包括71款化药,98款生物制品,15款中药。
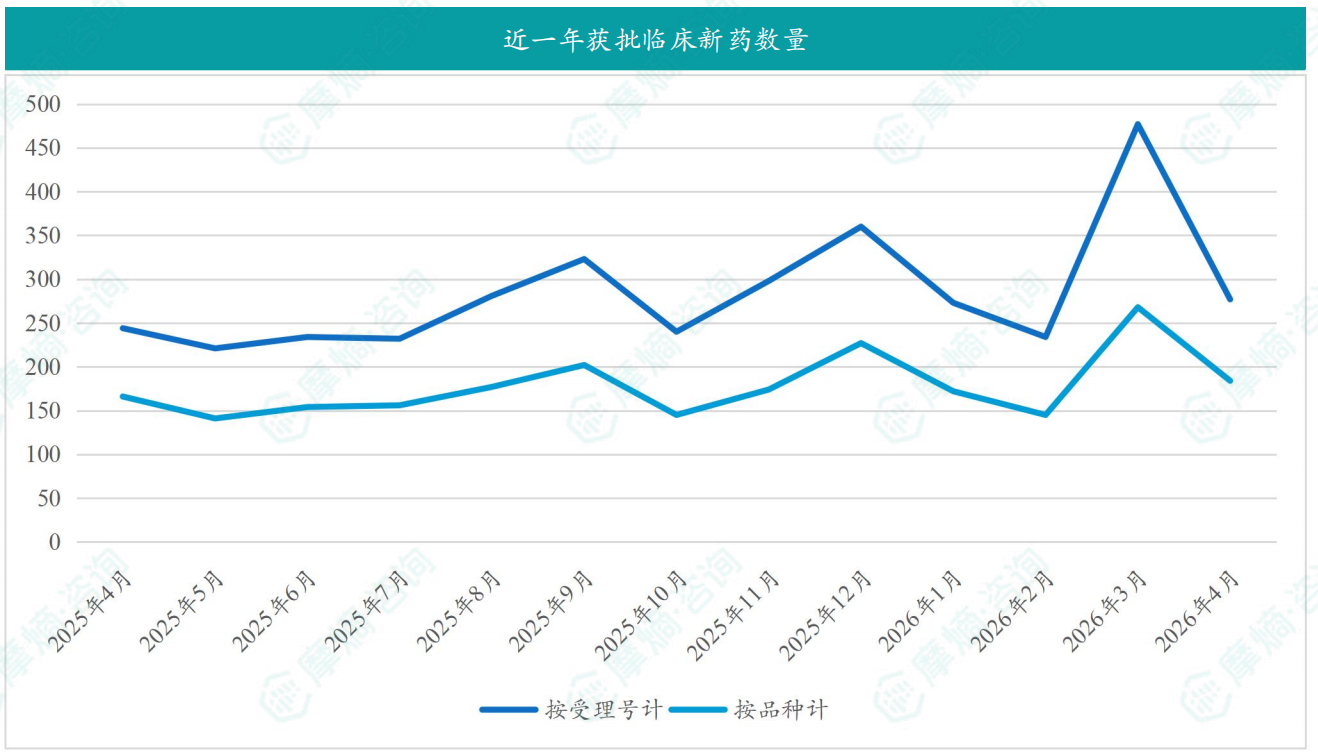
截图来源:摩熵咨询月报
本月获批临床受理号数量最多的新药为抗肿瘤药和免疫机能调节药物,有106个,占比61%,神经系统药物获批数量也比较多,有18个。获批剂型主要为注射剂与片剂,分别有156个,79个。
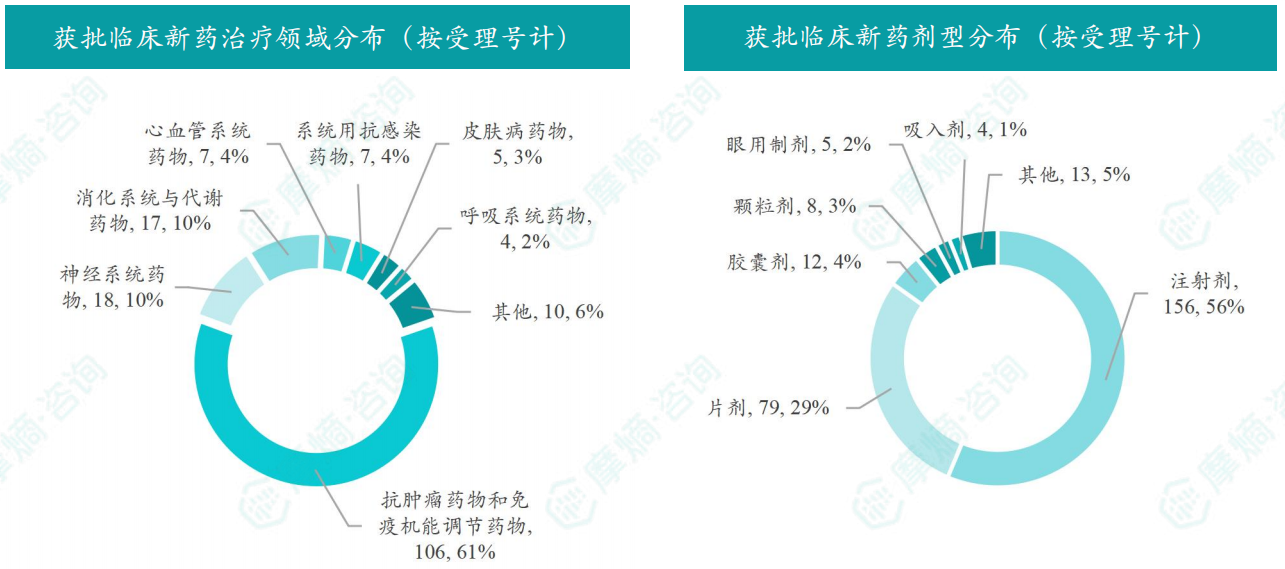
截图来源:摩熵咨询月报
2026年4月,国内医药市场迎来了6款创新药物的获批上市,涉及瑞迪奥的1类放射性创新药锝[99mTc]佩昔瑞特加肽注射液及制备该药品的注射用锝[99mTc]佩昔瑞特加肽药盒通过优先审评审批程序获批上市,用于可疑肺癌患者区域淋巴结转移的辅助检查。这是中国第一个自主研发的1类创新核药,也是全球首个用于SPECT显像的广谱肿瘤显像剂。该产品的获批,突破了核医学SPECT(单光子发射计算机断层)影像技术不能用于肿瘤诊断、分期、疗效监测的瓶颈问题。更重要的是,打破了过去近30年间美国主导的核医学肿瘤显像诊断只有PET(正电子发射断层)影像技术的局面,为核医学领域带来突破。
4月10日,国家药监局官网显示,阿斯利康的抗CTLA-4单抗——曲麦利尤单抗(曾用名:替西木单抗)获批上市。该药物常与阿斯利康的抗PD-L1单抗度伐利尤单抗组成组合疗法,该组合疗法已在美国、日本和欧洲获批用于不可切除的肝癌患者以及无EGFR敏感突变或ALK阳性突变的转移性非小细胞肺癌(NSCLC)患者的一线治疗。此次获批基于多项全球多中心Ⅲ期临床研究的积极数据,其中在肝癌领域开展的HIMALAYA 研究、肺癌领域开展的POSEIDON研究均证实,曲麦利尤单抗联合度伐利尤单抗的双免疫方案,可显著延长患者总生存期,降低死亡风险,且整体安全性可控,为临床应用奠定了坚实的循证医学基础。
2026 年4月国内获批上市的新药
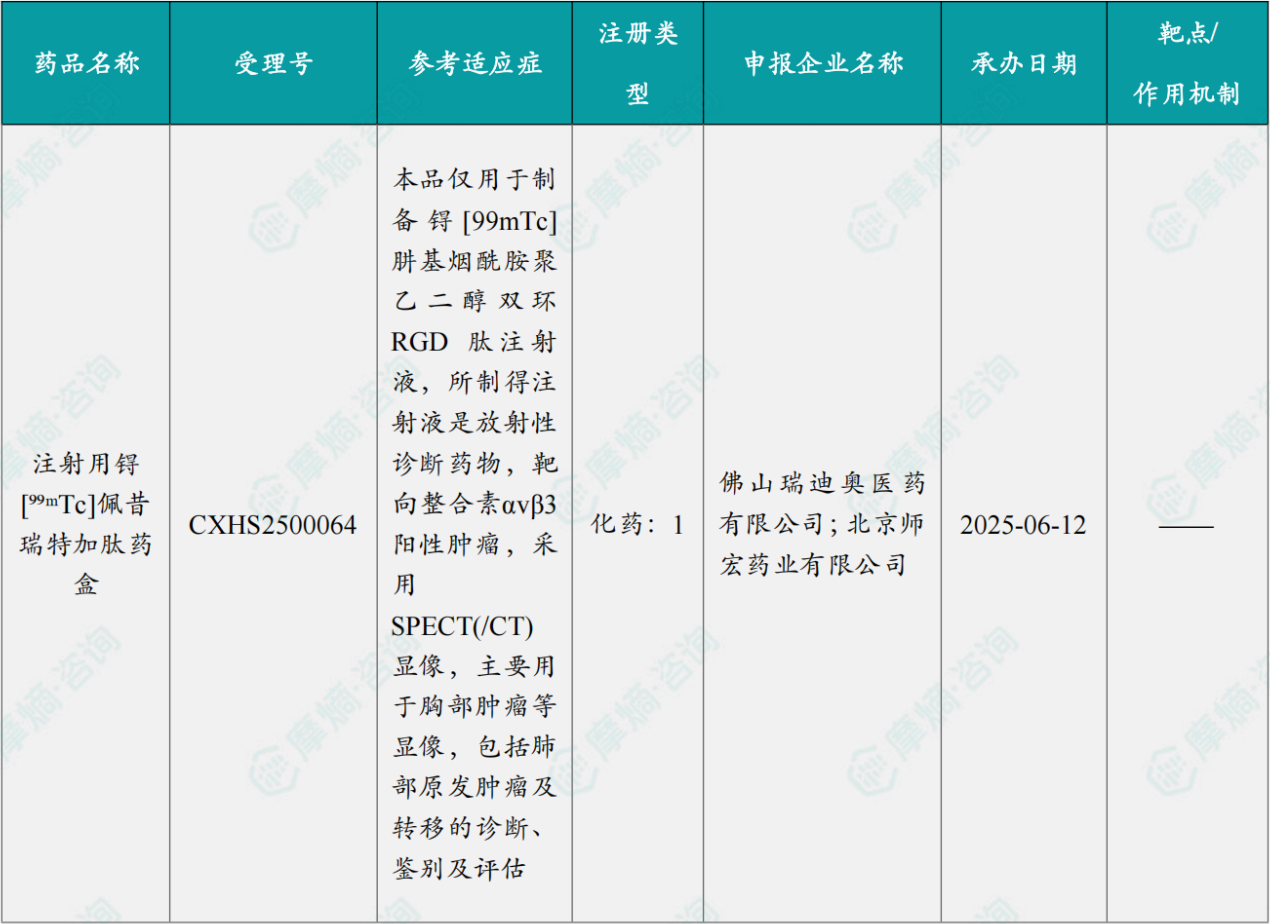
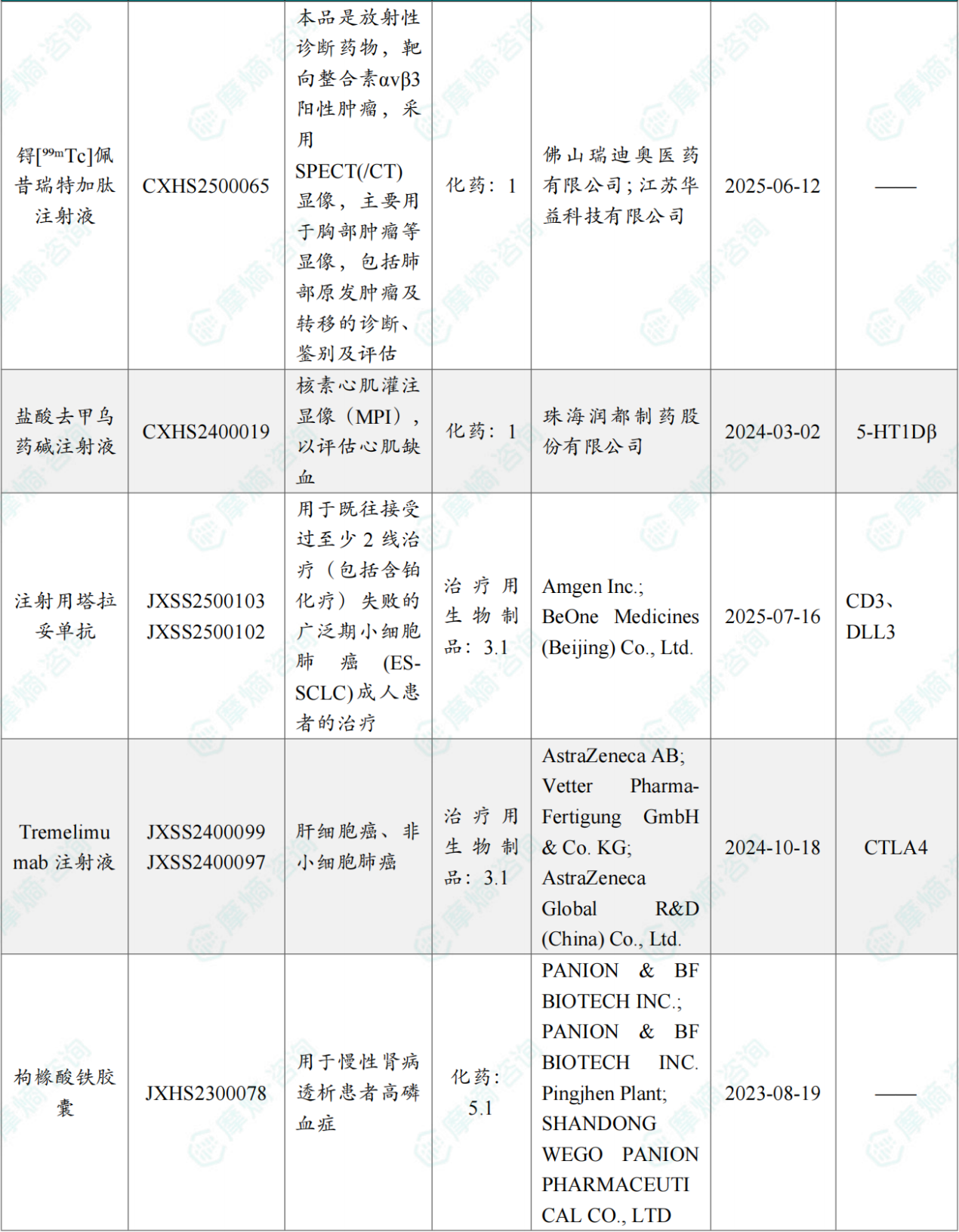
截图来源:摩熵咨询月报
二、全球获孤儿药/突破性/快速通道资格认定品种盘点
据摩熵医药数据统计,2026年4月共有27款药物获孤儿药/突破性疗法/快速通道资格认定。
其中值得关注的是,4月30日,上海安领科生物医药有限公司宣布美国食品药品监督管理局(FDA)已授予其核心在研管线ALK-201用于治疗胃癌的孤儿药资格认定(Orphan Drug Designation,ODD)。
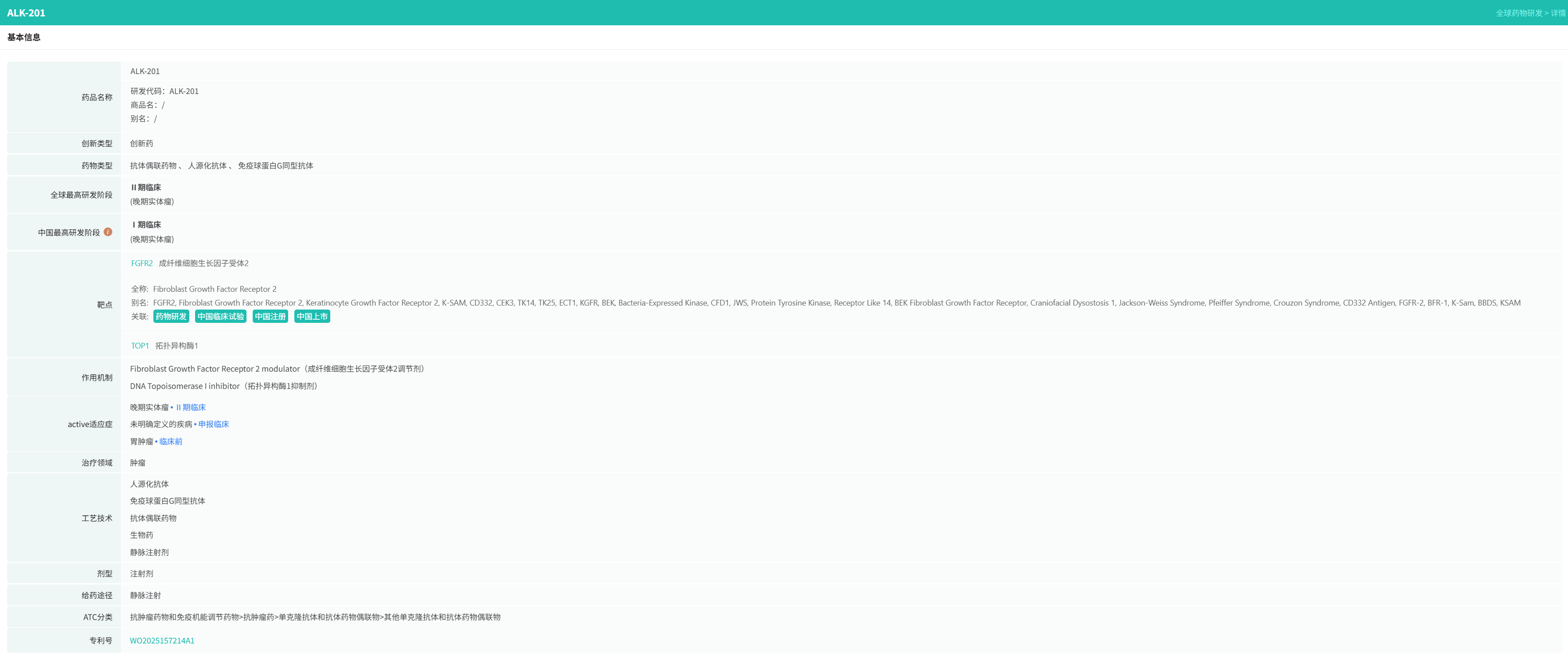
查数据,找摩熵,图源:摩熵医药-全球药物研发数据库
ALK201是一款针对成纤维细胞生长因子受体-2b(FGFR2b)、由安领科生物自主研发的一款创新FGFR2b靶向ADC药物。作为驱动肿瘤生长的关键驱动因子,FGFR2b在胃癌及多种上皮来源的恶性肿瘤中具有显著的预后指示意义。研究表明,FGFR2b在肿瘤组织中的病理性过表达与肿瘤的侵袭性行为及不良预后密切相关。
4月全球孤儿药/突破性/快速通道资格认定品种一览表(部分)
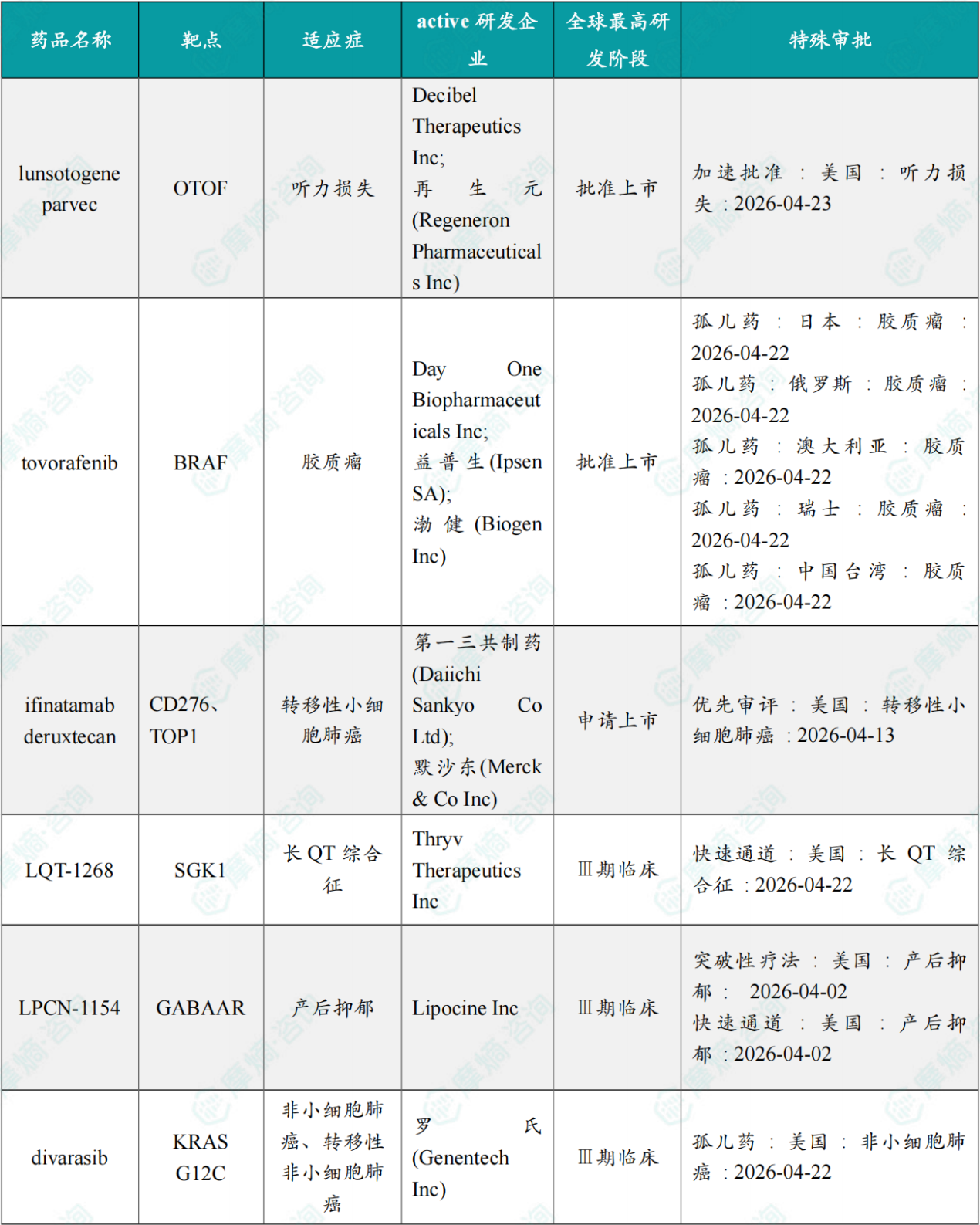
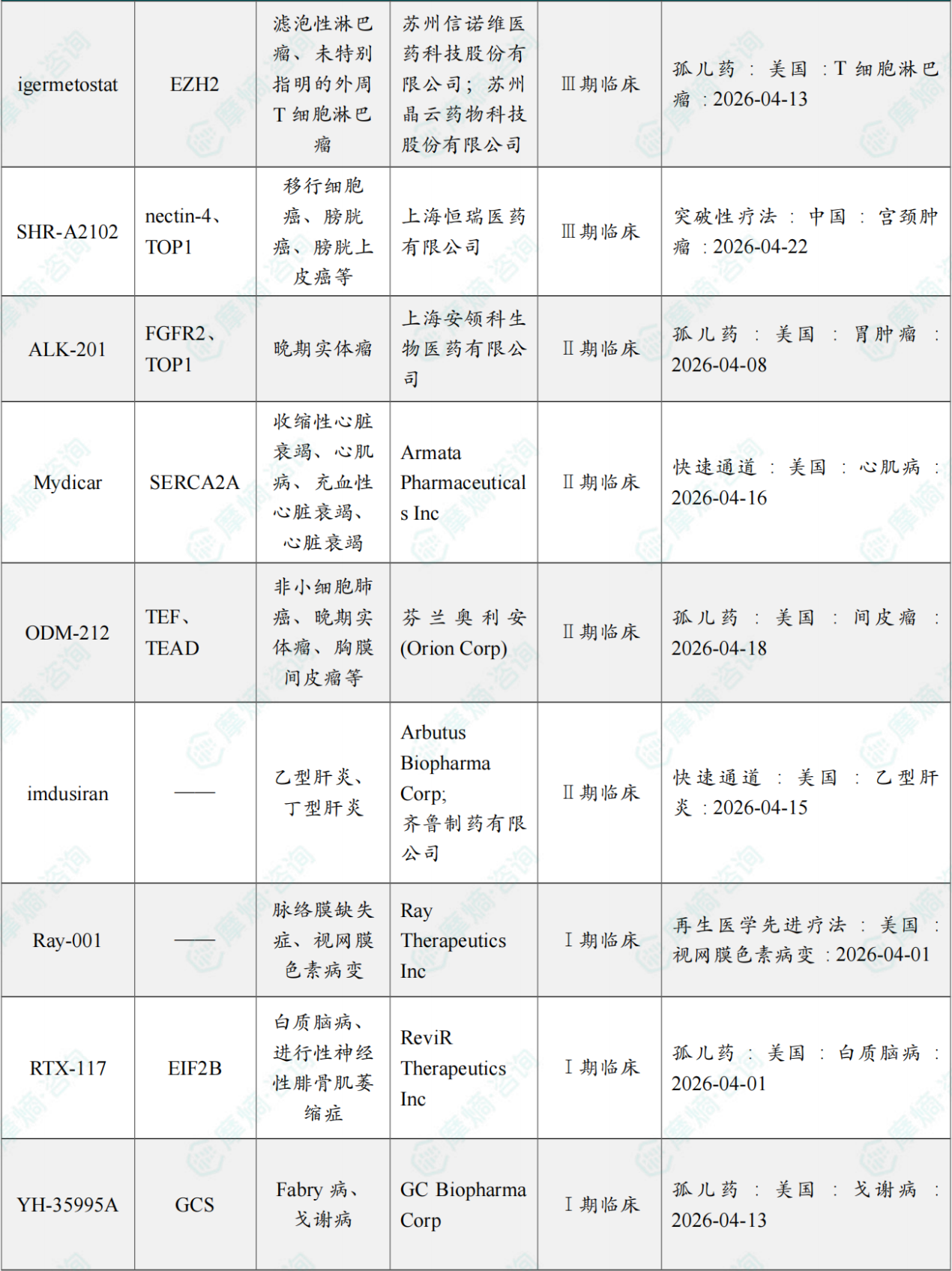
截图来源:摩熵咨询月报
三、全球在研创新药积极/失败临床结果TOP20
4月6日,安进(Amgen)宣布其治疗中重度活动性甲状腺眼病(TED)的药物TEPEZZA在皮下注射(使用贴片式注射器,即OBI)的3期临床试验中取得了积极的顶线结果。
数据显示,在24周的安慰剂对照期内,TEPEZZA OBI达到了主要终点,具有高度统计学意义和临床意义的突眼反应率高达77%,而安慰剂组仅为19.6%。作为一个关键的次要终点,TEPEZZA OBI在第24周时的平均突眼减少量达到了3.17毫米,远优于安慰剂组的0.80毫米。这一结果证明了皮下注射能够提供与传统静脉输注(IV)相当的卓越疗效,还为患者提供了一种更为便捷的治疗选择,从而避免了传统方法中需要每三周进行一次、共计8次且每次耗时60至90分钟的静脉输注。
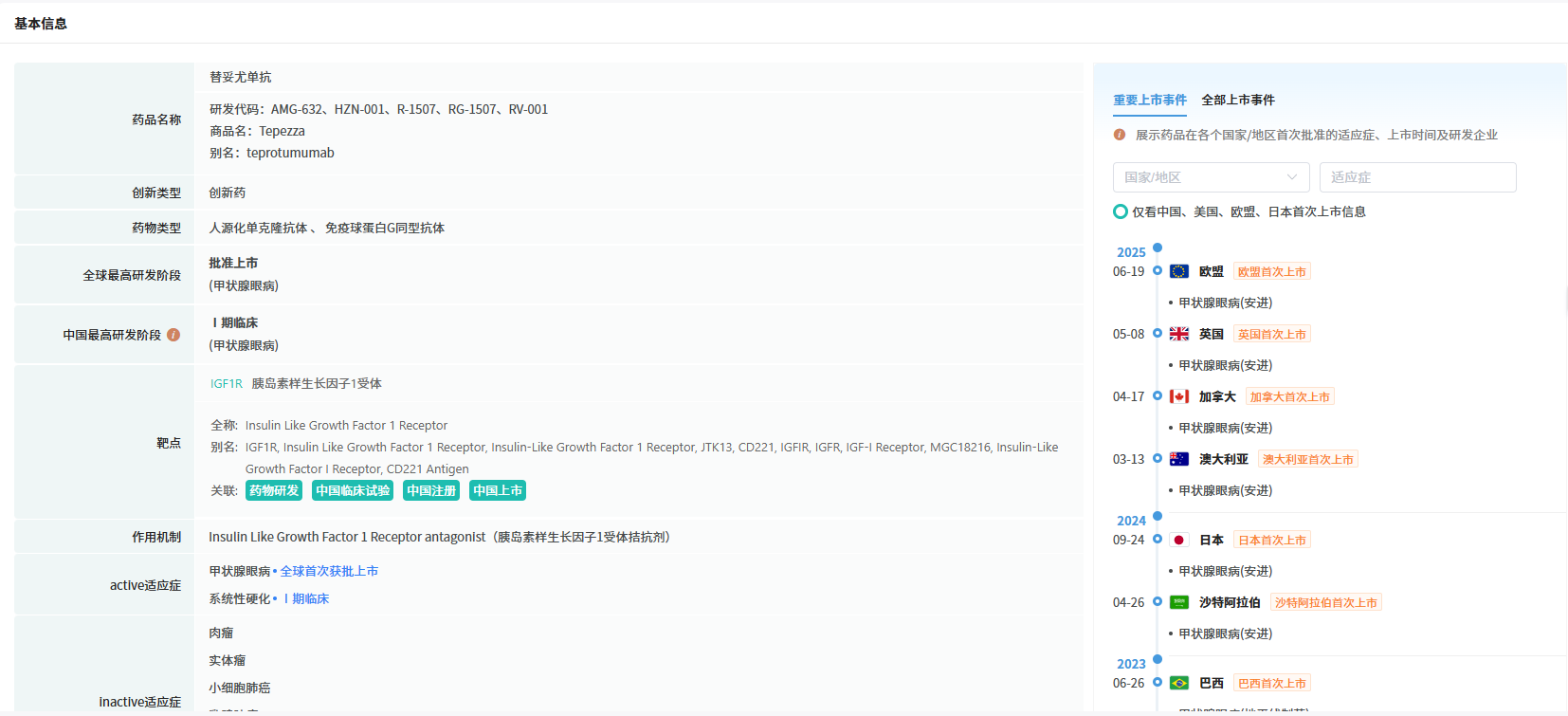
查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
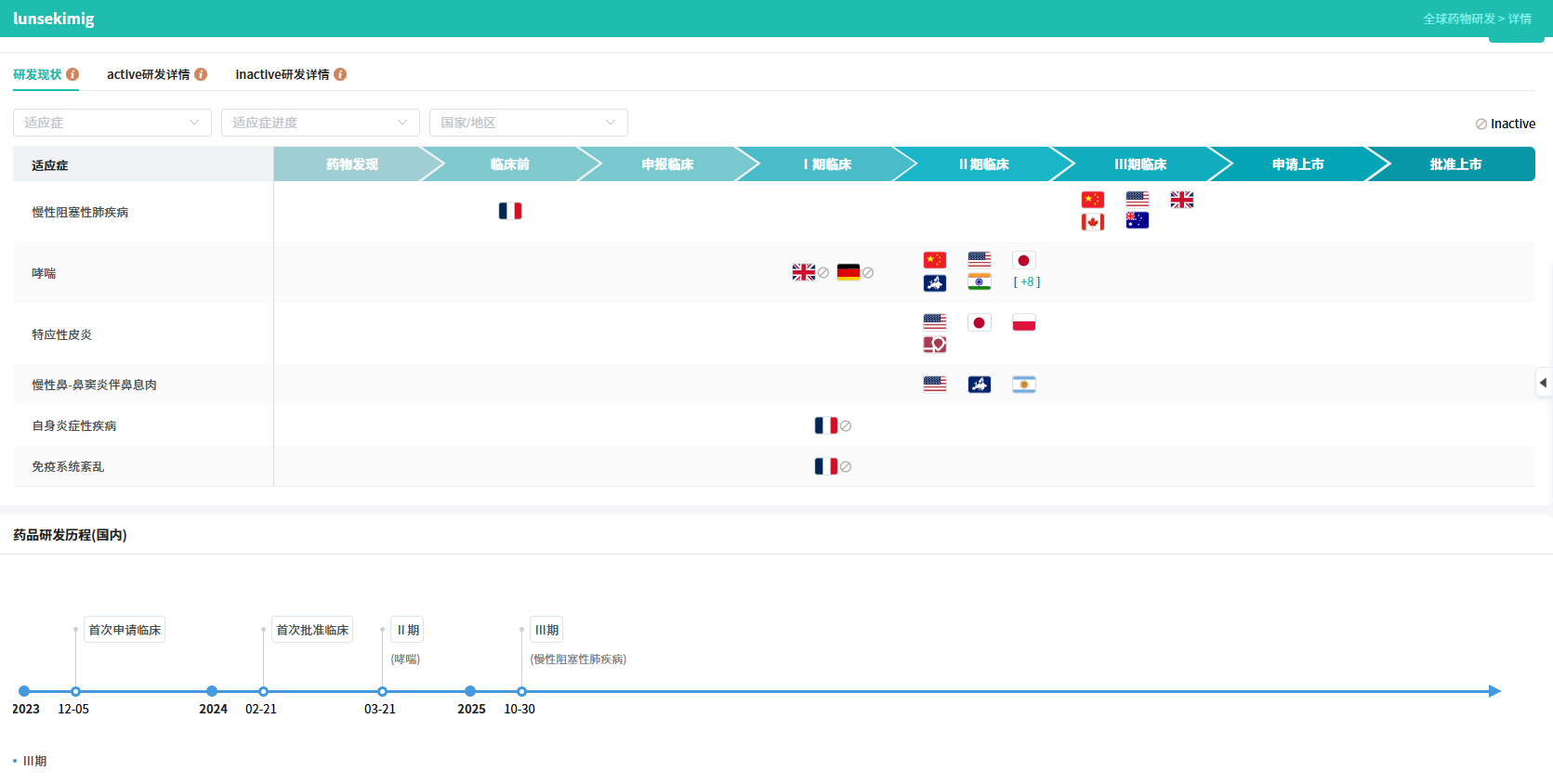
4月7日,赛诺菲宣布TSLP/IL-13双抗lunsekimig在两种慢性呼吸系统疾病中进行的II期研究均达到了主要终点和关键次要终点。在两项研究中,lunsekimig耐受性良好,安全性特征可接受。
Lunsekimig是一款first in class新型五价纳米抗体VHH,由五个连接的抗体片段组成,旨在同时阻断TSLP和IL-13,同时结合白蛋白以延长半衰期。AIRCULES是一项随机、双盲、安慰剂对照的IIb期临床研究,旨在评估皮下注射lunsekimig联合标准治疗在中重度哮喘成人患者中的疗效、安全性和耐受性。
查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
结果显示,lunsekimig达到了主要终点和关键次要终点,显示出哮喘急性加重率的统计学显著性和临床意义的降低,以及肺功能的改善。DUET是一项随机、双盲、安慰剂对照的IIa期研究,旨在评估皮下注射lunsekimig在慢性鼻窦炎伴鼻息肉(CRSwNP)成人患者中的疗效、安全性和耐受性。该研究同样达到了主要终点,即鼻息肉评分自基线的变化,以及关键次要终点,患者报告的鼻塞/阻塞评分变化和Lund-Mackay计算机断层扫描(LMK-CT)评分变化。
全球在研创新药积极/失败临床结果TOP20
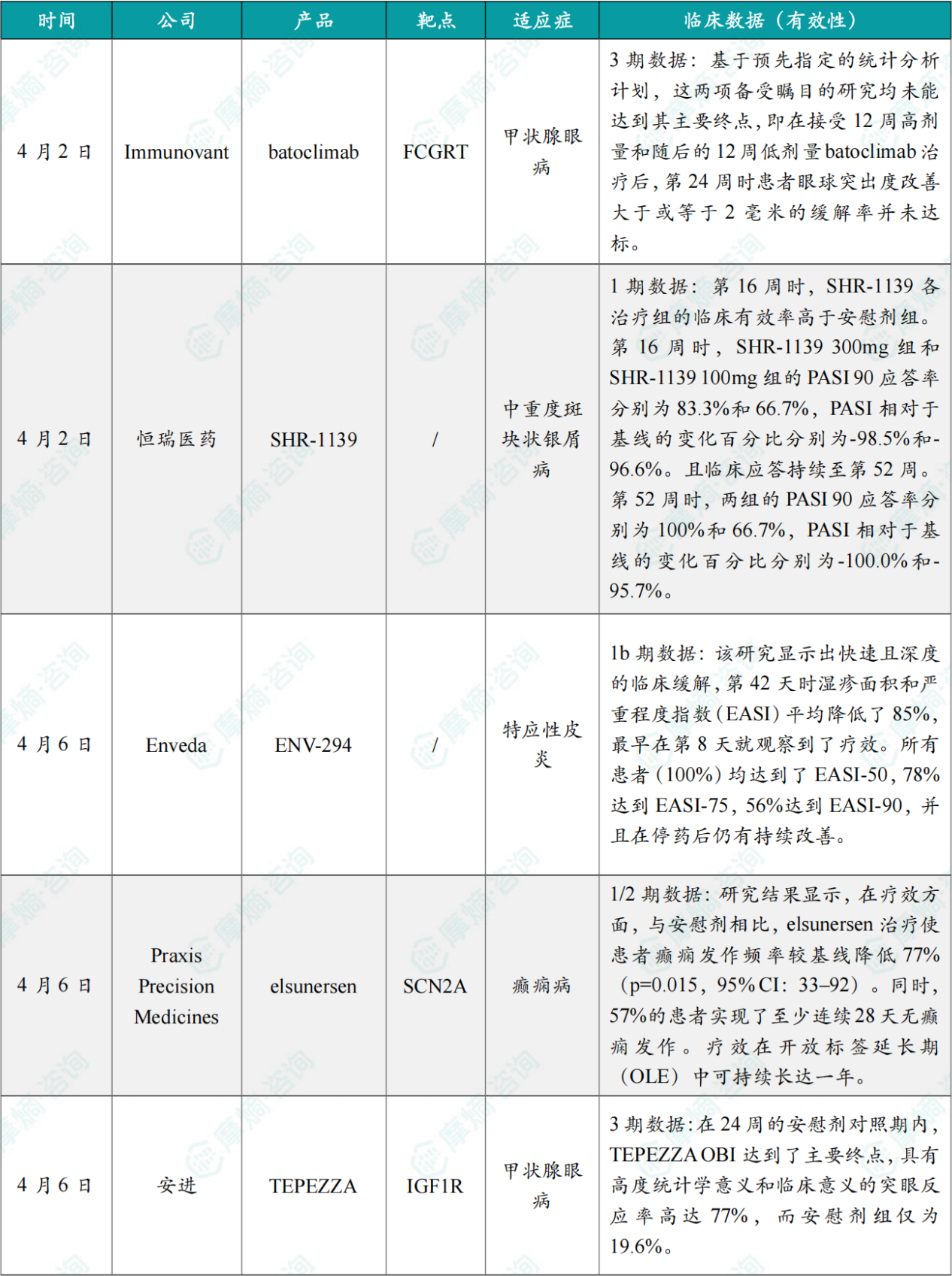
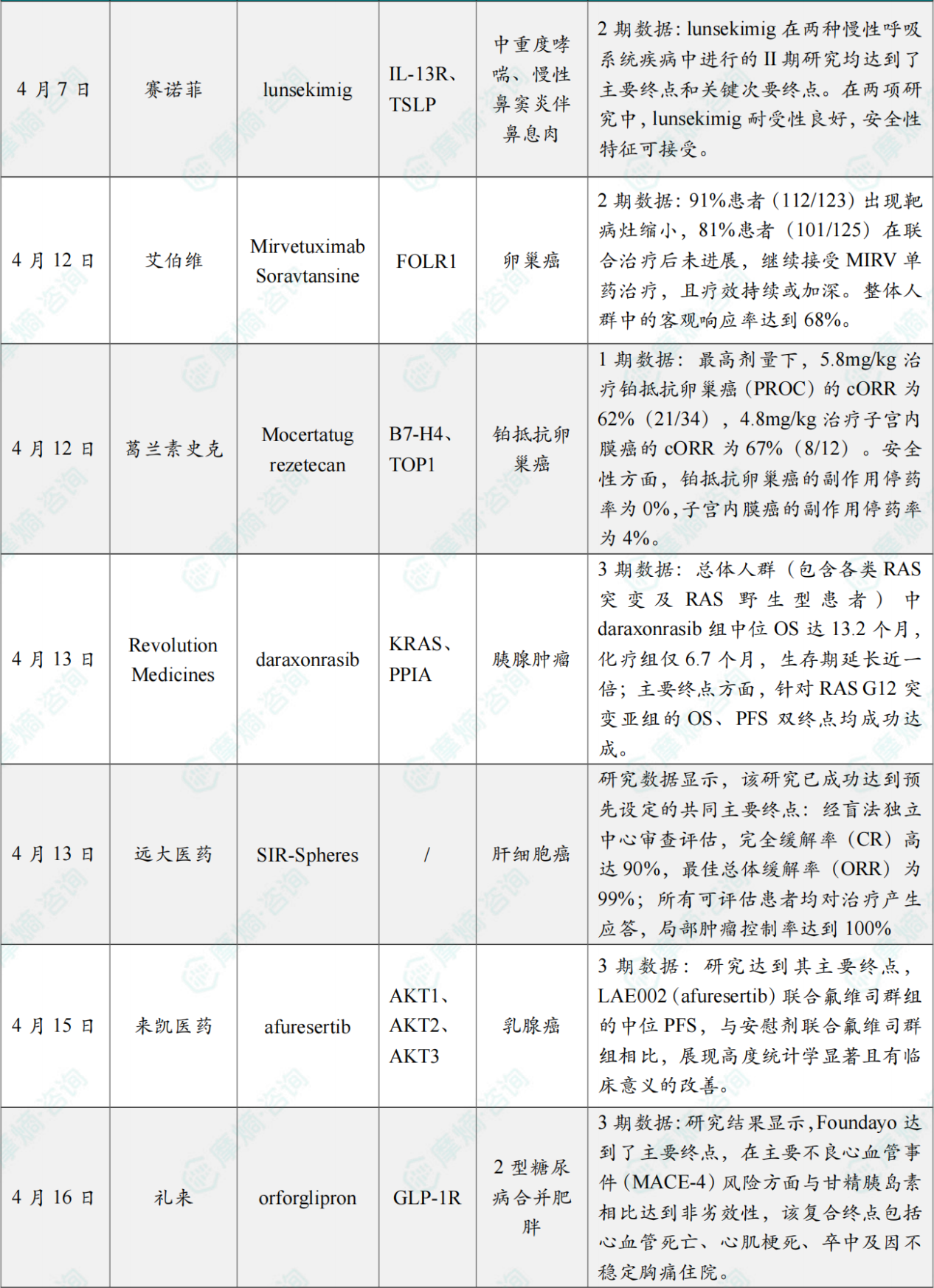
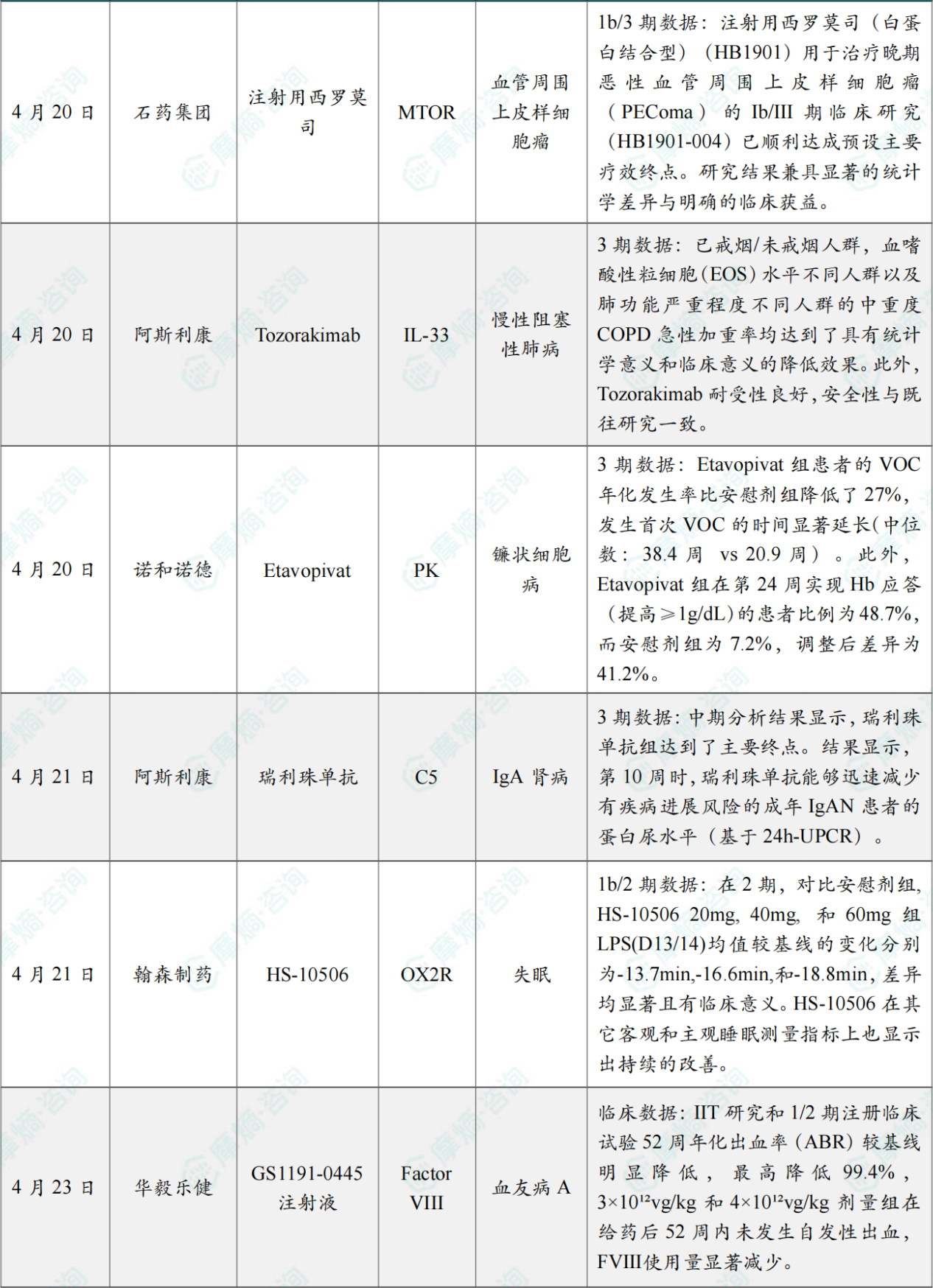
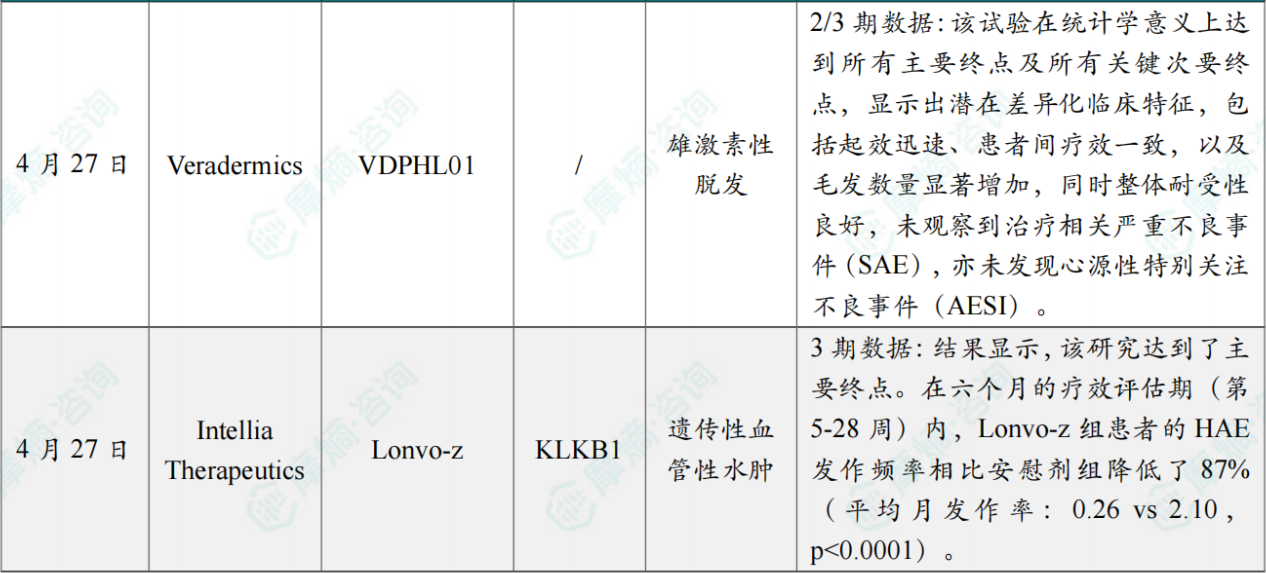
截图来源:摩熵咨询月报
四、全球创新药研发进展TOP20
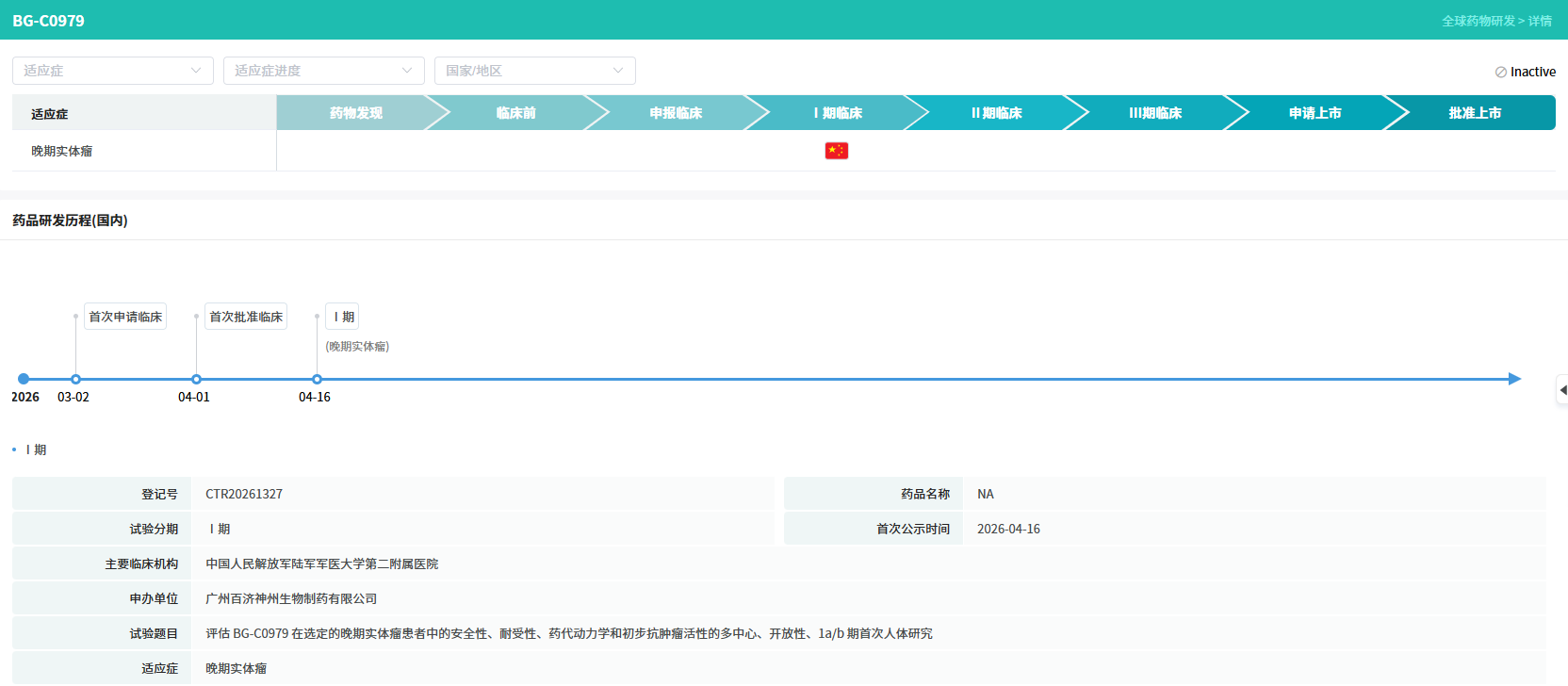
4月1日,CDE官网显示,百济神州的注射用BG-C0979获批临床,用于治疗晚期实体瘤。这是国内第二款获批临床的ADAM9 ADC。此前2026年2月,百济神州已经在Clinicaltrial网站上登记了一项评估BG-C0979单药治疗或与替雷利珠单抗联合治疗晚期实体瘤患者的安全性、耐受性、药代动力学和初步抗肿瘤活性的I期临床(NCT07414836)。
目前全球在研的ADAM9 ADC中进入临床阶段的有3款,分别是MacroGenics的MGC028、映恩生物的DB-1317和百济神州的BG-C0979。
查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
4月7日,CDE官网显示,施维雅的Vorasidenib片拟纳入优先审评,用于携带异柠檬酸脱氢酶-1(IDH1)或异柠檬酸脱氢酶-2(IDH2)突变的2级星形细胞瘤或少突胶质细胞瘤成人和12岁及以上儿童患者的手术(包括活检、次全切除或全切除)后治疗。
Vorasidenib是施维雅在2020年通过收购Agios公司所得的一款口服、选择性、高度脑渗透性的双重抑制剂,2024年8月,该药首次获得FDA批准上市,成为全球首个获批上市的IDH1/2双靶点抑制剂,也是近20年来IDH突变型弥漫性脑胶质瘤治疗领域首个创新靶点药物。
全球创新药研发进展 TOP20
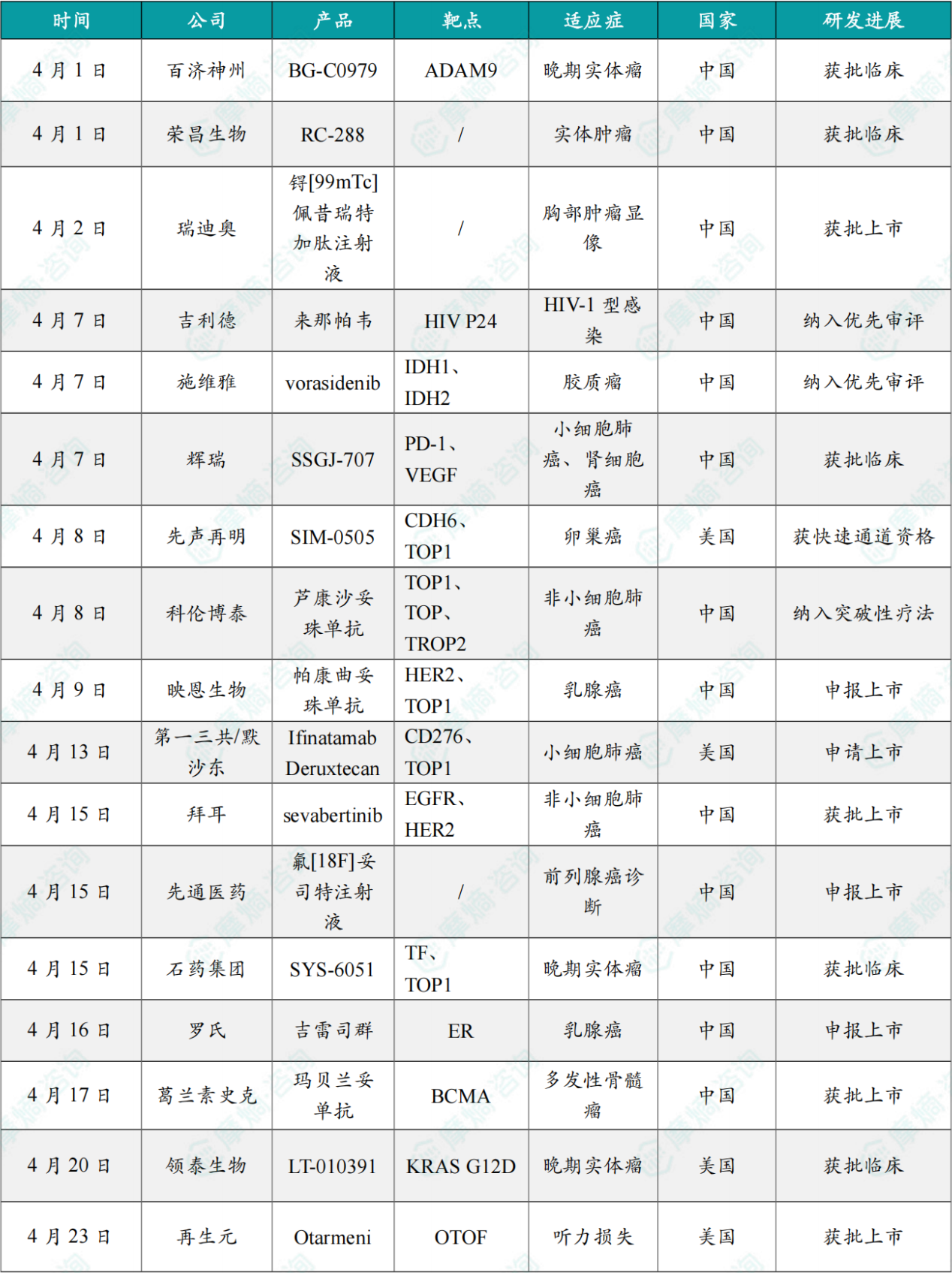
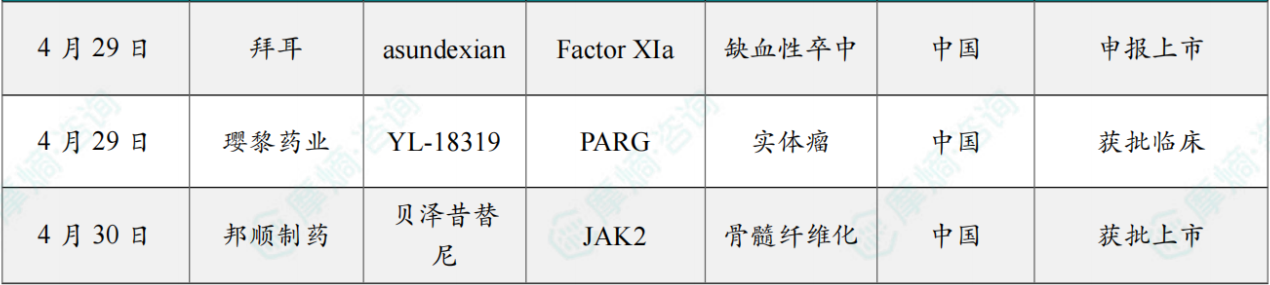
截图来源:摩熵咨询《2026年4月全球在研新药月报》
以上内容均来自摩熵咨询{ 2026年4月全球在研新药月报 },如需查看或下载完整版报告,可点击!
扩展阅读:
1. 2026年3月新药月报:268款新药获批临床!15款纳入特殊审评,涉及赛诺菲、辉瑞、华东医药…
2. 2026年2月全球新药全景:145款新药获批临床!41款纳入特殊审评,涉及赛诺菲、阿斯利康、武田…
3. 2026年1月全球新药动态全览:172款新药获批临床!35款纳入特殊审评,涉及默沙东、礼来、诺华…
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论