1.4.1 本周全球TOP10创新药研发进展
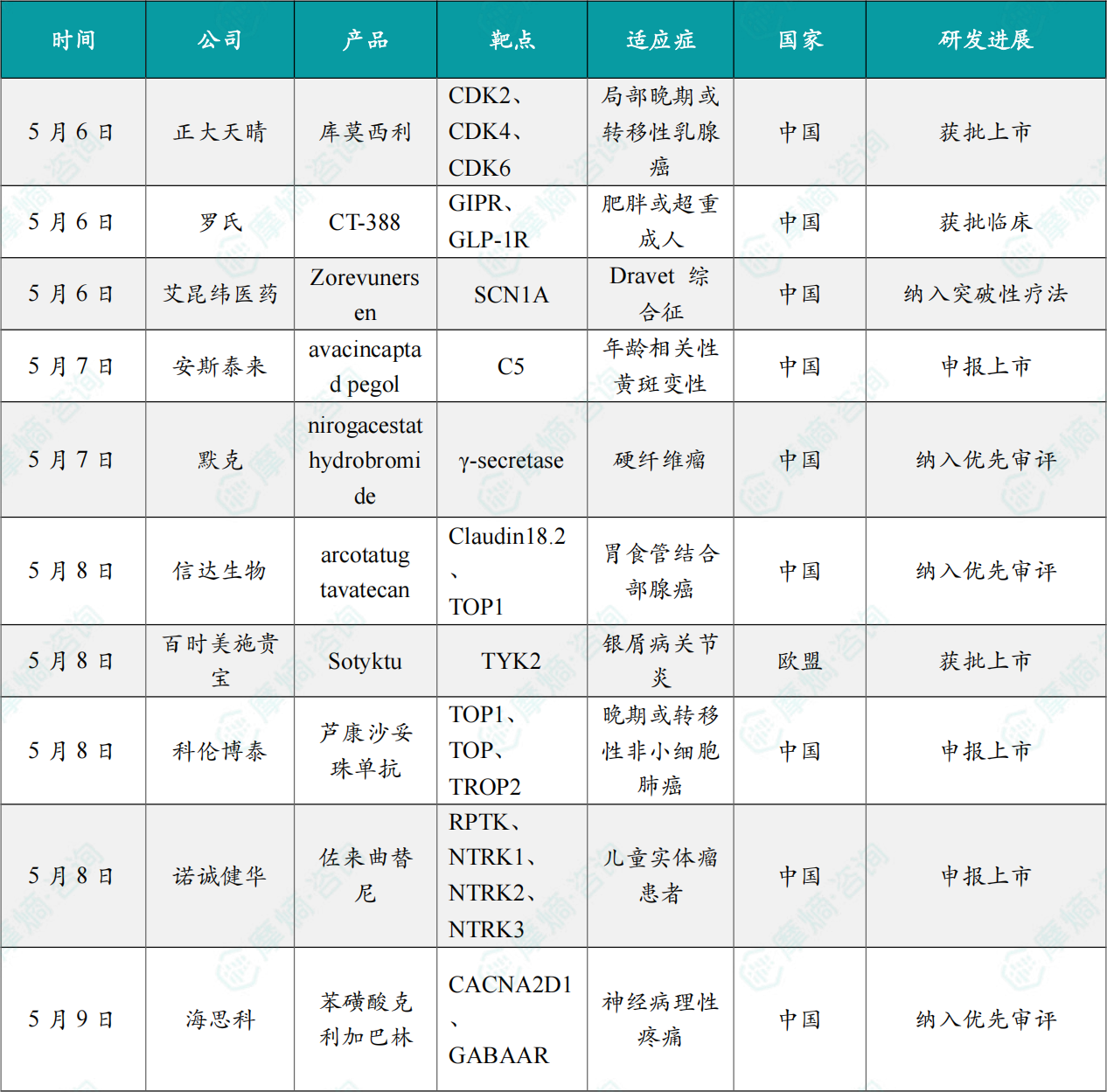
(1)正大天晴全球首款CDK2/4/6抑制剂一线适应症获批
5月6日,中国生物制药下属企业正大天晴自主研发的全球首个CDK2/4/6抑制剂库莫西利胶囊获得国家药品监督管理局(NMPA)批准,联合氟维司群用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌患者的初始治疗。
这是库莫西利胶囊获批上市的第2个适应症。本次新增适应症的获批主要基于CULMINATE-2临床研究结果。CULMINATE-2研究证实,库莫西利联合氟维司群一线治疗HR+/HER2-晚期乳腺癌,客观缓解率达59.3%,疾病进展或死亡风险降低44%。
(2)罗氏GLP-1新药首次在国内获批临床
5月6日,CDE 官网显示,罗氏 RO7795068 注射液获批临床,用于控制饮食和增加运动的基础上对肥胖或超重成人患者的长期体重管理。RO7795068 是 Carmot 开发的一款 GLP-1R/GIPR 双重激动剂。
2023年12 月,罗氏31亿美元收购Carmot囊获了该产品。目前,RO7795068 的肥胖适应症在境外已经推进到了 III 期临床阶段。II 期结果显示,每周一次皮下注射 RO7795068(剂量逐渐增加至 24mg)可使患者体重显著减轻 22.5%(疗效估计值),且在 48 周时未达到体重减轻平台期。研究观察到体重减轻与剂量之间存在明显的剂量反应关系。在治疗方案估计值分析中,RO7795068 实现的安慰剂校正体重下降为 18.3%(p<0.001)。
(3)艾昆纬医药申报的 Zorevunersen 注射液拟纳入突破性治疗品种
5月6日,CDE官网显示,艾昆纬医药申报的 Zorevunersen注射液 拟纳入突破性治疗品种,用于治疗 Dravet 综合征。
Zorevunersen 是一种在研反义寡核苷酸,旨在通过从未受影响的(野生型)SCN1A 基因拷贝中提高大脑细胞内功能性 NaV1.1 蛋白的产量,从而治疗 Dravet 综合征的病因。Zorevunersen 已展现出疾病修正潜力,并已获得 FDA 和 EMA 授予的孤儿药资格认定。此外,FDA 还授予 zorevunersen 治疗伴有经确认的 SCN1A 基因非功能获得性突变的 Dravet 综合征的罕见儿科疾病认定和突破性疗法认定。
2025年2月,Stoke与渤健达成战略合作,渤健则获得该药物在美国、加拿大和墨西哥以外的全球其他地区的独家商业化权益。
(4)安斯泰来眼科新药申报上市
5月7日,CDE网站显示,安斯泰来的眼科新药培阿普特玻璃体内注射液(Avacincaptad pegol)申报上市。根据3月的优先审评动态,本次申报的适应症为用于治疗继发于年龄相关性黄斑变性(AMD)的地图样萎缩(GA)。该药物有望成为国内首个获批上市的AMD继发GA治疗药物。
Avacincaptad pegol是一种旨在抑制补体C5蛋白的聚乙二醇化RNA适配体。2023年5月,安斯泰来以59亿美元的总交易额收购Iveric Bio,获得该药物的相关权益。2023年8月,该药物(商品名:Izervay)获FDA批准上市,用于治疗AMD继发GA,获批的用药方案是每个月给药1次,持续最多1年。2025年2月,经FDA批准,Izervay的给药持续时间再无限制——为医生和患者管理GA提供了更大的灵活性。
(5)默克39亿美元收购新药国内拟纳入优先审评
5月7日,CDE官网显示,默克申报的氢溴酸尼罗司他片(Nirogacestat)拟纳入优先审评,用于需要系统性治疗的进展性韧带样纤维瘤病(也称为硬纤维瘤或侵袭性纤维瘤病)的成人患者。
Nirogacestat(商品名:Ogsiveo)是一种 first-in-class 疗法,已获得美国 FDA 和欧洲药品管理局 (EMA) 批准上市,是治疗需要全身治疗的进展性纤维瘤成人患者的系统性标准疗法。
默克于2025年4月以39亿美元收购SpringWorks Therapeutics 囊获了这款药物。FDA 和 EMA 的批准是基于其 III 期 DeFi 试验的结果,该试验达到了改善无进展生存期(PFS)的主要终点,与安慰剂相比,疾病进展或死亡风险显著降低 71%(HR= 0.29)。
(6)信达生物CLDN18.2 ADC拟纳入优先审评
5月8日,CDE网站显示,信达生物的CLDN18.2 ADC拟纳入优先审评,用于至少接受过两种系统治疗的局部晚期不可切除或转移性CLDN18.2阳性胃或胃食管结合部腺癌。该适应症已于2024年5月被纳入突破性疗法。目前尚无CLDN18.2 ADC正式申报上市,也无同类药物被纳入优先审评。
IBI343是信达生物自主研发的潜在全球首创注射用重组抗CLDN18.2单克隆抗体-依喜替康偶联物。作为创新型TOPO1i型ADC,IBI343在临床I期研究中展现出可控的安全性和令人鼓舞的疗效性信号。目前信达生物正在开展IBI343后线治疗胃癌和胰腺癌的III期临床试验。此前,IBI343已经有3项适应症被纳入突破性疗法。
(7)百时美施贵宝宣布欧洲委员会已正式批准Sotyktu用于治疗成人活动性银屑病关节炎
5月8日,百时美施贵宝宣布,欧洲委员会已正式批准Sotyktu(deucravacitinib)用于治疗成人活动性银屑病关节炎(PsA)。该药物可单独使用,适用于对既往改善病情抗风湿药(DMARD)治疗应答不足或不耐受的患者。
作为每日一次口服给药的酪氨酸激酶2(TYK2)选择性抑制剂,Sotyktu是欧盟首个获批用于治疗活动性银屑病关节炎的TYK2抑制剂。此次欧盟批准基于两项关键性III期临床试验——POETYK PsA-1和POETYK PsA-2的积极结果。
(8)科伦博泰重磅ADC第5项新适应症在华申报上市
5月8日,科伦博泰发布公告称,其 TROP2 ADC 芦康沙妥珠单抗(sac-TMT,亦称 SKB264/MK-2870)的一项新增适应症上市申请已获 CDE 受理,用于联合默沙东的 PD-1 单抗帕博利珠单抗一线治疗 PD-L1 肿瘤比例分数 (TPS)≥1% 的 EGFR 基因突变阴性和 ALK 阴性的局部晚期或转移性非小细胞肺癌 (NSCLC) 患者。
该申请是芦康沙妥珠单抗获 NMPA 受理的第五项适应症上市申请,已被纳入优先审评。本次受理是基于 OptiTROP-Lung05 注册Ⅲ期研究的积极结果。
(9)诺诚健华不限癌种疗法新适应症在华申报上市
5月8日,CDE官网显示,诺诚健华的佐来曲替尼口崩片一项新适应症上市申请获得受理。根据该药的研究进度推测本次申报的新适应症为:用于治疗携带神经营养酪氨酸受体激酶(NTRK)融合基因的儿童实体瘤患者(2 岁至 12 岁)。此前,该适应症已被 CDE 纳入优先审评和「儿童抗肿瘤药物研发鼓励试点计划(星光计划)」。
佐来曲替尼(Zurletrectinib, ICP-723)是诺诚健华自主研发的新一代 TRK 抑制剂,该药于 2025 年 12 月首次获得 NMPA 批准上市,用于治疗携带 NTRK 融合基因的成人和 12 岁以上青少年实体瘤患者,成为首款获批的国产 TRK 抑制剂。
(10)海思科克利加巴林拟纳入优先审评
5月9日,CDE网站显示,海思科的克利加巴林(HSK16149)拟纳入优先审评,用于神经病理性疼痛。
克利加巴林是一款抑制性神经递质γ-氨基丁酸(GABA)的结构衍生物,可以与钙离子通道α2δ亚受体结合,具备高靶点选择性、强效镇痛、长效镇痛、中枢副作用小等特点,对中至重度患者疗效可能更佳。
临床前研究表明,克利加巴林具有强效镇痛、长效镇痛、中枢副作用小等特点,有望替代普瑞巴林、加巴喷丁,具有成为慢性神经性疼痛首选用药的潜力。
2024年5月,克利加巴林胶囊(商品名:思美宁)首次获得国家药监局(NMPA)批准上市,用于治疗成人糖尿病性周围神经病理性疼痛。同年7月,第二项适应症获批,用于治疗成人糖尿病性周围神经病理性疼痛和带状疱疹后神经痛。
1.4.2 本周全球TOP10积极/失败临床结果
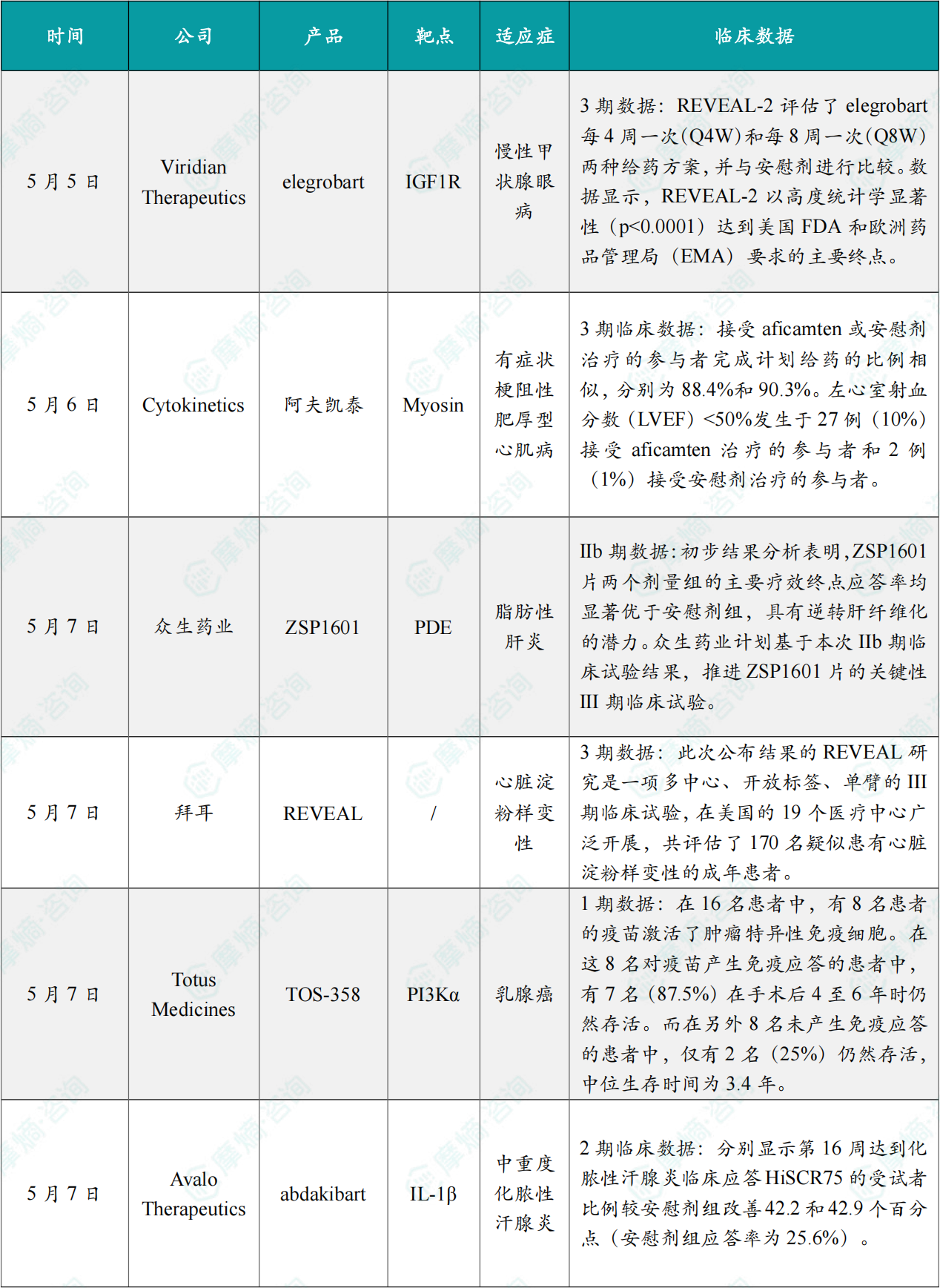
(1)Viridian Therapeutics公司宣布,elegrobart治疗慢性甲状腺眼病3期临床结果积极
5月5日,Viridian Therapeutics公司宣布,在研疗法elegrobart用于治疗慢性甲状腺眼病(TED)患者的REVEAL-2 3期临床试验取得积极顶线数据。
Elegrobart是一款通过皮下注射给药、半衰期延长的单克隆抗体,靶向胰岛素样生长因子-1受体(IGF-1R)。REVEAL-2评估了elegrobart每4周一次(Q4W)和每8周一次(Q8W)两种给药方案,并与安慰剂进行比较。
数据显示,REVEAL-2以高度统计学显著性(p<0.0001)达到美国FDA和欧洲药品管理局(EMA)要求的主要终点。此外,在Q4W和Q8W治疗组中,REVEAL-2均以高度统计学显著性达到所有眼球突出关键次要终点;Q4W治疗组在第24周显示出具有统计学显著性的复视应答率。
(2)Cytokinetics公司宣布3期临床试验ACACIA-HCM取得积极顶线结果
Cytokinetics公司今日宣布,关键性3期临床试验ACACIA-HCM取得积极顶线结果。数据显示,ACACIA-HCM达到双重主要终点,与安慰剂相比,从基线至第36周,在堪萨斯城心肌病调查问卷临床汇总评分(KCCQ-CSS)和最大运动能力(pVO2)方面均取得具有统计学显著性的改善。安全性方面,未发现新的安全性信号。接受aficamten或安慰剂治疗的参与者完成计划给药的比例相似,分别为88.4%和90.3%。左心室射血分数(LVEF)<50%发生于27例(10%)接受aficamten治疗的参与者和2例(1%)接受安慰剂治疗的参与者。2例接受aficamten治疗的参与者发生了与LVEF<50%相关的心力衰竭严重不良事件。接受aficamten治疗的参与者中,3%因LVEF<40%而中断治疗。
(3)众生药业宣布ZSP1601片的IIb期临床试验达到主要终点
5月7日,众生药业宣布ZSP1601片治疗代谢功能障碍相关脂肪性肝炎(MASH)的IIb期临床试验达到主要终点。
初步结果分析表明,ZSP1601片两个剂量组的主要疗效终点应答率均显著优于安慰剂组,具有逆转肝纤维化的潜力。众生药业计划基于本次IIb期临床试验结果,推进ZSP1601片的关键性III期临床试验。
ZSP1601是一款磷酸二酯酶(PDE)抑制剂,为国家重大新药创制项目。治疗48周后,100mg组、50mg组和安慰剂组的应答率分别为64.9%、57.6%和32.5%,与安慰剂组的率差分别为31.85%和27.37%。
(4)拜耳放射性示踪剂临床III期成功
5月7日,拜耳(Bayer)宣布REVEAL III期临床研究取得了积极的顶线数据。该研究主要评估的在研PET/CT放射性示踪剂I 124 evuzamitide(又称AT-01),在诊断心脏淀粉样变性方面,基于视觉扫描解释,成功达到了敏感性(识别患病个体的能力)和特异性(识别未患病个体的能力)的主要终点。
此次公布结果的REVEAL研究是一项多中心、开放标签、单臂的III期临床试验,在美国的19个医疗中心广泛开展,共评估了170名疑似患有心脏淀粉样变性的成年患者。
(5)Totus Medicines公布了TOS-358的1b期临床试验中期数据
5月7日,Totus Medicines在欧洲肿瘤内科学会(ESMO)乳腺癌年会上公布了其在研疗法TOS-358的1b期临床试验中期数据。TOS-358是一款下一代泛突变、共价、α选择性PI3Kα抑制剂。
TOS-358-001是一项正在进行的开放标签、全球多中心1期研究。10例可评估HR阳性、HER2阴性乳腺癌患者接受TOS-358联合fulvestrant治疗(中位既往治疗线数为3.5线)。接受TOS-358+fulvestrant治疗的女性患者疾病控制率(DCR)为100%。女性患者临床获益率(CBR)为89%,其中包括既往接受过PI3K/AKT/mTOR(PAM)靶向治疗的患者,以及接受四线及以后治疗的患者。应答随时间推移持续加深,包括从疾病稳定(SD)转化为部分缓解(PR),与TOS-358对PI3Kα信号传导的近乎完全抑制一致。
(6)Avalo Therapeutics宣布,其abdakibart的2期试验取得积极结果
5月7日,Avalo Therapeutics今日宣布,其评估abdakibart用于治疗中重度化脓性汗腺炎(HS)成人患者的2期LOTUS试验取得积极顶线结果。2期LOTUS试验在所研究的两个剂量组均成功达到主要终点(150 mg组,p=0.018;300 mg组,p=0.015;合并分析p=0.004),分别显示第16周达到化脓性汗腺炎临床应答HiSCR75的受试者比例较安慰剂组改善42.2和42.9个百分点(安慰剂组应答率为25.6%)。
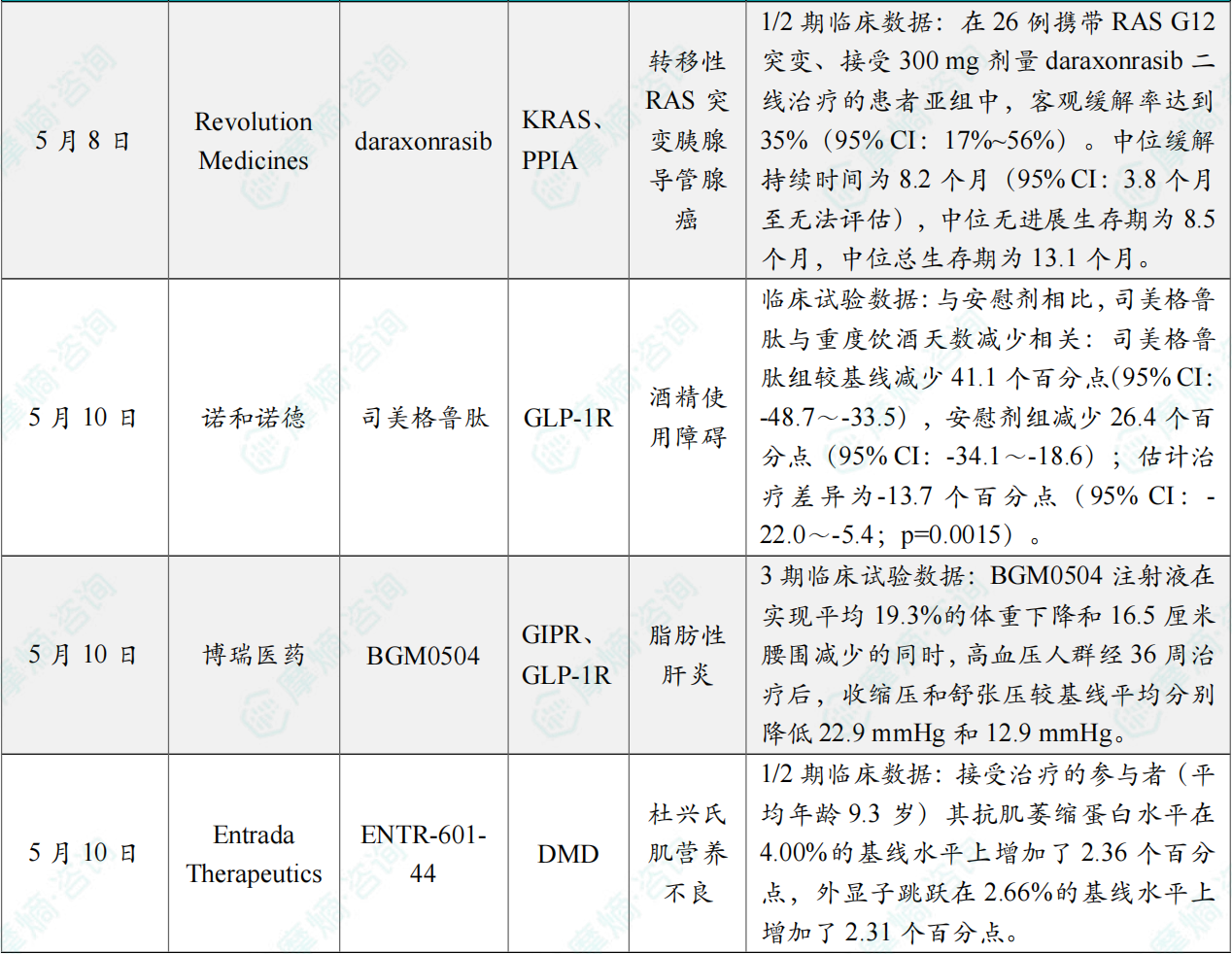
(7)Revolution Medicines公司宣布在研RAS抑制剂daraxonrasib1/2期临床试验数据果
5月8日,Revolution Medicines公司日前宣布,著名医学期刊《新英格兰医学杂志》(NEJM)已发表一份报告,介绍了在研RAS抑制剂daraxonrasib在既往接受过治疗的转移性RAS突变胰腺导管腺癌(PDAC)患者中的1/2期临床试验数据。
试验数据显示,在26例携带RAS G12突变、接受300 mg剂量daraxonrasib二线治疗的患者亚组中,客观缓解率达到35%(95% CI:17%~56%)。中位缓解持续时间为8.2个月(95% CI:3.8个月至无法评估),中位无进展生存期为8.5个月,中位总生存期为13.1个月。在38例携带RAS G12、G13或Q61突变的患者中,29%的患者达到客观缓解(95% CI:15%~46%)。中位缓解持续时间为8.2个月(95% CI:3.8个月至8.8个月),中位无进展生存期为8.1个月,中位总生存期为15.6个月。
(8)诺和诺德发表司美格鲁肽治疗酒精使用障碍患者的临床试验结果
5月10日,诺和诺德发表司美格鲁肽治疗酒精使用障碍患者的临床试验结果。临床试验共入组108名参与者(53名女性和55名男性),司美格鲁肽组和安慰剂组各54名,所有参与者均纳入数据分析。总体而言,88名参与者(81%)完成了完整干预。
试验结果显示,与安慰剂相比,司美格鲁肽与重度饮酒天数减少相关:司美格鲁肽组较基线减少41.1个百分点(95% CI:-48.7~-33.5),安慰剂组减少26.4个百分点(95% CI:-34.1~-18.6);估计治疗差异为-13.7个百分点(95% CI:-22.0~-5.4;p=0.0015)。不良事件大多为一过性,通常为轻度至中度胃肠道反应,且在司美格鲁肽组发生更为频繁。
(9)博瑞医药宣布其药物BGM0504注射液的3期临床试验取得积极结果
5月10日,博瑞医药宣布,其候选药物BGM0504注射液用于治疗超重或肥胖受试者的3期临床试验取得了积极的顶线结果。此次公布结果的3期临床研究达成主要终点和所有关键次要终点。
数据显示,BGM0504注射液在实现平均19.3%的体重下降和16.5厘米腰围减少的同时,高血压人群经36周治疗后,收缩压和舒张压较基线平均分别降低22.9 mmHg和12.9 mmHg。同时,受试者尿酸平均降低70.7 μmol/L,全身骨密度、腰椎骨密度、髋关节骨密度分别增加0.3%、1.4%和3.9%,血脂、血糖等其他心血管代谢指标方面也呈现出综合改善能力。此外,BGM0504注射液的整体安全性和耐受性良好,治疗52周各剂量组因不良事件导致的终止治疗比例分别为1.7%、1.2%和0.7%。
(10)Entrada Therapeutics公司公布其1/2期临床研究ELEVATE-44-201的数据
5月10日,Entrada Therapeutics公司公布了其1/2期临床研究ELEVATE-44-201队列1的最新顶线数据。该研究旨在评估在研药物ENTR-601-44在4至20岁、适合外显子44跳跃疗法的杜氏肌营养不良患者中的表现。
此次公布的队列1结果显示,ENTR-601-44具有良好的安全性和耐受性,未报告严重不良事件,也未发生因不良事件导致的停药,且估算肾小球滤过率(eGFR)、胱抑素C和镁等肾功能指标均在正常范围内。疗效方面,接受治疗的参与者(平均年龄9.3岁)其抗肌萎缩蛋白水平在4.00%的基线水平上增加了2.36个百分点,外显子跳跃在2.66%的基线水平上增加了2.31个百分点。与安慰剂组相比,治疗组在“起身速率”(time to rise velocity)这一经临床验证的功能性指标上,展现出具有统计学意义且具备潜在差异化优势的改善。
同期事件:
1. 2026年第19周05.04-05.10国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第19周05.04-05.10国内仿制药/生物类似物申报/审批数据分析
3. 2026年第19周05.04-05.10国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.05.04-2026.05.10) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论