
2026年4月22日,国家药品监督管理局发布2026年第40号公告,宣布即日起暂停进口、销售和使用由两家印度企业生产的秋水仙碱原料药。原因为国家药监局在境外现场检查中,发现其生产过程存在严重违反《药品生产质量管理规范》的问题。

截图来源:NMPA官网
一、涉事企业与产品详情:均为知名天然药物原料生产商
本次被采取监管措施的具体企业与产品信息如下:
- Alkaloids Bioactives Private Limited:其登记的秋水仙碱原料药(登记号:Y20190009002)被暂停。该公司位于印度特伦甘纳邦,隶属于1967年成立的Alkaloids Corporation集团,前身为Alkaloids Pvt Ltd,是一家专注于植物源原料药与天然提取物生产的企业。
- Alchem International Private Ltd:其登记的三批秋水仙碱原料药(登记号:Y20190009011、Y20190009012、Y20190009013)被暂停。该公司是印度哈里亚纳邦一家成立于1935年的老牌植物化学品企业,拥有超过75年行业经验,主营天然来源原料药、保健品及化妆品原料,产品获WHO、美国FDA等多国认证,并出口至全球约35个国家。
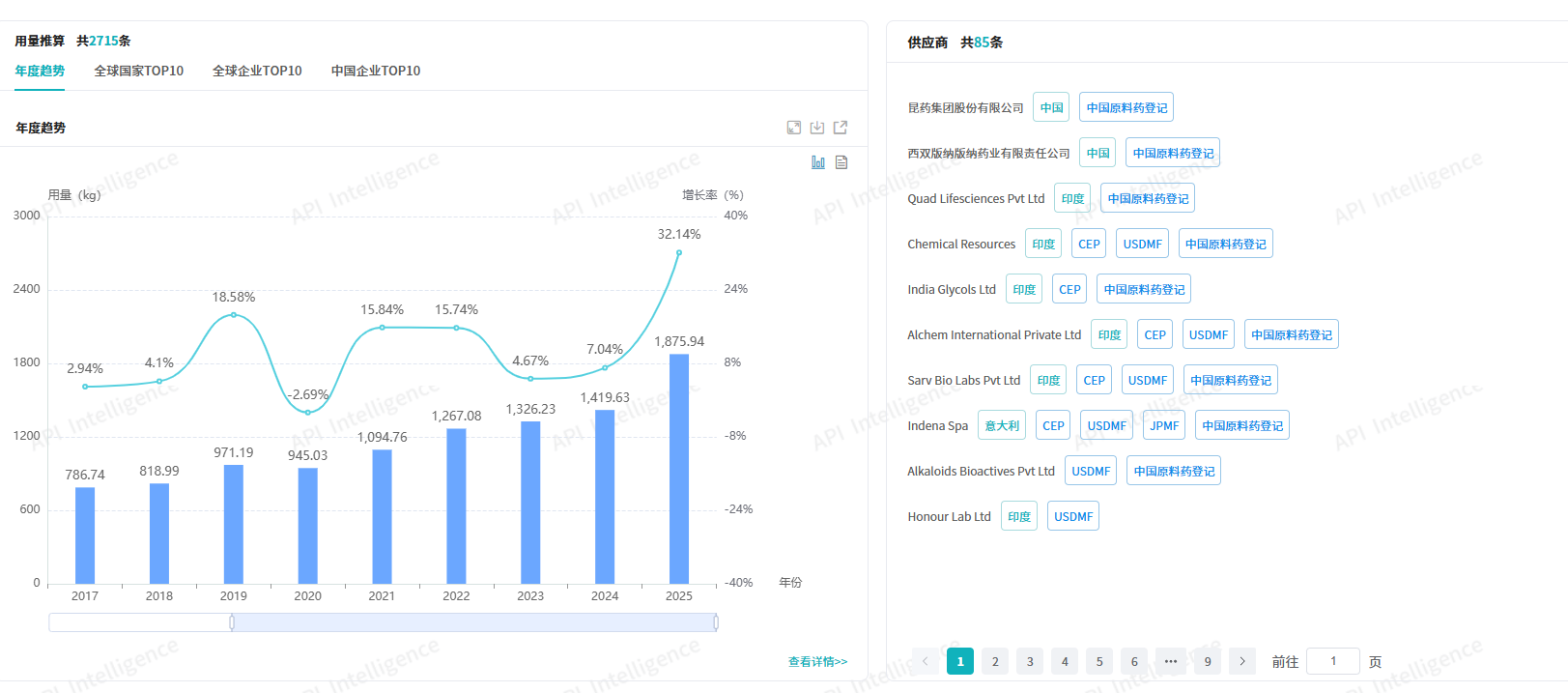
查数据,找摩熵!图源:摩熵医药数据库
二、违规核心:擅自变更工艺,质量管理体系存在严重缺陷
根据国家药监局公告,检查发现两家企业主要存在以下严重问题:
1. 违规实施工艺变更:在未按照中国相关规定获得批准或完成备案的情况下,擅自对生产工艺进行了变更。
2. 质量管理体系不合规:企业的质量管理体系未能满足我国《药品生产质量管理规范(2010年修订)》的相关要求。
基于上述发现,依据《中华人民共和国药品管理法》及《药品医疗器械境外检查管理规定》等法规,国家药监局作出以下决定:
- 暂停进口上述原料药,各口岸药监部门暂停发放进口通关单。
- 将上述原料药在药品审评中心的登记状态调整为“I”(未通过与制剂共同审评审批)。
- 禁止上述原料药在境内销售及用于制剂生产,相关已生产制剂不得放行;已上市制剂,持有人须立即开展评估并采取风险控制措施。
三、年内二度被查,监管持续收紧,供应链面临切换压力
值得注意的是,这已是Alchem International公司今年以来第二次因同类问题被中国监管暂停进口。就在2026年3月24日,该公司生产的利血平、地高辛原料药也因类似违规问题被采取了相同措施。
监管部门的连续出手,清晰传递出对境内外原料药实施统一、最严格监管的决心,坚决防止不合规原料进入我国药品供应链。
秋水仙碱是治疗急性痛风、家族性地中海热等疾病的关键药物。此次暂停进口预计将对国内相关药品制剂的原料供应产生直接影响。相关药品上市许可持有人及制剂生产企业需立即启动供应链评估,尽快寻找并切换至符合中国GMP要求的合规原料药供应商,以保障药品的正常生产和市场供应。
参考来源:
[1] NMPA官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 国家药监局急刹!印度产阿尔茨海默一线药、感冒药原料被暂停进口,用药安全再拉警报
2. 2025年药监局审评加严:551条仿制药受理号被拒,这些品种为何集体“折戟”?
3. 国家药监局严审:118个品种上市申请被否,13款首仿折戟!九典、东阳光药布局受挫引深思
查数据,找摩熵!想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论