
4月23日,再生元宣布美国FDA加速批准其在研基因疗法Otarmeni(lunsotogene parvec))上市。该疗法成为首个也是目前唯一获批用于治疗遗传性听力损失的基因疗法,同时也是再生元首个获得批准的基因疗法。

再生元表示,将向美国患者免费提供这款基因疗法,不收取任何费用。Otarmeni是首个通过FDA局长国家优先审评券试点项目(CNPV)批准的基因疗法,也是第二个通过 CNPV 获批的新分子实体。
一、OTOF基因突变听力损失有救,Otarmeni实现持续性生理听力恢复
OTOF基因突变引起的听力损失是一种极其罕见的疾病,在美国每年仅有约 50名新生儿受到影响。尽管耳内所有结构完整,但OTOF基因的变异会导致功能性耳蛋白(Otoferlin)缺失,这种蛋白对于内耳感觉细胞与听神经之间的信息传递至关重要。
过去,OTOF基因突变引起的遗传性听力损失被认为是永久性的,患者需终身佩戴助听设备。这些设备虽可放大声音,但无法恢复全部频谱的自然听觉。
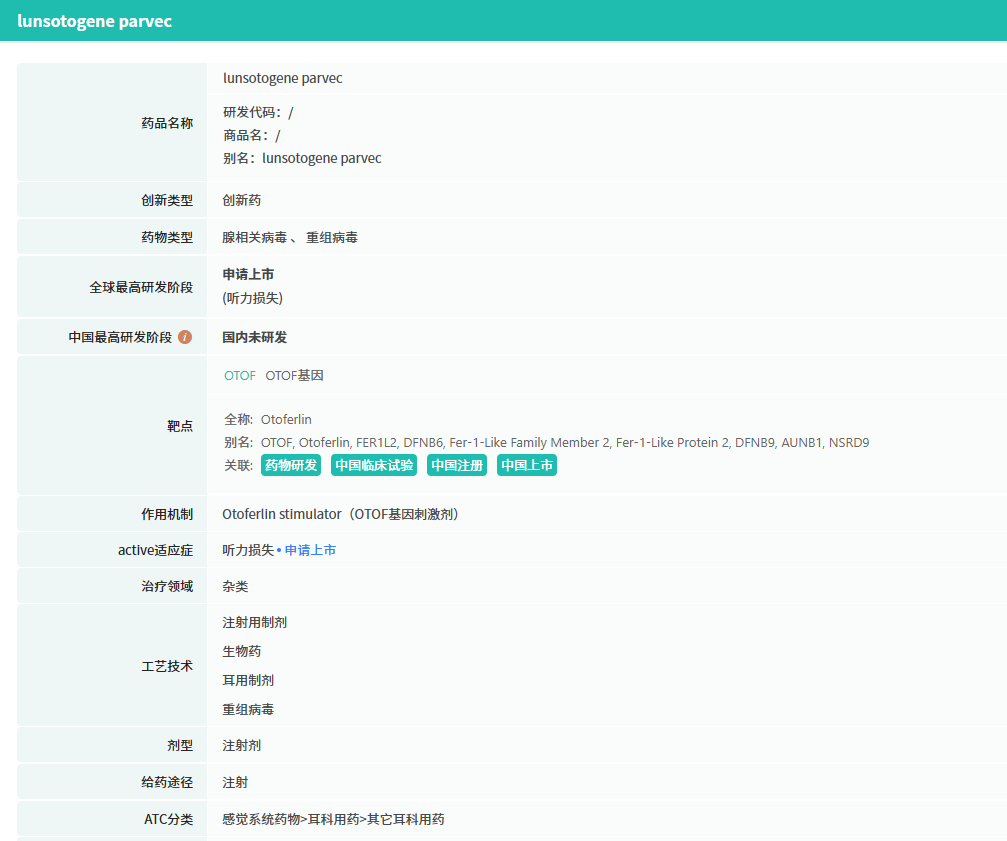
查数据,找摩熵!图源:摩熵医药数据库-中国药品审评数据库
Otarmeni是一种基于腺相关病毒载体的基因疗法,适用于因OTOF基因变异导致重度以上感音神经性听力损失的儿童与成人。该疗法旨在通过修饰后的非致病性病毒,将正常的OTOF基因拷贝递送至耳蜗,从而恢复患者持续性生理听力。
二、关键试验结果:八成受试者实现“自然听力”,四成听力恢复正常
FDA 的批准基于关键性 CHORD 试验的结果。该试验中,20 名10个月至16岁的受试者接受单剂量Otarmeni耳蜗内输注,其中10名单侧(单耳)输注,10名双侧(双耳)输注。
试验主要结果显示:
- 80%(16/20)受试者在 24 周时纯音测听阈值≤70 dB HL,达到试验主要终点;另有一名受试者在第 48 周达到该阈值。该阈值符合临床“自然听力”标准,通常可免于人工耳蜗植入。
- 70%(14/20)受试者在 24 周时听觉脑干反应(ABR)≤90 分贝,达到关键次要终点。ABR 为客观听力功能确认方法。
- 在完成 48 周随访的患者中,所有先前有效者均维持治疗反应,42% 的参与者(5/12)听力恢复正常,可听清耳语(≤25 dB HL)。
在安全性方面,CHORD 研究安全人群(n=24)中,与Otarmeni相关的最常见不良反应(≥5%)包括中耳炎、呕吐、恶心、眩晕、手术疼痛、步态障碍和眼球震颤。其植入手术方法与人工耳蜗类似,可用于低龄婴幼儿。
三、再生元“以价换量”:免费提供基因疗法,未来药物价格与海外看齐
值得关注的是,再生元在宣布基因疗法获批的同一日,与美国政府达成一项关于药品定价的重要协议。
根据协议,再生元将依据其他发达国家的药品价格,降低其在美国医疗补助计划(Medicaid)中的多款现有及未来重要药物的价格,并承诺未来在美药品价格与这些发达国家保持一致。
此外,再生元还将通过 TrumpRx.gov 平台,让符合条件的患者以最惠国价格直接购买其PCSK9抑制剂 Praluent(Alirocumab)。该公司再次明确,将在美国免费提供其基因疗法Otarmeni。
作为协议的一部分,再生元将获得为期三年的关税减免,且不再受未来联邦定价指令约束。再生元承诺在未来几年内投资超过900亿美元,用于支持其在美国的研发与生产基础设施建设。
结语
从“无法治愈”到“听力恢复”,Otarmeni的获批不仅标志着遗传性耳聋治疗进入基因时代,更揭示出在遗传性听力损失的基因疗法领域,突破性疗法正从科学探索走向临床可及。
参考来源:
[1] 企业官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 全球首个AFRS靶向药获批!赛诺菲/再生元的度普利尤单抗斩获FDA新适应症,稳坐自免“药王”宝座
2. 再生元DB-OTO基因疗法新突破:CHORD试验成效显著,听力损失治疗迎新篇
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论