
2026年4月27日,诺华宣布,欧盟委员会(EC)正式批准其重磅新药Rhapsido®(remibrutinib)上市,用于治疗对H1抗组胺药应答不佳的成人慢性自发性荨麻疹患者。

作为全球首款获批用于CSU的口服靶向药物,其“每日两次、无需监测”的便捷方案,正在重塑这一顽固性皮肤病的治疗格局。
一、填补巨大未满足需求,改写国际指南
慢性自发性荨麻疹是一种以反复发作的瘙痒性风团和血管性水肿为特征的疾病,全球患者约4000万。在20-40岁人群中高发,且女性患者人数约为男性的两倍。尽管传统的抗组胺药是标准一线疗法,但超过50%的患者症状仍无法得到有效控制,长期承受着剧烈的瘙痒、皮损和与之相关的焦虑、抑郁与睡眠障碍,临床存在巨大的治疗缺口。
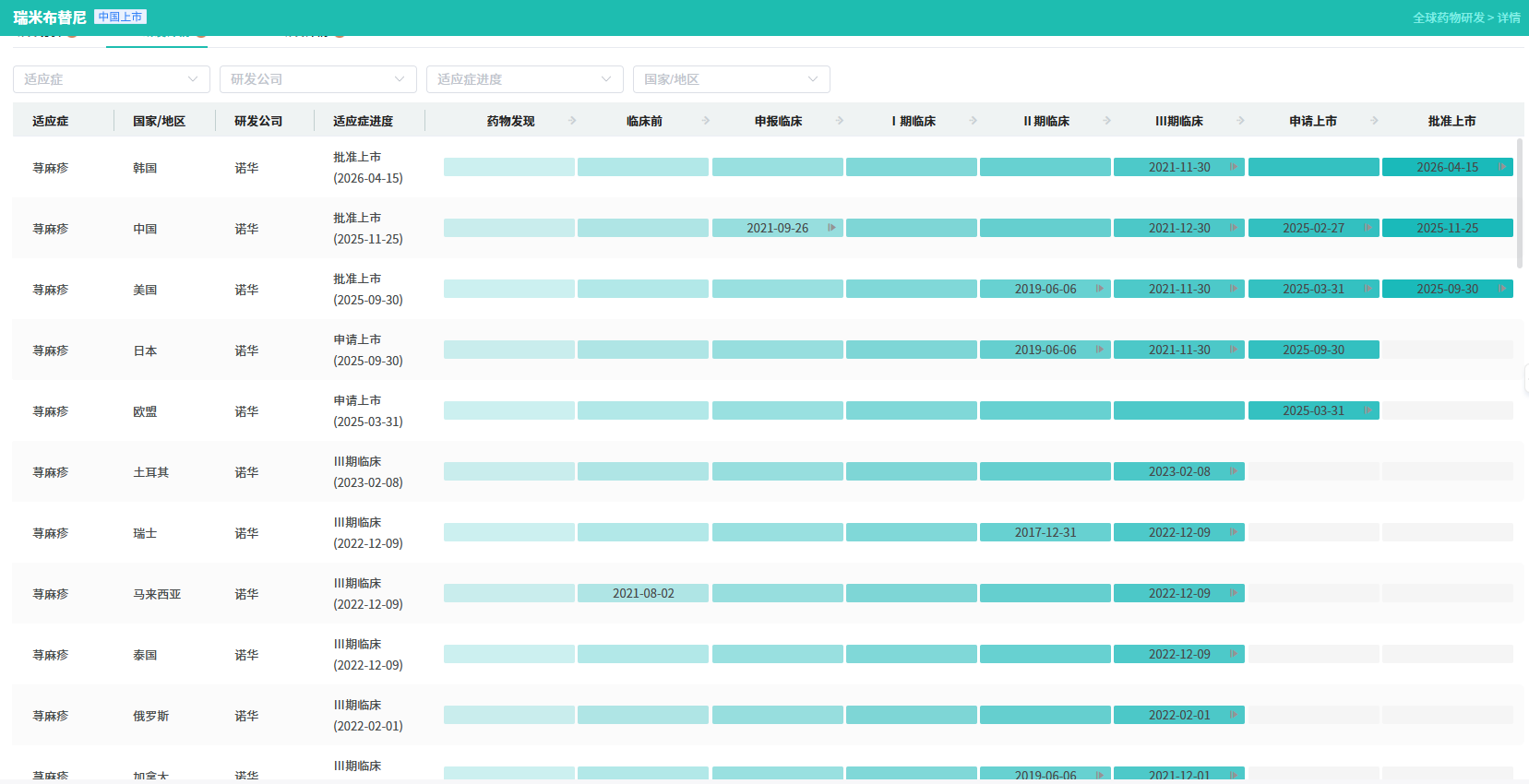
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
Rhapsido®的获批,源自一系列坚实的证据。2026年2月,欧洲药品管理局人用药品委员会(CHMP)已给出积极审评意见。更具里程碑意义的是,该药物被正式纳入了2026年更新的国际荨麻疹诊疗指南,被推荐用于所有经抗组胺药治疗后仍有症状的患者,确立了其在二线治疗中的核心地位。
二、精准狙击BTK通路,一周起效无需监测
Remibrutinib是一种高选择性、强效的口服布鲁顿酪氨酸激酶抑制剂。BTK是肥大细胞和嗜碱性粒细胞内信号传导的关键分子,其活化最终导致组胺等炎性介质的释放,引发荨麻疹症状。Rhapsido®通过精准阻断该通路,从源头上抑制了核心致病环节。
其疗效与安全性在全球III期临床研究(REMIX-1和REMIX-2)中得到证实。这两项全球性、随机、双盲、安慰剂对照研究共纳入925名患者。结果显示:
- 疗效卓越:治疗第12周,在改善瘙痒、风团和每周荨麻疹活动度方面,Rhapsido®显著优于安慰剂。
- 快速起效:患者早在治疗第1周即可观察到症状的显著改善。
- 安全性良好:该药展现了已验证的安全性特征,研究中未发现肝脏安全问题,且治疗全程无需常规实验室监测,极大提升了用药便捷性。最常见不良反应(发生率≥3%)包括鼻咽炎、出血、头痛、恶心和腹痛。
三、全球布局与管线拓展,构建免疫赛道新王牌
Rhapsido®的获批,只是诺华在该分子上全球布局的开端。目前,remibrutinib(拟用于治疗荨麻疹)于2025年9月30日在美国率先上市,随后于2025年11月25日在中国获批,并于2026年4月15日在韩国上市。
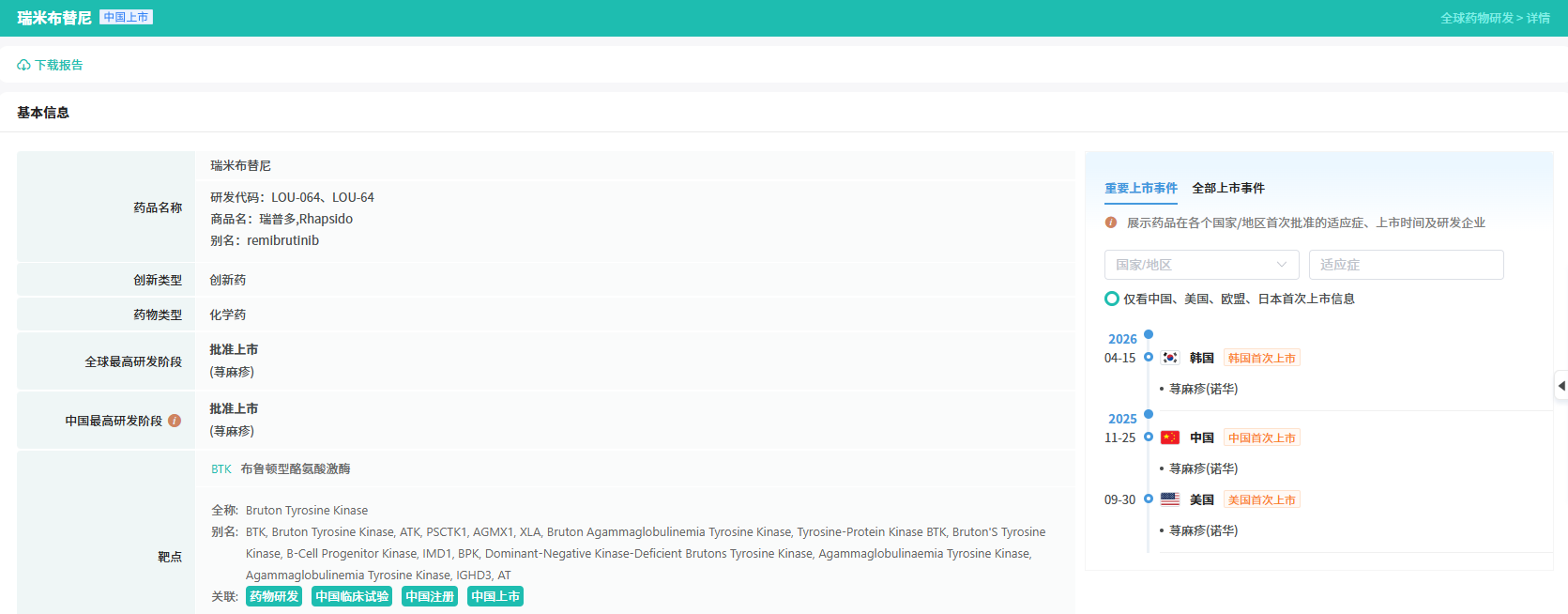
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
更重要的是,其应用边界正在快速扩展,有望成为诺华在免疫学领域的又一核心产品:
- 横向拓展:针对慢性诱导性荨麻疹三种最常见亚型的关键III期试验(RemIND)已取得积极顶线结果。
- 纵向深入:该药正在化脓性汗腺炎、食物过敏等适应症中进行研究,并有望应用于多发性硬化症等神经系统疾病,展现出广阔的平台潜力。
结语
随着Rhapsido®在欧盟获批,CSU靶向治疗正式迈入口服时代。对于半数以上对抗组胺药应答不佳的患者而言,这一无需监测、口服便捷的新选择,有望显著改善其治疗体验与生活质量。
目前,全球CSU治疗市场仍存在巨大未满足需求,Rhapsido®的获批不仅丰富了临床治疗武器库,也预示着BTK抑制剂在免疫炎症领域拥有更广阔的应用前景。未来,随着其在慢性诱导性荨麻疹、化脓性汗腺炎等更多适应症中取得进展,该药有望惠及更广泛的免疫疾病患者群体,进一步重塑相关疾病的治疗格局。
参考来源:
[1] 企业官网/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 诺华司库奇尤单抗获批儿童化脓性汗腺炎新适应症,IL-17A靶点战场白热化,2025年销售近67亿美元
2. 全球罕见病领域药物研发Top5企业揭秘:诺华“砸钱”扩张与辉瑞“王牌”保卫战
3. 诺华制药转型全景洞察:财务、研发、业务多维度破局与展望
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论