
3月18日,诺华公司宣布,司库奇尤单抗新适应症获得美国 FDA 批准,适用于12岁及以上儿童中重度化脓性汗腺炎(HS)患者的治疗。这标志着这款“药王”级产品的应用人群得到进一步拓宽。

截图来源:企业官微
多适应症拓展,儿科治疗新适应获批
司库奇尤单抗是全球首个获批的全人源白介素(IL)-17A抑制剂,可特异性中和多种来源的IL-17A,从而抑制其在自身免疫性疾病中的核心促炎作用。
据摩熵医药数据库显示,该药自2014年12月在日本实现全球首次获批以来,已相继在美国、欧盟、中国等多个主要市场上市,并陆续拓展了斑块状银屑病、银屑病关节炎、强直性脊柱炎、放射学阴性中轴型脊柱关节炎等多个适应症。
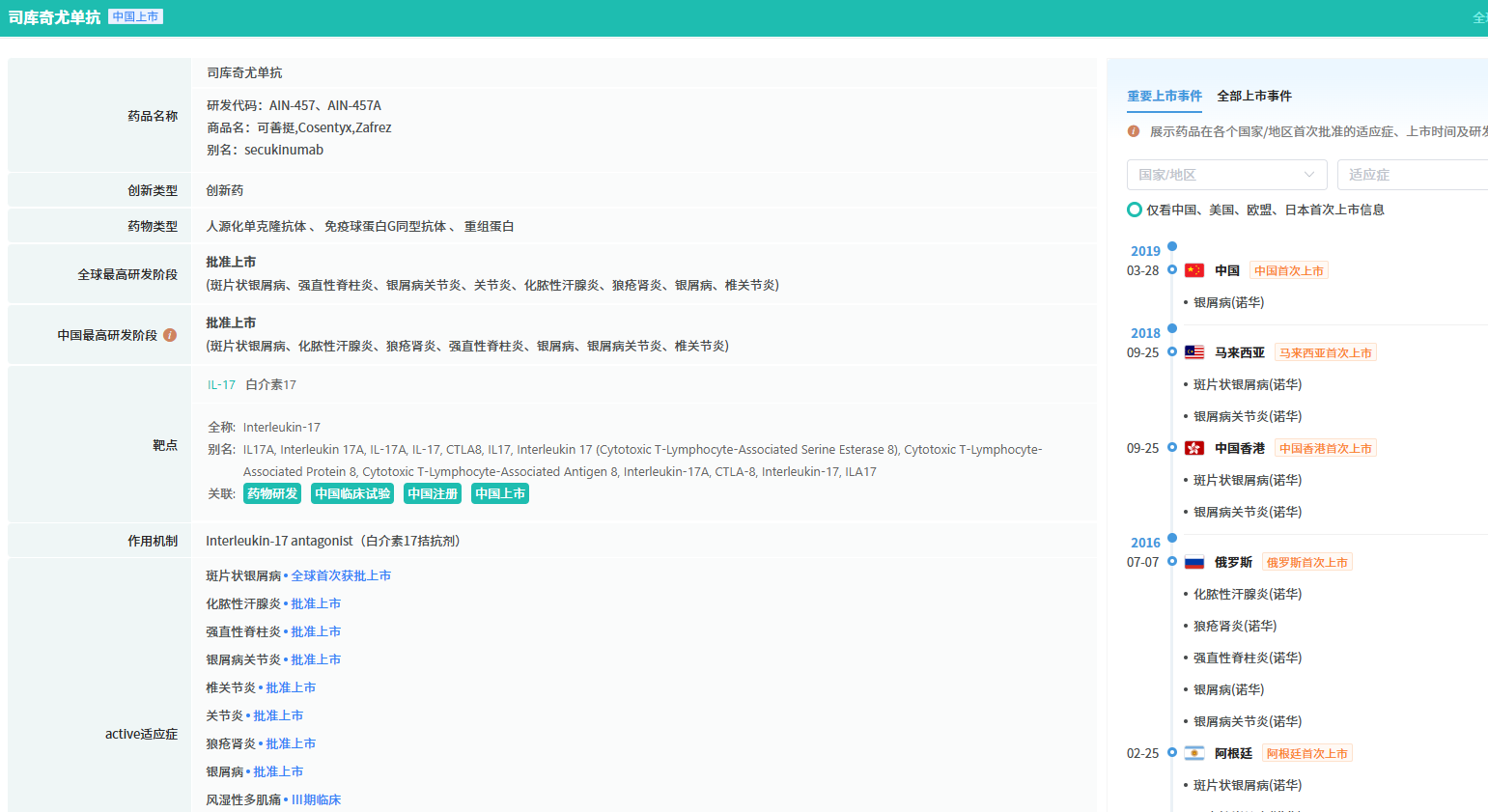
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
本次获批用于12岁及以上、体重超30公斤的中重度HS患者。获批依据包括严谨的成人研究、基于成人HS和银屑病临床试验推断的药代动力学模型,以及其他已获批适应症的儿科临床试验数据,还获剂量分析支持,其预测儿科患者体重剂量调整可获与成人HS患者相似的药物暴露量。
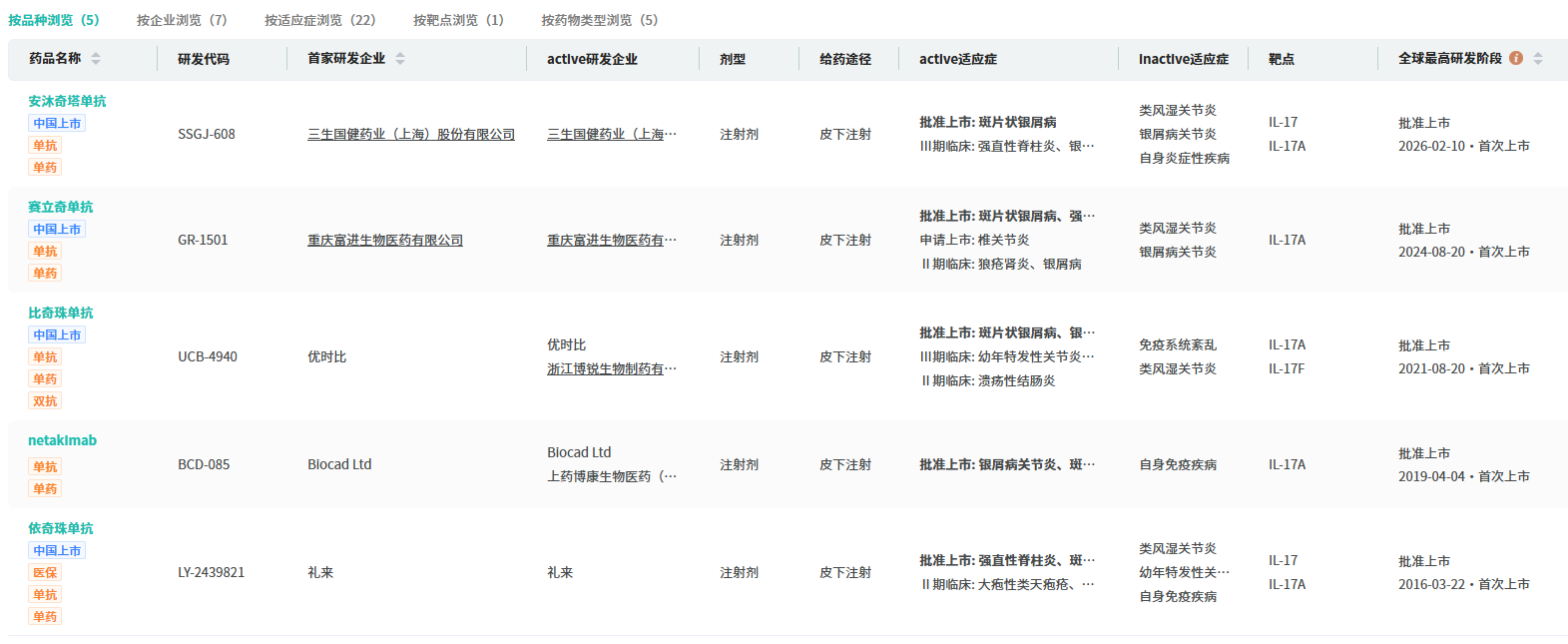
2025年销售近67亿美元,靶点竞争白热化
作为自免领域的超级重磅炸弹,司库奇尤单抗的市场表现持续强劲。根据摩熵医药市场数据显示,该药在上市后迅速放量,2016年全球销售额即达11.28亿美元,至2025年已飙升至66.68亿美元,同比增长8.58%,彰显了IL-17A靶点在自身免疫性疾病治疗中的巨大市场潜力。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论