
4月10日,NMPA 官网显示,阿斯利康的度伐利尤单抗(PD-L1)和曲麦利尤单抗(CTLA4)联合疗法在国内获批上市,用于表皮生长因子受体(EGFR)敏感突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非小细胞肺癌(NSCLC)的一线治疗。

截图来源:NMPA
这不仅是阿斯利康“双免疫治疗”方案在中国落地的首个适应症,也标志着阿斯利康第二款免疫治疗药物曲麦利尤单抗在中国正式获批。
一、曲麦利尤单抗首获国内批准,度伐利尤单抗适应症扩至8项
曲麦利尤单抗是一种人源抗细胞毒性T淋巴细胞相关蛋白 4(CTLA-4)的单克隆抗体,通过阻断 CTLA-4 介导的抑制信号,促进T细胞活化并增强机体的抗肿瘤免疫应答,促进癌细胞死亡。
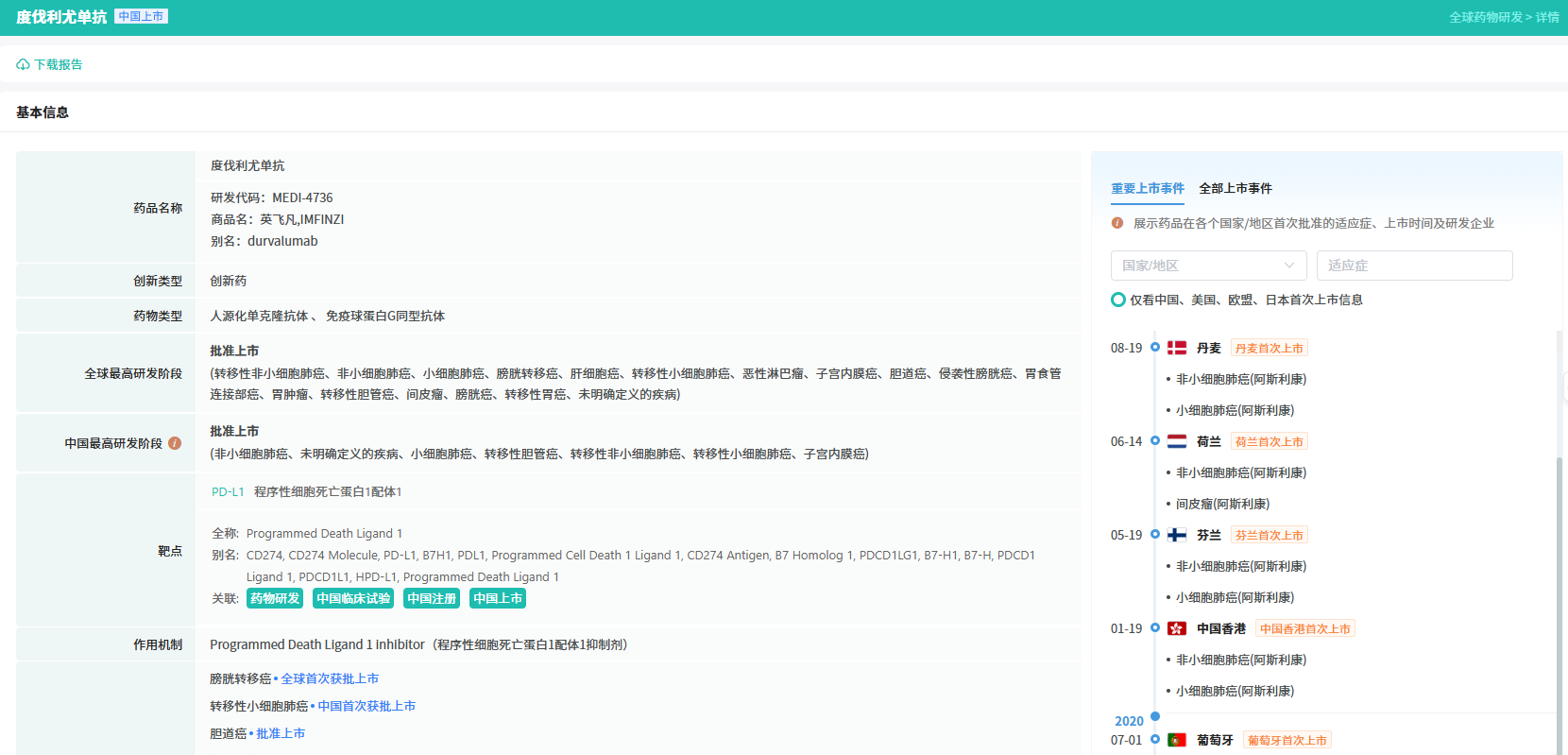
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
据摩熵医药数据库显示,度伐利尤单抗是一种人源PD-L1单克隆抗体,自自2019年在中国上市以来,已获批7项适应症,覆盖肺癌、胆道癌和妇科肿瘤。本次获批是其在国内斩获的第8项适应症,同时也是曲麦利尤单抗首次在国内获批。
二、数据力证疗效,POSEIDON研究改写生存曲线
此次NMPA的批准决定主要基于III期临床研究POSEIDON的惊艳数据。该研究不仅验证了疗效,更确立了“短疗程”联合的安全优势。
显著生存获益:与单独化疗相比,接受曲麦利尤单抗(5个周期)+ 度伐利尤单抗 + 含铂化疗的患者,死亡风险降低了23%(HR 0.77; p=0.00304)。联合组中位总生存期(OS)达到14.0个月,显著优于化疗组的11.7个月;2年OS率分别为33% vs 22%。
强效控疾:该联合方案将疾病进展或死亡风险显著降低28%(HR 0.72; p=0.00031)。
长拖尾效应:在2023年ESMO IO大会上公布的超5年随访数据显示,联合组5年OS率高达15.7%,而单独化疗组仅为6.8%(HR 0.76),这意味着近六分之一的患者实现了临床治愈般的长期生存可能。
此外,该方案未出现新的安全信号,证实了短疗程CTLA-4抑制剂在提升疗效的同时,并未显著增加长期毒副作用,为患者提供了更具耐受性的治疗选择。
三、群雄逐鹿,双抗崛起下的“双免”突围
尽管目前国内已获批的 CTLA-4 × PD-(L)1 双免联合疗法仅有纳武利尤单抗+伊匹木单抗这一项,但在 CTLA-4 单抗单药层面,BMS/小野制药的伊匹木单抗与信达生物的伊匹木单抗 N01 早已先行一步。随着阿斯利康曲麦利尤单抗的获批,国内 CTLA-4 靶点单抗增至 3 款,同时也让“双免联合”从“一枝独秀”走向“双雄并立”。
然而,市场竞争远不止于此。随着生物技术的迭代,双特异性抗体(双抗)的崛起正对传统联合疗法构成挑战。 目前,康方生物的卡度尼利单抗(PD-1/CTLA-4双抗)已在国内获批宫颈癌及胃癌一线疗法;齐鲁制药的艾帕洛利单抗/托沃瑞利单抗(PD-1/CTLA-4混合抗体)也已在宫颈癌二线获批。这些“一药双靶”的药物在给药便利性上具有天然优势。
但在肺癌这一最大战场,阿斯利康此次凭借POSEIDON研究的扎实数据,证明了“分步联合”策略在肺癌一线治疗中的不可替代性。随着曲麦利尤单抗的加入,阿斯利康在肺癌领域的“免疫+靶向+化疗”全矩阵布局已基本成型。
结语
此次“双免”方案的获批,不仅是阿斯利康在中国市场的一次重要补位,更为驱动基因阴性的晚期非小细胞肺癌患者提供了新的长生存希望。在双抗与双免的博弈中,谁能最终主导肺癌一线治疗格局,仍需更多真实世界数据的验证。
参考来源:
[1] NMPA官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 阿斯利康罕见病管线迎突破!新型酶替代疗法efzimfotase alfa三项Ⅲ期研究达终点
2. 中国首个TSLP单抗获批!阿斯利康/安进重磅药特泽利尤单抗抢滩哮喘与慢性鼻窦炎伴鼻息肉病市场
3. 阿斯利康PD-L1单抗度伐利尤单抗成欧盟唯一获批胃癌/胃食管癌围手术期免疫治疗新选择
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论