1.4.1 本周全球TOP10创新药研发进展
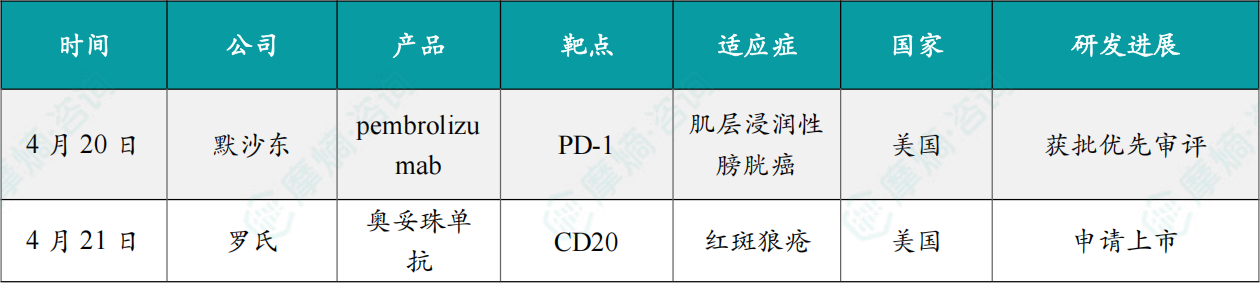
(1)Keytruda/ADC组合疗法获美国FDA受理并授予优先审评资格
4月20日,默沙东(MSD)宣布,美国FDA已受理其两项补充生物制品许可申请(sBLA),并授予优先审评资格。此次申请涉及抗PD-1疗法Keytruda(pembrolizumab)静脉输注制剂,以及Keytruda Qlex(pembrolizumab和berahyaluronidase alfa)皮下注射制剂。上述两种方案均拟联合辉瑞(Pfizer)和安斯泰来(Astellas)共同开发的抗体偶联药物(ADC)Padcev(enfortumab vedotin),用于治疗适合接受顺铂化疗的肌层浸润性膀胱癌(MIBC)患者。
FDA已将该申请的PDUFA目标审评日期定为2026年8月17日。根据新闻稿,若获批,该联合疗法有望成为首个适用于所有MIBC患者(无论是否适合顺铂治疗)的围手术期治疗选择,并可能成为新的标准治疗方案。此次申报主要基于3期KEYNOTE-B15研究结果。
(2)罗氏奥妥珠单抗新适应症在美国申报上市,治疗系统性红斑狼疮
4月21日,罗氏宣布奥妥珠单抗(Gazyva/Gazyvaro)的补充生物制剂许可证申请(sBLA)获得FDA受理,用于治疗系统性红斑狼疮(SLE)。FDA预计将在2026年12月前作出批准决定。如果获得批准,奥妥珠单抗将成为首个可用于治疗SLE的CD20疗法。
奥妥珠单抗于2013年在美国获批上市,属于第三代Fc段经修饰的II型人源化CD20单抗。目前该药物已获批用于治疗3类血液瘤,包括慢性淋巴细胞白血病、滤泡性淋巴瘤、小淋巴细胞性淋巴瘤,并获批用于治疗狼疮性肾炎。此次sBLA是基于III期ALLEGORY研究的积极结果。结果显示,奥妥珠单抗组有76.7%的患者达到SRI-4,而安慰剂组这一比例为53.5%(调整后差异为23.1%,P<0.001)。
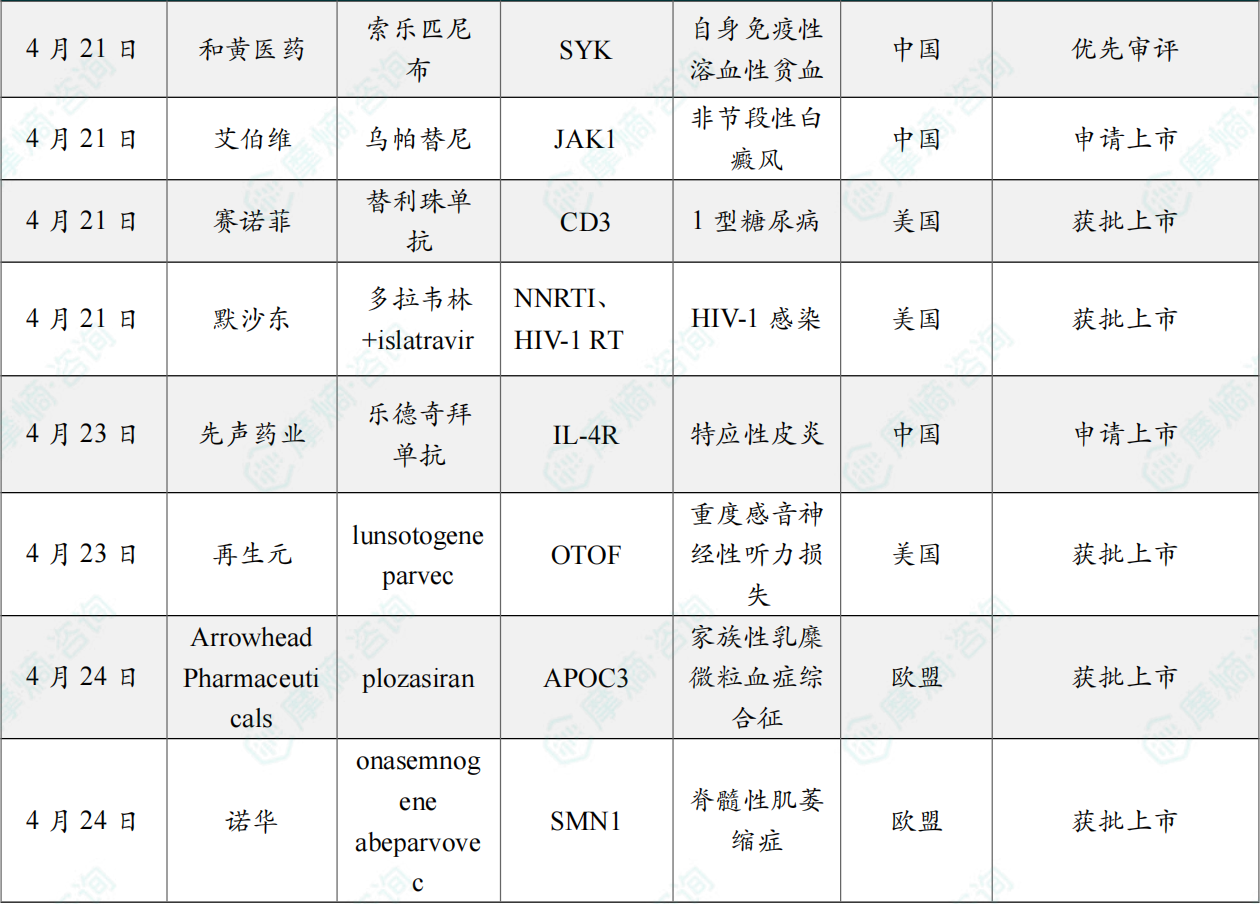
(3)和黄医药1类新药拟纳入优先审评
4月21日,CDE官网显示,和黄医药醋酸索乐匹尼布片的一项新适应症拟纳入优先审评,适用于既往至少对糖皮质激素治疗反应不佳的成人温抗体型自身免疫性溶血性贫血(wAIHA)的患者。
索乐匹尼布是一种新型、研究性的选择性口服小分子 Syk 抑制剂。2026年2月,索乐匹尼布用于治疗免疫性血小板减少症的上市申请获得CDE受理,并被纳入优先审评,这是首个报上市的国产 Syk 抑制剂。
2026年1月7日,和黄医药宣布,索乐匹尼布用于治疗温抗体型自身免疫性溶血性贫血成人患者的 ESLIM-02 研究的 III 期注册阶段取得阳性顶线结果,已达到第5至24周治疗期间持久血红蛋白 (Hb) 应答这一主要终点。
(4)艾伯维乌帕替尼在华申报白癜风适应症
4月21日,CDE官网显示,艾伯维的乌帕替尼申报新适应症。根据注册进展,推测此次申报的适应症为非节段性白癜风。该适应症已在今年3月被CDE纳入优先审评。
乌帕替尼是一种选择性JAK抑制剂,2019年8月,该产品首次获FDA批准上市,是全球首款获批上市的JAK1抑制剂。截止目前,乌帕替尼已获批用于治疗10类疾病,包括特应性皮炎、类风湿关节炎、银屑病关节炎、幼年银屑病关节炎、幼年特发性关节炎、溃疡性结肠炎、克罗恩病、强直性脊柱炎、非放射学中轴型脊柱关节炎和巨细胞动脉炎。
据摩熵医药数据库显示,2025年10月,乌帕替尼(15mg,每日1次)治疗白癜风的两项III期研究达到主要终点。基于此,艾伯维已在美国和欧盟递交乌帕替尼用于治疗青少年和成人非节段性白癜风患者的补充新药申请(sNDA)。
(5)赛诺菲替利珠单抗在美国获批拓展适应症
4月22日,赛诺菲宣布FDA已批准Tzield(替利珠单抗)的补充生物制剂许可申请(sBLA),用于延缓1岁及以上儿童和成人1型糖尿病(T1D)患者从2期进展至3期的速度。经本次批准后,Tzield的适用人群从8岁及以上儿童和成人扩大至1岁及以上儿童和成人。此外,Tzield的第三项适应症正在接受FDA的审查,用于延缓新诊断为3期T1D的8岁及以上儿童和成人患者的进展速度。
替利珠单抗是MacroGenics开发的一款CD3单抗,通过与效应T细胞表面的CD3结合,抑制T细胞对胰岛β细胞的攻击,从而保护胰岛β细胞不受破坏。
2022年10月,赛诺菲与Provention Bio达成合作,获得替利珠单抗的美国商业化权益。同年11月,替利珠单抗在美国获批上市。随后,赛诺菲出手29亿美元并购Provention Bio,获得该产品的所有权益。
(6)默沙东HIV-1新药获FDA批准上市
4月21日,默沙东宣布双药单片制剂 Idvynso(100mg多拉韦林+0.25艾拉曲韦)获得FDA批准上市,用于治疗HIV-1感染成人患者。这些患者在接受稳定抗逆转录病毒药物治疗后病毒复制得到抑制(HIV-1 RNA<50拷贝数/mL),无病毒学治疗失败史,也没有使用已知与多拉韦林耐药相关的替代药物,Idvynso可作为其新的抗逆转录病毒方案。
需要注意的是,Idvynso禁止与强细胞色素P450(CYP)3A酶诱导剂及拉米夫定(3TC)或恩曲他滨(FTC)联用,因为这些药物可能会降低Idvynso的疗效。Idvynso是默沙东开发的一款抗HIV-1感染复方药物,包含固定剂量的多拉韦林和艾拉曲韦。
(7)先声药业将重新递交乐德奇拜单抗上市申请
4月23日,先声药业宣布,出于产品整体商业化布局之战略优化,已主动撤回乐德奇拜单抗的NDA,并预计本月重新递交NDA。先声药业将与监管机构密切沟通,争取早日获准上市。
三期临床研究显示,乐德奇拜单抗不仅起效迅速,且在持续治疗后的累积获益更为显著,呈现与同类产品相比更有效的潜质。第16周,乐德奇拜单抗组EASI-75、EASI-90和IGA 0/1,应答率分别达到74.2%、43.0%和47.7%(p < 0.0001),表明患者在治疗早期即可获得明确的临床获益;至第52周,EASI-75、EASI-90和IGA0/1应答率分别升至96.6%、85.3%和87.1%,显示出持续治疗背景下更为突出的深度缓解优势。
(8)再生元宣布Otarmeni获得FDA加速批准上市
4月23日,再生元宣布Otarmeni(lunsotogene parvec-cwha,DB-OTO)获得FDA加速批准上市,用于治疗存在重度至极重度以及重度感音神经性听力损失(任何频率>90分贝听力水平)的儿童和成人患者。这些患者的听力损失与耳畸蛋白(otoferlin,OTOF,在内毛细胞的囊泡释放和信号转导方面起到重要作用)编码基因出现双等位基因变异相关,外毛细胞功能尚有,且同侧耳无人工耳蜗植入。
该药物是首个可用于治疗OTOF相关听力损失的体内基因疗法,是FDA专员国家优先审查代金券(CNPV)试点计划批准的首个基因疗法,也是该计划批准的第二个新分子实体。并且,再生元将在美国向患者免费提供治疗。(相关扩展阅读:再生元Otarmeni获FDA加速批准,全球首个遗传性耳聋基因疗法在美国免费提供)
(9)Arrowhead Pharmaceuticals宣布欧洲药品管理局人用药品委员会已采纳积极意见建议批准上市
4月24日,Arrowhead Pharmaceuticals宣布,欧洲药品管理局人用药品委员会已采纳积极意见,建议批准Redemplo(plozasiran)上市。该药是一款小干扰RNA(siRNA)药物,拟作为饮食控制的辅助治疗,用于降低家族性乳糜微粒血症综合征(FCS)成年患者的甘油三酯水平。
Redemplo旨在沉默编码载脂蛋白C-III(apoC-III)的mRNA。apoC-III是甘油三酯代谢的关键调节因子,可抑制甘油三酯分解与清除,导致甘油三酯水平升高。携带APOC3功能缺失遗传变异的个体通常具有显著较低的甘油三酯水平,并且动脉粥样硬化性心血管疾病风险更低。CHMP的积极意见基于3期PALISADE研究的临床数据支持。
(10)诺华宣布欧洲药品管理局人用药品委员会已采纳积极意见批准Itvisma上市许可
4月24日,诺华(Novartis)宣布,欧洲药品管理局人用药品委员会已采纳积极意见,建议批准Itvisma(鞘内注射onasemnogene abeparvovec)的上市许可。该意见支持其用于治疗2岁及以上儿童、青少年及成人脊髓性肌萎缩症(SMA)患者,这些患者携带运动神经元生存基因1(SMN1)双等位基因突变。
Itvisma是一种基于腺相关病毒9型载体(AAV9)的基因疗法,采用独特设计,通过一次性鞘内注射递送人SMN1基因的功能性拷贝,从而针对SMA的遗传根源进行治疗,并通过持续表达SMN蛋白改善运动功能。CHMP的积极意见基于注册性STEER研究,以及支持性3b期STRENGTH研究和1/2期STRONG研究的数据。
1.4.2 本周全球TOP10积极/失败临床结果
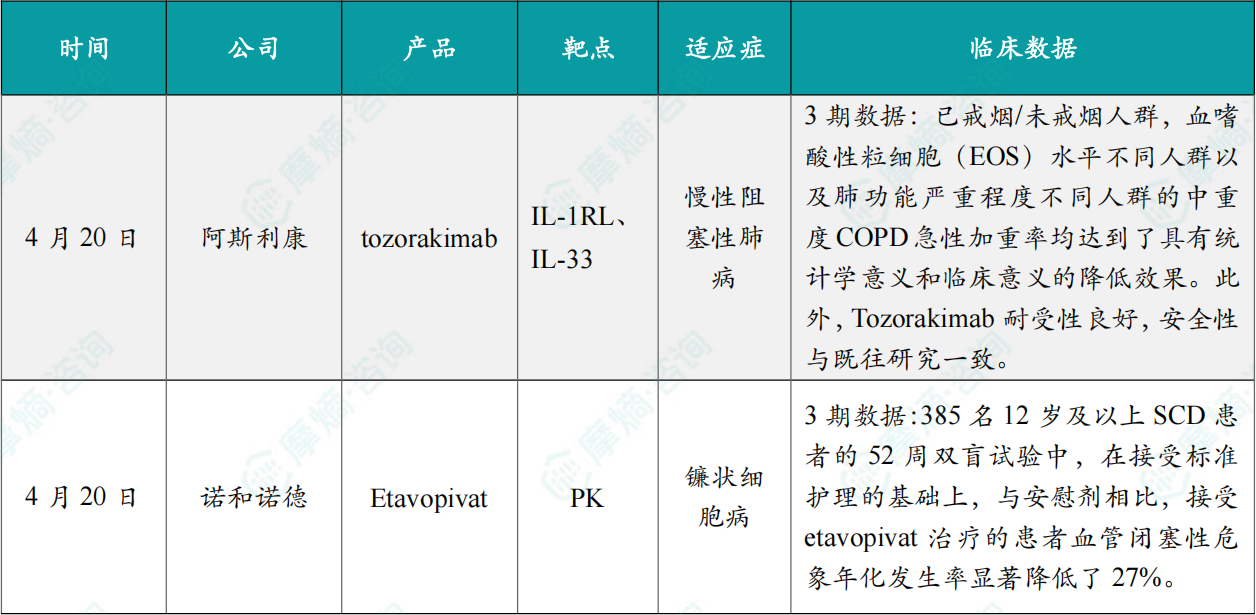
(1)阿斯利康IL-33单抗第3项COPD III期研究成功
4月20日,阿斯利康宣布潜在首创IL-33单抗Tozorakimab治疗慢性阻塞性肺病(COPD)的III期MIRANDA研究取得了高水平积极结果。该研究招募了在接受标准吸入治疗期间仍出现中度至重度加重的COPD患者,评估了Tozorakimab(300mg,每2周1次)的有效性和安全性。
结果显示,已戒烟/未戒烟人群,血嗜酸性粒细胞(EOS)水平不同人群以及肺功能严重程度不同人群的中重度COPD急性加重率均达到了具有统计学意义和临床意义的降低效果。此外,Tozorakimab耐受性良好,安全性与既往研究一致。为评估Tozorakimab在COPD人群中的疗效和安全性,阿斯利康共开展了4项全球注册性III期研究,其它三项为OBERON、TITANIA和PROSPERO,其中前两项已达到主要终点,最后一项预计将在今年上半年读出数据。
(2)诺和诺德同类首创新药III期临床成功,针对镰状细胞病
4月20日,诺和诺德宣布其针对成人和青少年镰状细胞病(SCD)的研究性药物etavopivat在HIBISCUS关键3期临床试验中取得了积极的顶线结果。
作为首个达到双重主要终点的同类首创(first-in-class)新药,Etavopivat是一种每日口服的小分子别构激活剂,专门针对红细胞中的PKR激酶发挥作用。在针对385名12岁及以上SCD患者的52周双盲试验中,在接受标准护理的基础上,与安慰剂相比,接受etavopivat治疗的患者血管闭塞性危象(VOC)年化发生率显著降低了27%。首次发生VOC的时间被大幅延长,中位时间达到了38.4周,而安慰剂组仅为20.9周。在血红蛋白(Hb)响应方面,etavopivat表现出优效性:在治疗24周后,48.7%的患者血红蛋白增加超过1g/dL,远高于安慰剂组的7.2%。作为探索性分析的一部分,该药物还显著降低了患者的输血风险。
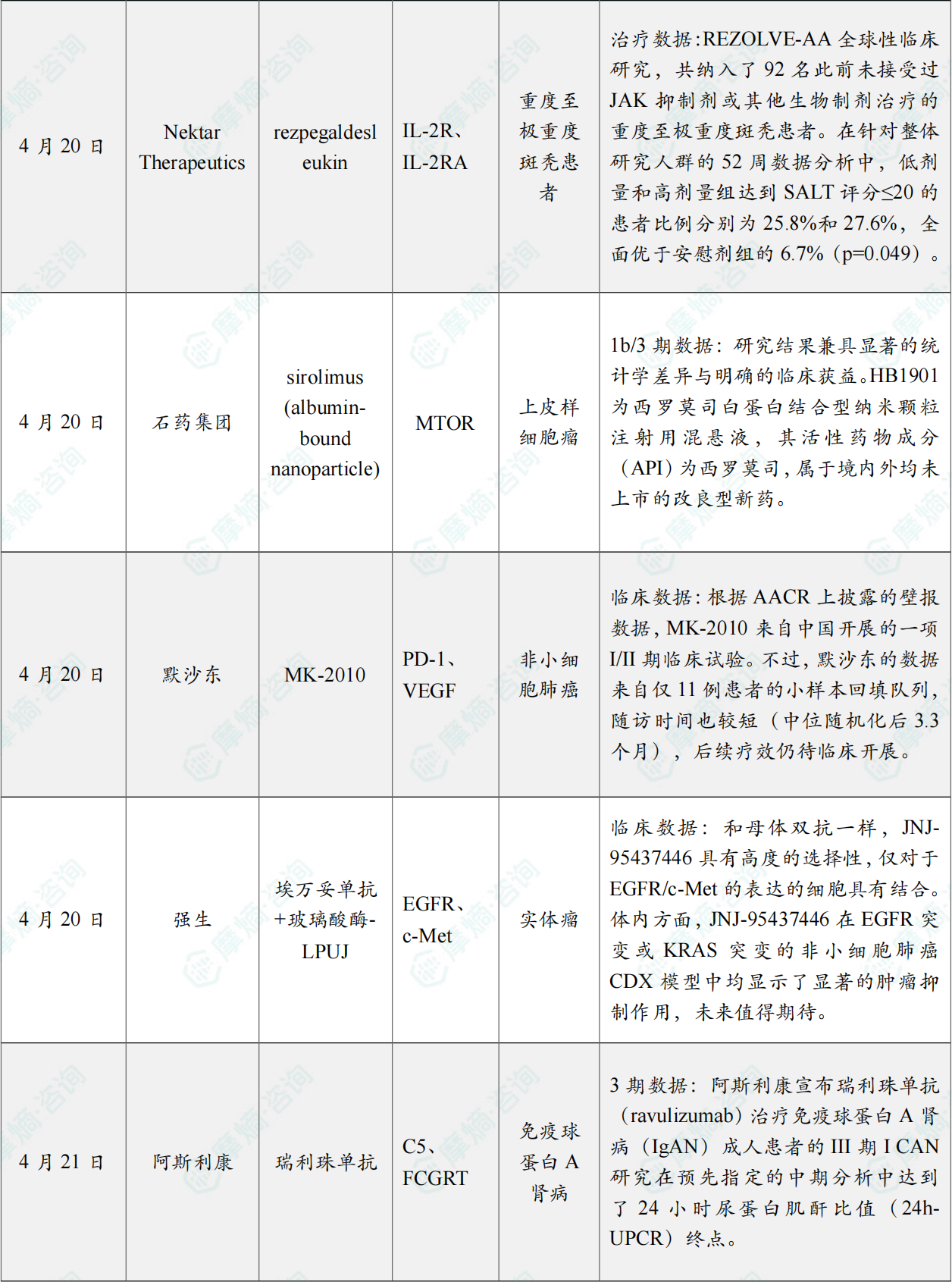
(3)偏向性IL-2治疗脱发成功
4月20日,Nektar Therapeutics公布其针对重度至极重度斑秃患者的Phase 2b期REZOLVE-AA研究在16周盲法延长治疗期后,取得了积极的52周顶线结果。受此消息影响,公司盘前股价大涨17%。
此次公布疗效的主角Rezpegaldesleukin(也被称为REZPEG或NKTR-358),是一种潜在的首创IL-2通路激动剂和调节性T细胞(Treg)生物制剂,偏向性IL-2,经过改造对IL-2Rα的亲和力更高。
凭借其独特的创新机制,该药物在2025年2月和7月分别获得了FDA授予的针对特应性皮炎和重度斑秃(针对成人及体重大于40公斤的12岁以上儿童)的快速通道资格。
REZOLVE-AA全球性临床研究,共纳入了92名此前未接受过JAK抑制剂或其他生物制剂治疗的重度至极重度斑秃患者。在针对整体研究人群的52周数据分析中,低剂量和高剂量组达到SALT评分≤20的患者比例分别为25.8%和27.6%,全面优于安慰剂组的6.7%(p=0.049)。
(4)石药突破性疗法Ib/III期研究成功
4月20日,石药集团宣布其自主开发的注射用西罗莫司(白蛋白结合型)(HB1901)用于治疗晚期恶性血管周围上皮样细胞瘤(PEComa)的Ib/III期临床研究(HB1901-004)已顺利达成预设主要疗效终点。研究结果兼具显著的统计学差异与明确的临床获益。
HB1901为西罗莫司白蛋白结合型纳米颗粒注射用混悬液,其活性药物成分(API)为西罗莫司,属于境内外均未上市的改良型新药。HB1901有效克服了传统口服制剂生物利用度低,以及无法向靶部位递送足够浓度药量的缺点,从而拓展了其在抗肿瘤领域的应用。与已上市的mTOR抑制剂片剂及口服悬液相比,HB1901预期可显著提高西罗莫司的生物利用度,并降低消化系统毒性。
(5)默沙东PD-1/VEGF双抗在AACR年会公布临床结果
4月20日,默沙东首次公布了其PD-1×VEGF双特异性抗体MK-2010(原研代号LM-299,源自礼新医药,现隶属中国生物制药)的临床数据,在一线PD-L1阳性非小细胞肺癌(NSCLC)患者中展现出55%的未确认客观缓解率(ORR),与目前该赛道的领跑者康方生物/Summit的依沃西单抗(ivonescimab)旗鼓相当。
根据AACR上披露的壁报数据,MK-2010来自中国开展的一项I/II期临床试验。不过,默沙东的数据来自仅11例患者的小样本回填队列,随访时间也较短(中位随机化后3.3个月),后续疗效仍待临床开展。
(6)强生公布EGFR/c-Met双抗ADC临床前数据
4月20日,强生已经在已上市的EGFR/c-Met双抗Rybrevant药物基础上,迭代开发了ADC药物JNJ-95437446,本次会议期间将公布期开发历程和临床前结果。
根据强生公开的墙报信息,JNJ-95437446的母体抗体采用Rybrevant,仍然具有低岩藻糖介导的ADCC效应。ADC构建方面,其采用了多禧生物的平台,Exatecan衍生物CPT-113作为毒素,AAA三肽的可切割连接子,偶联方面采用了二硫键桥,以实现在重轻链的定点偶联,DAR值为4。和母体双抗一样,JNJ-95437446具有高度的选择性,仅对于EGFR/c-Met的表达的细胞具有结合。体内方面,JNJ-95437446在EGFR突变或KRAS突变的非小细胞肺癌CDX模型中均显示了显著的肿瘤抑制作用,未来值得期待。
2025年7月,强生已经在clinical trials网站上,登记了JNJ-95437446的首次临床试验,将在非小细胞肺癌和结直肠癌等多种实体瘤中进行首次临床探索,预计入组380例受试者。
(7)阿斯利康宣布全球首个C5单抗IgA肾病III期研究结果积极
4月21日,阿斯利康宣布瑞利珠单抗(ravulizumab)治疗免疫球蛋白A肾病(IgAN)成人患者的III期I CAN研究在预先指定的中期分析中达到了24小时尿蛋白肌酐比值(24h-UPCR)终点。该药物是全球首个在III期研究中取得积极结果的C5药物。
瑞利珠单抗是阿斯利康斥资390亿美元收购Alexion后获得的罕见病管线,也是目前最长效的C5补体抑制剂,可提供即时、完全且持续的补体抑制。它通过抑制人体免疫系统中末端补体级联反应中的C5蛋白发挥作用。
目前,瑞利珠单抗已在多国获批,用于治疗阵发性睡眠性血红蛋白尿症(PNH)、非典型溶血性尿毒症综合征(aHUS)、全身型重症肌无力(gMG) 和视神经脊髓炎谱系疾病(NMOSD)。
(8)默沙东/卫材肾癌新药III期临床失败
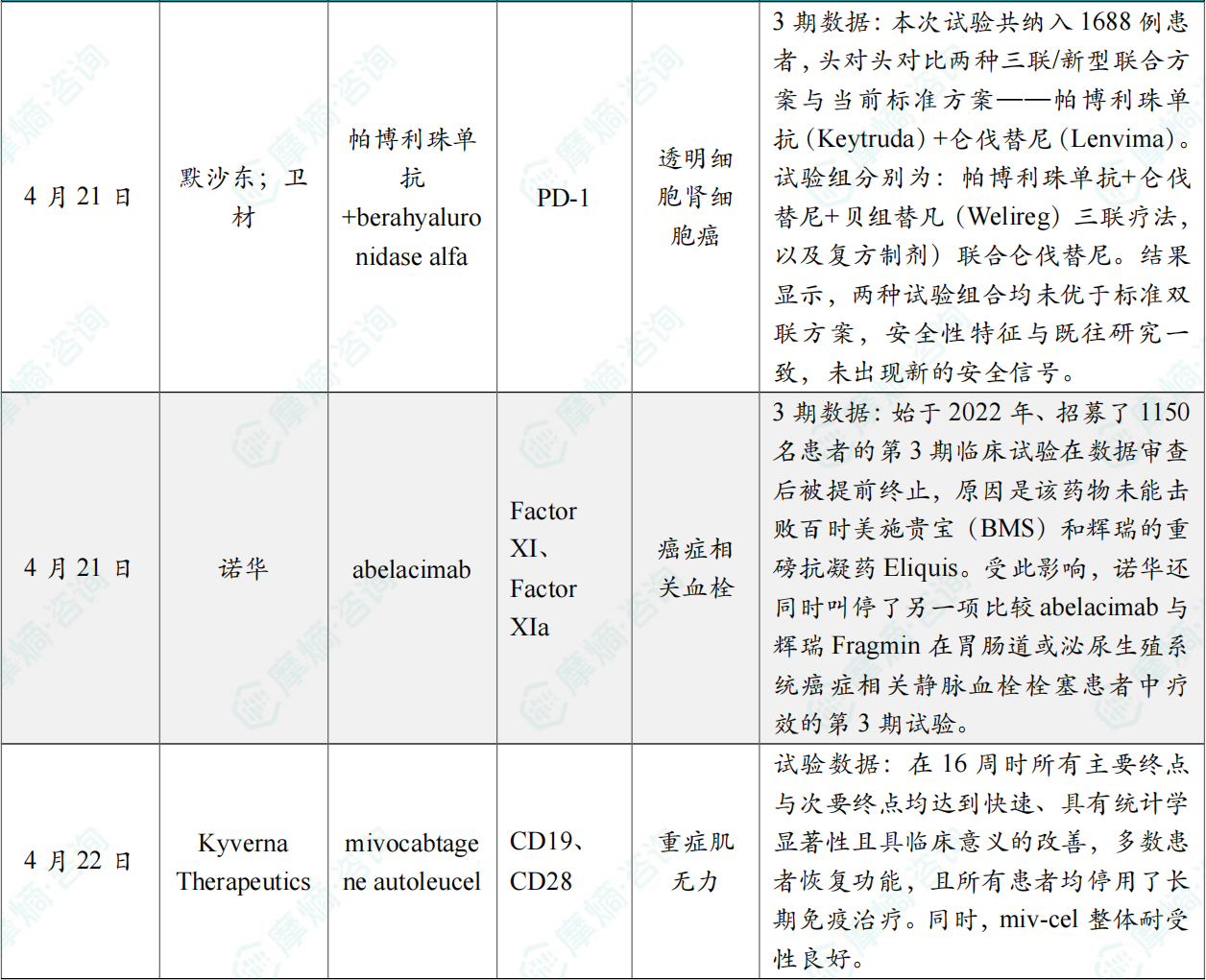
4月21日,默沙东与卫材联合宣布,用于晚期透明细胞肾细胞癌(RCC)一线治疗的三期临床试验LITESPARK-012,在预设中期分析中未达到无进展生存期(PFS)和总生存期(OS)双重主要终点。
本次试验共纳入1688例患者,头对头对比两种三联/新型联合方案与当前标准方案——帕博利珠单抗(Keytruda)+仑伐替尼(Lenvima)。试验组分别为:帕博利珠单抗+仑伐替尼+贝组替凡(Welireg)三联疗法,以及MK-1308A(Keytruda+Quavonlimab复方制剂)联合仑伐替尼。结果显示,两种试验组合均未优于标准双联方案,安全性特征与既往研究一致,未出现新的安全信号。
(9)诺华终止一项临床III期试验
4月21日,诺华(Novartis)宣布停止其抗凝血抗体药物abelacimab针对癌症相关血栓(CAT)的开发工作。这项始于2022年、招募了1150名患者的第3期临床试验在数据审查后被提前终止,原因是该药物未能击败百时美施贵宝(BMS)和辉瑞的重磅抗凝药Eliquis。
受此影响,诺华还同时叫停了另一项比较abelacimab与辉瑞Fragmin在胃肠道或泌尿生殖系统癌症相关静脉血栓栓塞患者中疗效的第3期试验。
尽管在2026年遭遇了这一重大挫折,诺华并未完全放弃该药物的开发,abelacimab目前仍在继续进行其首要适应症——心房颤动(AFib)的第3期临床试验,公司计划在2028年提交该适应症的上市批准申请。
(10)Kyverna Therapeutics宣布自身免疫CAR-T疗法注册性试验结果积极
4月22日,Kyverna Therapeutics宣布,其注册性试验KYSA-8取得积极主要分析结果。该研究评估miv-cel(mivocabtagene autoleucel,KYV-101)治疗僵人综合征(SPS)的疗效与安全性。
结果显示,患者接受单次miv-cel治疗后,在16周时所有主要终点与次要终点均达到快速、具有统计学显著性且具临床意义的改善,多数患者恢复功能,且所有患者均停用了长期免疫治疗。同时,miv-cel整体耐受性良好。
Miv-cel是一款全人源、CD19靶向自体CAR-T疗法,具有CD28共刺激域,旨在实现高效活性与良好耐受性,目前正在开发用于治疗B细胞驱动的自身免疫疾病。
同期事件:
1. 2026年第17周04.20-04.26国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第17周04.20-04.26国内仿制药/生物类似物申报/审批数据分析
3. 2026年第17周04.20-04.26国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.04.20-2026.04.26) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论