
2026年4月13日,第一三共与默沙东联合宣布,旗下靶向B7-H3的抗体偶联药物(ADC)ifinatamab deruxtecan(I-DXd)的生物制品许可申请(BLA)已获美国FDA受理,用于治疗含铂化疗后进展的广泛期小细胞肺癌(ES-SCLC)成人患者。
FDA同时授予该申请优先审评资格,并设定处方药用户付费法案(PDUFA)目标日期为2026年10月10日。这意味着全球首款B7-H3 ADC的上市进程进入冲刺阶段,有望为缺乏有效后续疗法的小细胞肺癌患者带来新选择。

截图来源:默沙东官网
一、临床数据亮眼:ORR达48.2%,中位OS超10个月
此次BLA主要基于IDeate-Lung01 II期临床试验的结果,并得到IDeate-PanTumor01 I/II期研究数据的支持。
在IDeate-Lung01研究的剂量优化及扩展阶段,共纳入137例接受12 mg/kg ifinatamab deruxtecan治疗的ES-SCLC患者。经盲法独立中央评审(BICR)评估:
- 确认的客观缓解率(ORR)为48.2%(95% CI: 39.6–56.9),其中包括3例完全缓解(CR)和63例部分缓解(PR)。
- 疾病控制率(DCR)高达87.6%(95% CI: 80.9–92.6),另有54例患者疾病稳定(SD)。
- 中位缓解持续时间(DOR)为5.3个月(95% CI: 4.0–6.5)。
- 中位无进展生存期(PFS)为4.9个月(95% CI: 4.2–5.5)。
- 中位总生存期(OS)达到10.3个月(95% CI: 9.1–13.3)。
该数据在既往经治的ES-SCLC患者中表现出显著的抗肿瘤活性与生存获益,为其加速审评提供了关键支撑。
二、技术机制:潜在“first-in-class”B7-H3 ADC
Ifinatamab deruxtecan是一款潜在“first-in-class”的B7-H3靶向ADC,采用第一三共专有的DXd ADC技术平台构建。
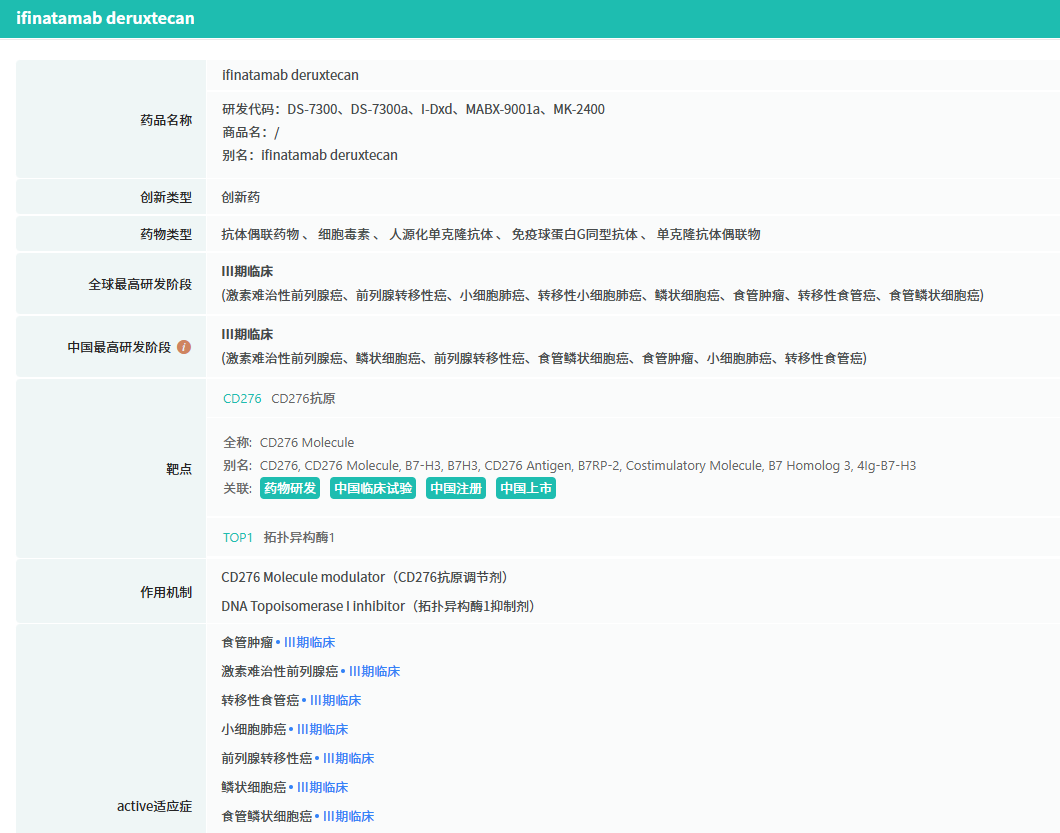
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
该药物以人源化抗B7-H3 IgG1单克隆抗体为载体,通过基于四肽的可裂解连接子,与多个高效拓扑异构酶I抑制剂有效载荷相连。这种设计旨在实现肿瘤靶向递送与高效杀伤,同时降低系统性毒性。
B7-H3(CD276)是B7免疫调节蛋白家族成员,在多种实体瘤中过度表达,但在正常组织中表达有限,使其成为ADC治疗的理想靶点。此前,该药物已于2025年8月获得FDA授予的突破性疗法认定,用于同一适应症。
三、竞争格局:全球暂无产品获批,中国药企竞速III期
据摩熵医药数据库显示,全球范围内尚未有B7-H3 ADC药物获批上市,但竞争已悄然白热化——目前已有超过20款B7-H3 ADC进入临床研发阶段,其中多数由中国药企主导开发。
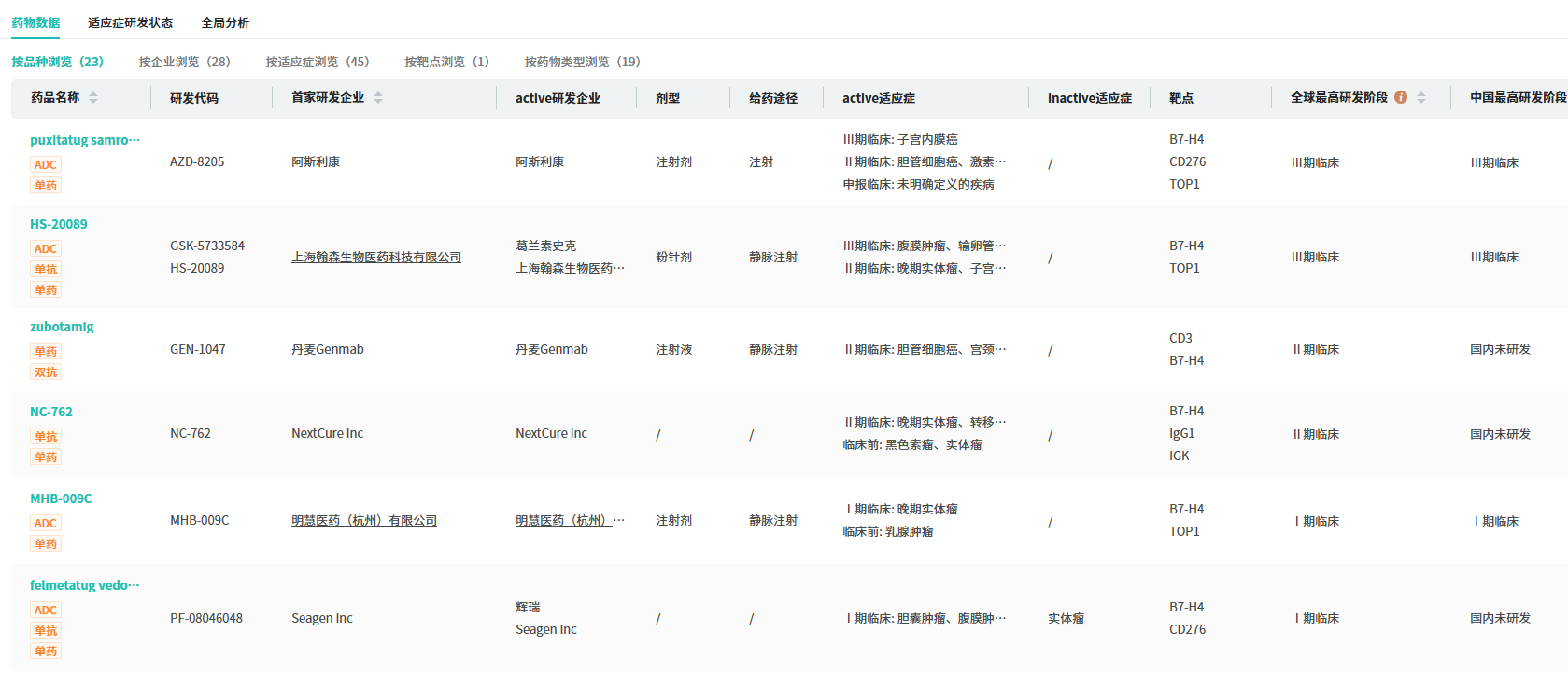
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
除第一三共/默沙东的ifinatamab deruxtecan外,目前另有4款B7-H3 ADC已进入III期临床,分别来自翰森制药/GSK、宜联/罗氏、明慧医药/齐鲁、映恩生物/BioNTech。这意味着,ifinatamab deruxtecan若能在今年10月顺利获批,不仅将成为全球首款B7-H3 ADC,更将在小细胞肺癌治疗领域树立新的治疗标杆,并为后续同靶点药物的开发与审评提供重要参考。
结语
从突破性疗法认定到优先审评,ifinatamab deruxtecan的上市进程持续提速,折射出FDA对填补小细胞肺癌后线治疗空白的迫切期待,也印证了第一三共DXd ADC平台与B7-H3靶点组合的临床潜力。在ADC竞争日益激烈的全球格局中,首款B7-H3 ADC的临近,不仅为患者带来了新的生存希望,也预示着该靶点赛道将从研发竞赛转向临床价值与市场占位的实质性比拼。2026年10月,这场关乎“first-in-class”的审评终局,值得期待。
参考来源:
[1] 企业官网/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 第一三共与默沙东联手:DS-6000a拟纳入突破性治疗!CDH6靶向ADC剑指难治肿瘤,多癌种布局加速
2. 齐鲁制药QLC5508突破性疗法双认定!B7-H3 ADC赛道国内领跑,难治食管癌与前列腺癌迎希望
3. 信达生物IBI3001:B7-H3/EGFR双抗ADC首次在中国获批IND
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论