1.4.1 本周全球TOP10创新药研发进展
(1)第一三共/默沙东在美国提交B7H3 ADC上市申请
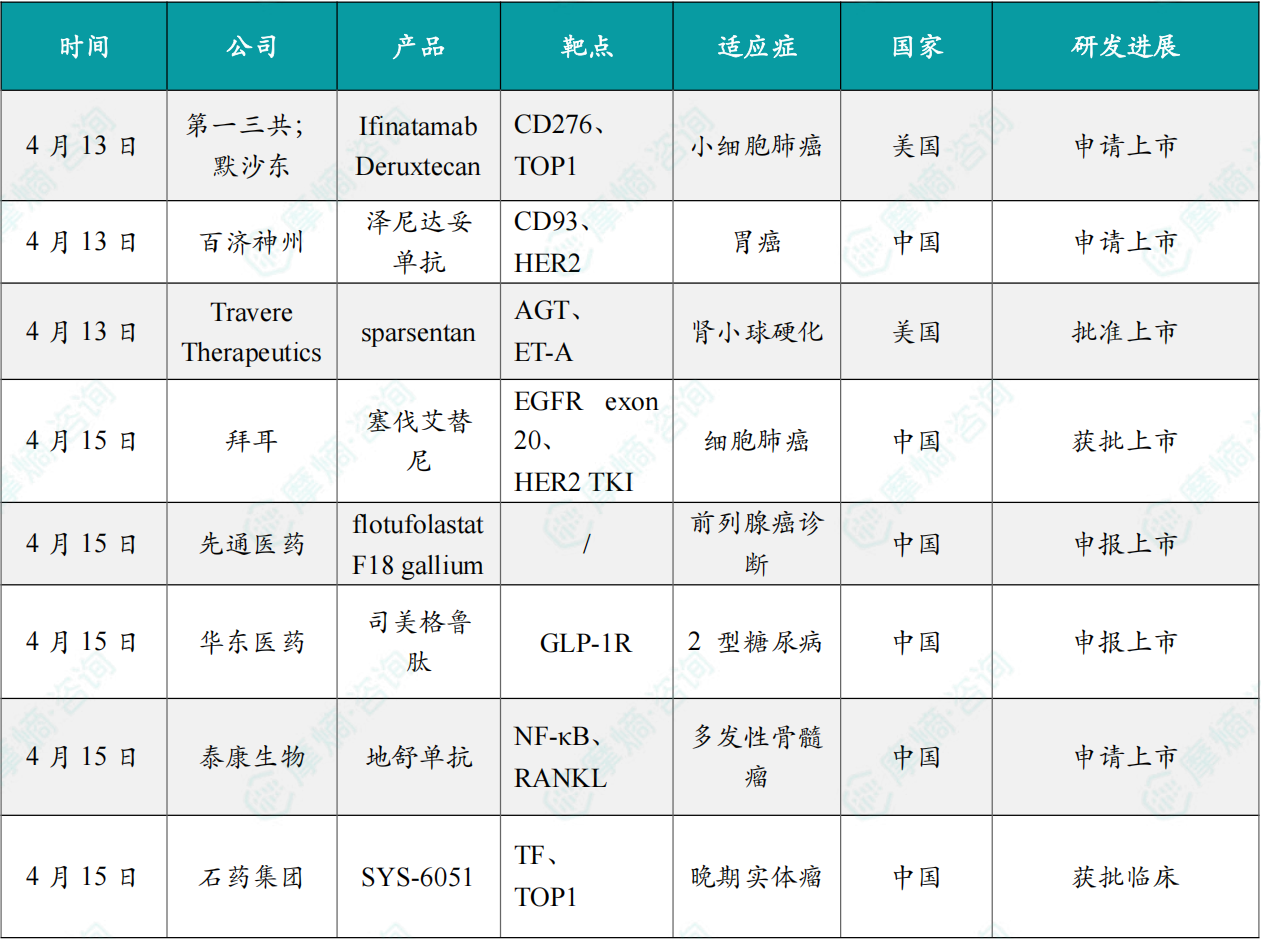
4月13日,第一三共和默沙东共同宣布,提交了B7H3 ADC药物Ifinatamab Deruxtecan的生物制品许可申请 (BLA),用于治疗接受铂类化疗后疾病进展的广泛期小细胞肺癌 (ES-SCLC) 成人患者,同时其已被美国食品药品监督管理局 (FDA) 受理并授予优先审评资格。FDA 正在根据实时肿瘤学审查 (RTOR) 项目和 Orbis 项目审查该生物制品许可申请 (BLA)。
Ifinatamab deruxtecan为第一三共开发的B7-H3 ADC药物,其采用GGFG-Dxd的构建搭载ADC药物,其DAR值为4。ifinatamab deruxtecan的该项BLA 基于 IDeate-Lung01 II 期试验的结果,并得到了 IDeate PanTumor01 I/II 期试验的支持。2025年WCLC会议期间公布的临床数据显示,其中位PFS值达到4.9个月,中位OS值达到10.3个月,ILD发生率为12.4%,三级及以上的仅为4.4%。
(2)百济神州HER2双抗+PD-1单抗组合申报上市
4月13日,百济神州宣布泽尼达妥单抗联合替雷利珠单抗的新适应症上市申请(sBLA)获得CDE受理,拟用于一线治疗局部晚期不可切除或转移性HER2阳性胃癌、胃食管结合部腺癌或食管腺癌。泽尼达妥单抗单药已于2025年5月在国内获批上市,用于治疗既往接受过全身治疗的HER2高表达(IHC3+)的不可切除局部晚期或转移性胆道癌(BTC)患者。
泽尼达妥单抗是一款HER2靶向人源化双特异性抗体,由Jazz Pharmaceuticals和百济神州共同开发和商业化。此次sBLA是基于III期HERIZON-GEA-01研究的积极结果。数据显示,无论PD-L1表达状态如何(包括PD-L1<1%的患者),泽尼达妥单抗+替雷利珠单抗+化疗组达到双重的主要研究终点。具体而言,泽尼达妥单抗+替雷利珠单抗+化疗组的中位PFS达到12.4个月(HR=0.63;P≤0.0001),疾病进展风险降低37%,改善超过4个月;中位OS达到26.4个月(HR=0.72;P=0.0043),死亡风险降低28%,改善超过7个月。
(3)Travere Therapeutics宣布药物FILSPARI获美国FDA批准上市
4月13日,Travere Therapeutics宣布美国FDA正式全面批准其药物FILSPARI(sparsentan)用于治疗无肾病综合征的8岁及以上局灶节段性肾小球硬化(FSGS)成人和儿童患者。作为首个也是唯一一个获得FDA批准治疗FSGS的药物,为依赖长效类固醇等超适应症疗法的患者带来了希望。
此前,由于FDA要求Travere提供更多关于FILSPARI临床获益特征的补充分析数据,并将此视为对补充新药申请(sNDA)的重大修改,因此将目标行动日期延后了三个月。Travere公司澄清FDA并未对该药物的安全状况或制造工艺提出任何质疑,这一推迟还是引发了市场的剧烈恐慌,导致公司股价在消息公布时一度暴跌高达33%,随后在当日收盘时跌幅收窄至近15%。
(4)拜耳肺癌新药在华获批上市
4月15日,拜耳宣布塞伐艾替尼(sevabertinib,BAY 2927088)获批上市,用于治疗携带HER2(ERBB2)激活突变且既往接受过一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
塞伐艾替尼是拜耳开发的一款口服非共价可逆选择性酪氨酸激酶抑制剂,对携带EGFR和HER2突变(包括HER2 exon 20插入突变)的肿瘤有抑制活性。
2025年11月19日,塞伐艾替尼在美国获批上市,用于治疗经FDA批准的伴随诊断设备证明肿瘤携带HER2(ERBB2)酪氨酸激酶结构域(TKD)激活突变并且接受过系统治疗的局部晚期或转移性非鳞状NSCLC成人患者。
(5)先通医药创新核药申报上市
4月15日,先通医药宣布,其创新放射性药物氟[18F]妥司特注射液(XTR020)新药上市申请(NDA)已获国家药监局受理,用于前列腺癌诊断。该申请基于一项成功的中国 III 期临床试验结果。
这是一项单臂、多中心 III 期临床,共纳入 121 例受试者,旨在评估XTR020注射液 PET 成像在既往治疗后前列腺癌生化复发(BCR)的受试者中的诊断效能和安全性。结果显示,该药物在BCR患者个体水平的正确检出率(CDR)达到预设目标,展现出较高的诊断效能。安全性方面,未发生严重不良反应。
(6)华东医药司美格鲁肽减重适应症上市许可申请获得受理
4月15日,CDE 官网显示,华东医药司美格鲁肽注射液新适应症上市许可申请获得受理,适用于在控制饮食和增加体力活动的基础上对成人患者的长期体重管理。2025年4月,该产品降糖适应症上市申请也已获受理。
司美格鲁肽是一种长效胰高血糖素样肽-1(GLP-1)受体激动剂,与人GLP-1有94%的序列同源性,临床上主要用于2型糖尿病患者的血糖控制、肥胖或超重患者的长期体重管理。原研由诺和诺德开发,一经上市便迅速火爆,2025年销售额已经达到了346亿美元,仅次于替尔泊肽。该产品在国内的市场表现亦是不俗,2025年销售额为10.33亿美元。
(7)迈威生物旗下地舒单抗新适应症补充申请获NMPA受理
4月15日,迈威生物宣布国家药品监督管理局(NMPA)已受理其全资子公司泰康生物自主研发的迈卫健®(地舒单抗注射液,研发代号:9MW0321)的增加适应症补充申请,用于治疗实体肿瘤骨转移和多发性骨髓瘤适应症(用于实体肿瘤骨转移患者或多发性骨髓瘤患者的治疗,以延迟或降低骨相关事件(病理性骨折、脊髓压迫、骨放疗或骨手术)的发生风险)。
迈卫健®是国内首款获批上市的地舒单抗生物类似药(120mg),于 2024年3月首次获批上市,用于治疗不可手术切除或者手术切除可能导致严重功能障碍的骨巨细胞瘤,包括成人和骨骼发育成熟(定义为至少 1 处成熟长骨且体重 ≥45kg)的青少年患者。
(8)石药集团靶向TF的ADC新药在中国获批临床
4月15日,中国国家药监局药品审评中心(CDE)官网公示显示,石药集团申报的1类新药SYS6051获批临床,拟开发治疗晚期实体瘤。公开资料显示,这是一款靶向组织因子(TF)的抗体偶联药物(ADC),拟开发用于治疗TF阳性表达的恶性肿瘤。
根据2025年AACR大会公布的临床前研究结果,SYS6051采用人源化TF靶向IgG1抗体,通过可被蛋白酶切割的连接子,将拓扑异构酶I抑制剂Exatecan定点偶联于抗体上,药物-抗体比(DAR)为6。与传统半胱氨酸硫醇-马来酰亚胺偶联ADC相比,SYS6051对逆Michael消除反应的抵抗力增强,因而具有更高的稳定性。
(9)罗氏口服SERD药物在华申报上市
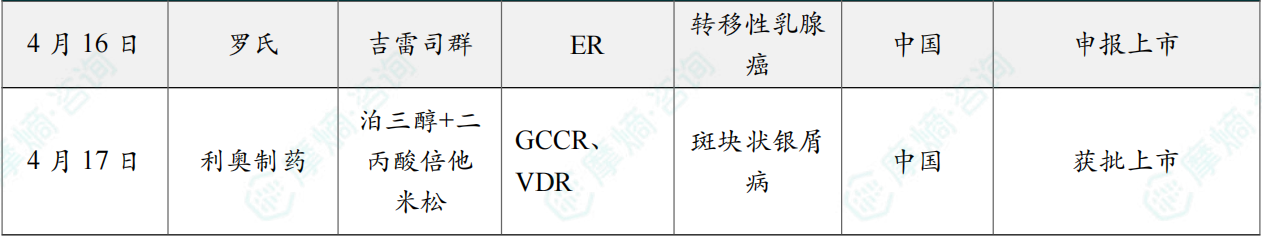
4月16日,CDE官网显示,罗氏的吉雷司群(Giredestrant)申报上市,用于联合依维莫司治疗既往接受过内分泌疗法治疗且携带ESR1突变的ER+/HER2-局部晚期或转移性乳腺癌患者。该药物已于今年2月在美国申报上市,PDUFA日期为2026年12月18日。
Giredestrant是罗氏自主研发的一款下一代口服选择性雌激素受体降解剂(SERD)和完全拮抗剂,旨在阻止雌激素与雌激素受体(ER)结合,诱导其降解,从而阻止或减缓癌细胞的生长。III期evERA研究结果显示,在意向治疗(ITT)人群中,Giredestrant组和对照组经研究者评估的无进展生存期(PFS)分别为8.77个月和5.49个月(HR=0.56);在ESR1突变亚组中,Giredestrant组和对照组经研究者评估的PFS分别为9.99个月和5.45个月(HR=0.38)。
(10)利奥制药银屑病外用新药在华获批上市
4月17日,利奥制药宣布国家药品监督管理局(NMPA)已批准卡泊三醇倍他米松泡沫剂(恩适达®)用于治疗成人斑块状银屑病患者。卡泊三醇倍他米松泡沫剂(恩适达®)是中国首个且目前唯一用于成人斑块状银屑病外用治疗的泡沫剂,专利的起泡装置可帮助患者轻松将药物均匀涂抹于皮肤,包括有毛发的部位。
临床研究显示,泡沫剂型可以在皮肤表面形成过饱和溶液,加速有效成分渗透,快速缓解症状。此次国家药监局的批准基于一项III期临床试验的结果,该试验在中国604例成人稳定性斑块状银屑病患者中,比较了使用恩适达®(卡泊三醇倍他米松泡沫剂)和得肤宝®(卡泊三醇倍他米松软膏)(每日一次)治疗4周后的疗效和安全性。该试验达到了主要和次要终点,且恩适达®的疗效优于得肤宝。
1.4.2本周全球TOP10积极/失败临床结果
(1)葛兰素史克B7H4 ADC临床结果积极
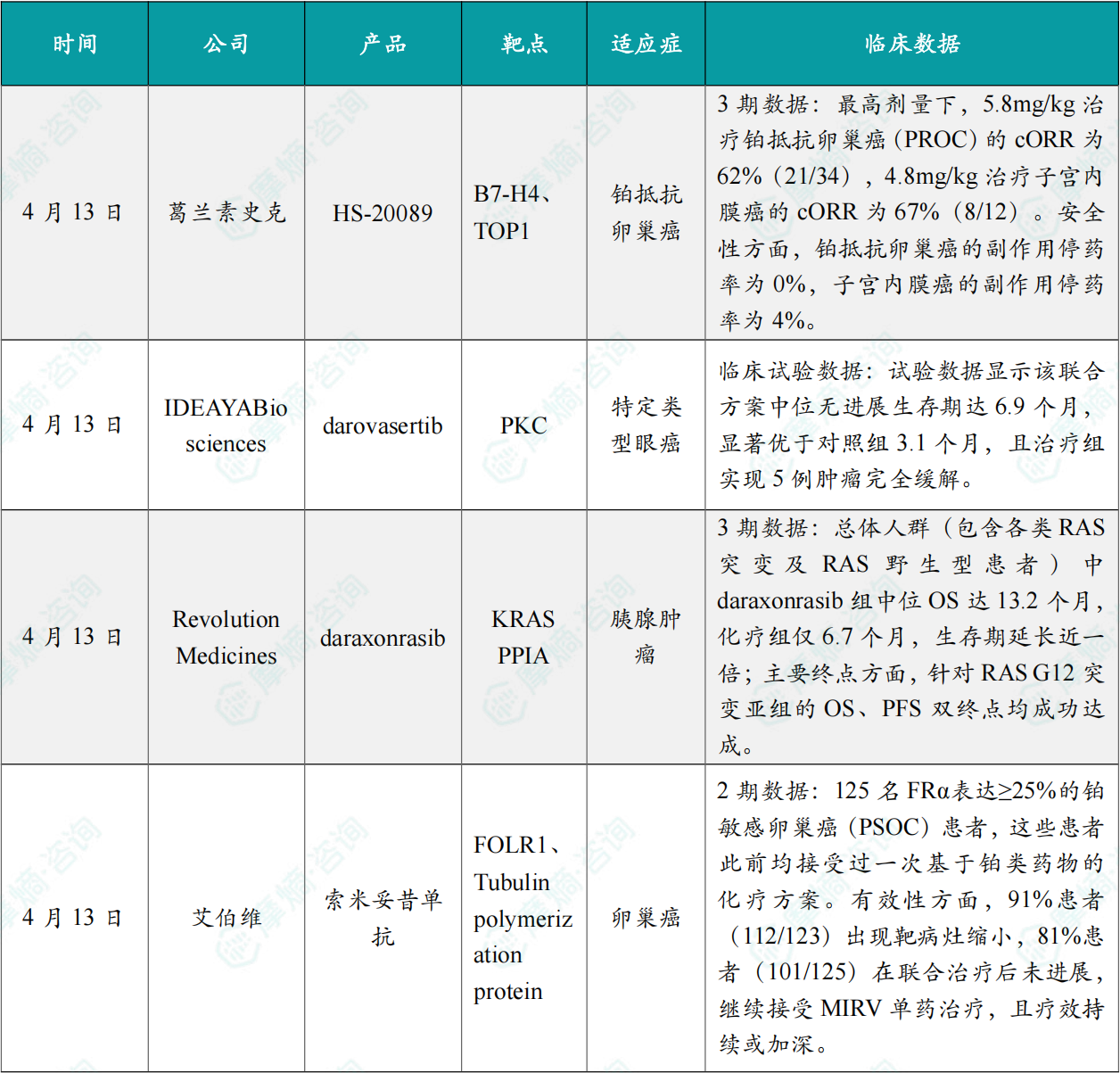
4月13日,葛兰素史克公布B7H4 ADC新药Mocertatug rezetecan全球一期临床BEHOLD-1的最新数据。最高剂量下,5.8mg/kg治疗铂抵抗卵巢癌(PROC)的cORR为62%(21/34),4.8mg/kg治疗子宫内膜癌的cORR为67%(8/12)。安全性方面,铂抵抗卵巢癌的副作用停药率为0%,子宫内膜癌的副作用停药率为4%。3级及以上副作用发生率分别为64%、54%,主要为血液毒性。
Mocertatug rezetecan由翰森制药研发,2023年10月,葛兰素史克以8500万美元预付款+14.85亿美元里程别+分级销售分成引进其大中华区外全球权益。基于初步临床的优异疗效,葛兰素史克将在今年启动5项全球三期临床,从铂抵抗卵巢(BEHOLD-Ovarian01)和二线子宫内膜癌(BEHOLD-Endometrial01)开始,其他三林城包括铂敏感卵巢癌(BEHOLD-Ovarian02)、一线维持场景治疗无同源重组缺陷的卵巢癌(BEHOLD-Ovarian03)、错配修复完整(pMMR)子宫内膜癌(BEHOLD-Endometrial02)。
(2)IDEAYA/辉瑞眼癌组合疗法成功
4月13日,路透社消息,IDEAYA Biosciences(IDYA)宣布,其用于治疗特定类型眼癌的在研药物组合,在一项中后期关键临床试验中成功达到主要研究终点,显著延长患者无进展生存期。受此利好消息影响,公司盘前股价大涨39.2%。
本次临床研究中,darovasertib联合辉瑞Xalkori的治疗方案,展现出突出疗效:中位无进展生存期达6.9个月,显著优于研究者选择的其他疗法(3.1个月);联合治疗组观察到5例完全缓解,即患者体内所有可检测到的癌症迹象完全消失。此次积极数据,为这款眼癌在研疗法的后续研发与上市申报奠定重要基础,也为眼癌患者带来新的治疗希望。
(3)Revolution Medicines宣布泛RAS抑制剂daraxonrasib的3期临床试验数据
4月13日,Revolution Medicines宣布,泛RAS抑制剂daraxonrasib(研发代号:RMC-6236) 用于治疗既往经治的转移性胰腺导管腺癌(PDAC)的3期临床试验成功抵达主要生存终点,相较标准化疗为患者带来显著且大幅的生存期改善。
具体而言,总体人群(包含各类RAS突变及RAS野生型患者)中daraxonrasib组中位OS达13.2个月,化疗组仅6.7个月,生存期延长近一倍;主要终点方面,针对RAS G12突变亚组的OS、PFS双终点均成功达成。Revolution Medicines表示,将以本次OS与PFS关键数据为核心,启动全球监管申报流程。美国市场将启用FDA局长国家优先审评券(CNPV) 试点计划,大幅加速上市审评进程。而完整试验数据计划在2026年5月底举办的美国临床肿瘤学会(ASCO)年会正式对外发布。
(4)艾伯维公布FRα ADC铂敏感卵巢癌II期临床数据
4月13日,正在举行的2026年美国妇科肿瘤学会(SGO)上,艾伯维以口头报告的方式,公布了FRα ADC药物Mirvetuximab Soravtansine(MIRV),联合卡铂治疗铂敏感卵巢癌(PSOC)的II期临床IMGN853-0420数据,其也成为首个证实ADC与卡铂在卵巢癌中可联合使用的临床试验。
Mirvetuximab Soravtansine(MIRV)为艾伯维从ImmunoGen收购的全球首款上市获批的FRα ADC药物,其采用SPDB的连接子和DM4的毒素,DAR为4。
这项名为IMGN853-0420的多中心、开放标签II期试验共招募了125名FRα表达≥25%的铂敏感卵巢癌(PSOC)患者,这些患者此前均接受过一次基于铂类药物的化疗方案。有效性方面,91%患者(112/123)出现靶病灶缩小,81%患者(101/125)在联合治疗后未进展,继续接受MIRV单药治疗,且疗效持续或加深。整体人群中的客观响应率达到68%。
(5)远大医药创新核药达到临床终点
4月13日,远大医药宣布,其联营公司Sirtex Medical Pty Ltd 的 SIR-Spheres®钇[90Y]微球注射液(易甘泰®)在美国开展的用于治疗不可切除肝细胞癌(HCC)临床研究 DOORwaY90成功达到了临床终点。
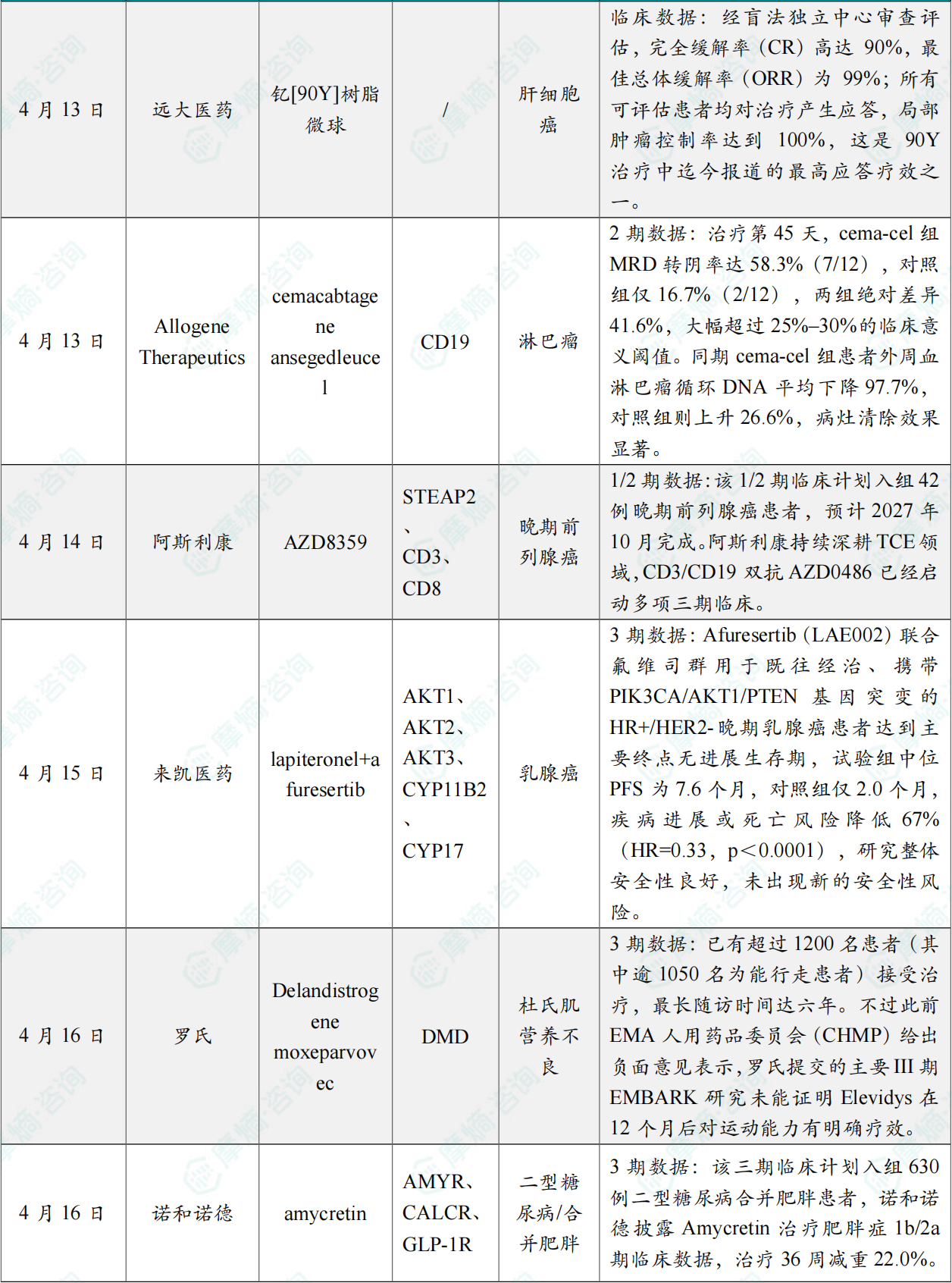
DOORwaY90研究是美国首个采用分割剂量学技术对不可切除 HCC 患者实施90Y选择性内放射治疗(SIRT)的关键性、前瞻性、多中心临床研究。研究数据显示,该研究已成功达到预先设定的共同主要终点:经盲法独立中心审查评估,完全缓解率(CR)高达90%,最佳总体缓解率(ORR)为99%;所有可评估患者均对治疗产生应答,局部肿瘤控制率达到100%,这是90Y治疗中迄今报道的最高应答疗效之一。
(6)Allogene Therapeutics公布II期临床试验积极数据
4月13日,细胞疗法企业Allogene Therapeutics公布其现货异体CAR-T疗法cema-cel(cemacabtagene ansegedleucel)II期ALPHA3试验首批关键临床数据,在一线化疗后仍存在微小残留病灶(MRD)的大B细胞淋巴瘤患者中,该疗法展现出远超临床预期的病灶清除效果与优异安全性,为长期陷入“核冬天”的异体CAR-T领域带来关键复苏信号。
ALPHA3为全球首个针对淋巴瘤MRD干预的随机对照II期试验,计划入组约220例患者,本次首批披露24例经6周期一线化疗后MRD仍呈阳性的大B细胞淋巴瘤患者,1:1随机分配至cema-cel治疗组与标准观察对照组。治疗第45天,cema-cel组MRD转阴率达58.3%(7/12),对照组仅16.7%(2/12),两组绝对差异41.6%,大幅超过25%–30%的临床意义阈值。同期cema-cel组患者外周血淋巴瘤循环DNA平均下降97.7%,对照组则上升26.6%,病灶清除效果显著。
(7)阿斯利康STEAP2/CD3/CD8三抗启动1/2期临床
4月14日,阿斯利康在Clinicaltrials.gov网站上注册了AZD8359治疗前列腺癌的1/2期临床试验CRIUS-1。
AZD8359为一款STEAP2/CD3/CD8三抗,阿斯利康将在今年AACR会议上汇报该管线的临床前研究数据。该1/2期临床计划入组42例晚期前列腺癌患者,预计2027年10月完成。阿斯利康持续深耕TCE领域,CD3/CD19双抗AZD0486已经启动多项三期临床。阿斯利康已经布局一款STEAP2靶向核药(AZD2284),一款STEAP2/CD3双抗(AZD6621),一款STEAP2 CAR-T(AZD0754)以及CD8/IL-2(AZD 6750),此次进一步将CD8-guided技术应用到实体瘤TCE领域。
(8)来凯医药宣布AfuresertibIII期研究成功
4月15日,来凯医药宣布Afuresertib(LAE002)联合氟维司群治疗HR+/HER2-乳腺癌的III期临床试验(AFFIRM-205)成功达到了主要终点——在无进展生存期(PFS)方面,Afuresertib(LAE002)联合氟维司群用于既往经治、携带PIK3CA/AKT1/PTEN基因突变的HR+/HER2-晚期乳腺癌患者达到主要终点无进展生存期,试验组中位PFS为7.6个月,对照组仅2.0个月,疾病进展或死亡风险降低67%(HR=0.33,p<0.0001),研究整体安全性良好,未出现新的安全性风险。
(9)罗氏启动基因疗法全球关键性III期临床
4月16日,罗氏宣布启动一项新的全球关键性III期临床试验,为其基因疗法Elevidys(delandistrogene moxeparvovec)在欧洲及其他地区的上市铺路。这款针对杜氏肌营养不良症(DMD)的基因疗法此前已在包括美国在内的九个国家获批,但欧洲药品管理局(EMA)去年拒绝了其有条件上市申请。
Elevidys的临床开发项目是DMD领域规模最大、随访时间最长的基因疗法研究,已有超过1200名患者(其中逾1050名为能行走患者)接受治疗,最长随访时间达六年。不过此前EMA人用药品委员会(CHMP)给出负面意见表示,罗氏提交的主要III期EMBARK研究未能证明Elevidys在12个月后对运动能力有明确疗效。安全性方面的担忧是Elevidys面临的另一重压力。美国FDA也添加了关于急性严重肝损伤和急性肝衰竭(包括致死病例)的黑框警告,并将适应症限定为4岁及以上的能行走DMD患者。
(10)诺和诺德Amycretin启动糖尿病合并肥胖三期临床
4月16日,诺和诺德在Clinicaltrials.gov网站上注册了Amycretin(NNC0487-0111)治疗二型糖尿病/合并肥胖的三期临床试验AMAZE 2。该三期临床计划入组630例二型糖尿病合并肥胖患者,预计2028年5月初步完成。
此前,诺和诺德披露Amycretin治疗肥胖症1b/2a期临床数据,治疗36周减重22.0%。此次糖尿病二期临床数据,再次验证Amycretin的优异疗效,超越GLP-1+Amylin联合治疗(非头对头)。诺和诺德计划今年陆续启动Amycretin的多项三期临床试验,覆盖减重、OSA、骨关节炎等适应症,以及口服给药途径的减重三期临床,未来或将拓展到ASCVD、心衰、CKD等更多适应症。
今年1月,诺和诺德启动了Amycretin治疗减重的首个三期临床AMAZE 1。今年3月,诺和诺德启动了Amycretin治疗肥胖合并骨关节炎的三期临床试验AMAZE 5。
同期事件:
1. 2026年第16周04.13-04.19国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第16周04.13-04.19国内仿制药/生物类似物申报/审批数据分析
3. 2026年第16周04.13-04.19国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.04.13-2026.04.19) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论