
1月10日,CDE官网显示,正大天晴的贝莫苏拜单抗注射液拟纳入优先审评,用于治疗晚期或不可切除腺泡状软组织肉瘤。

截图来源:CDE
贝莫苏拜单抗,作为一种针对PD-L1的单克隆抗体药物,已在国内取得两项重要适应症批准:一是与安罗替尼及化疗联合,作为一线治疗方案应用于广泛期小细胞肺癌;二是与安罗替尼联用,针对那些曾经历系统性抗肿瘤治疗失败且不宜接受根治性手术或放疗的非MSI-H/非dMMR复发性或转移性子宫内膜癌患者。
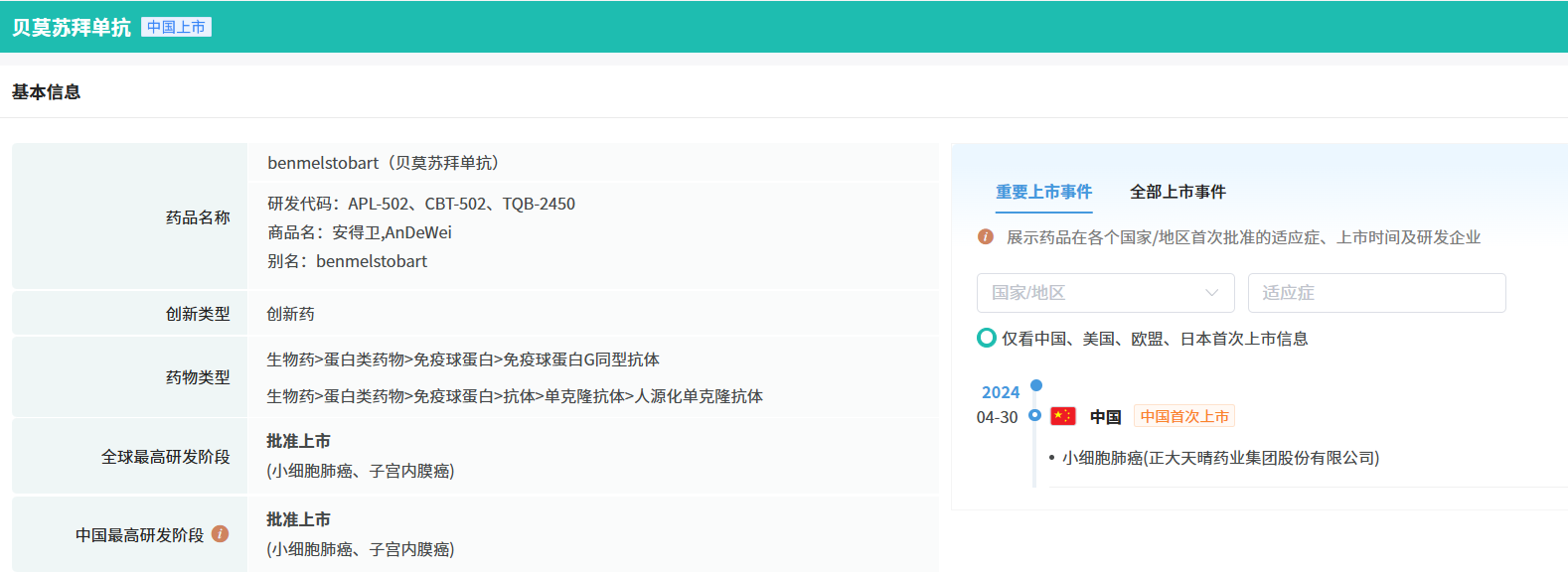
截图来源:摩熵医药全球药物研发数据库
在2024年ASCO大会上,正大天晴公司发布了贝莫苏拜单抗联合盐酸安罗替尼胶囊在治疗腺泡状软组织肉瘤(ASPS)患者中的临床研究数据(CTR20190938)。该研究共涉及29名患者,其中28名(1名患者退出)的总体缓解率(ORR)高达79.3%,包括3例完全缓解和20例部分缓解。中位无进展生存期(PFS)及缓解者的中位持续时间(DOR)均未达到。进一步对7名患者(含3例反应良好与4例反应不佳者)的肿瘤微环境深入分析揭示,两组间三级淋巴结构(TLS)的存在情况存在显著差异。
安全性评估方面,研究期间未记录到死亡病例,且治疗方案展现出良好的耐受性,大多数不良反应为1级和2级。尽管有13例患者(44.83%)报告了3级及以上不良反应,但主要是高甘油三酯血症(13.79%)、脂肪酶升高(6.90%)、淀粉酶升高(3.45%)及高血压(3.45%)等。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论