
近日,Astellas公布了用于X连锁肌管肌病的AAV基因疗法AT132的安全性和有效性,以及试验中4名患者死亡原因。
X连锁肌管肌病(XLMTM)是一种严重的骨骼肌单基因疾病,由MTM1中的表达/功能突变缺失引起的(肌管蛋白)基因。在婴儿期发病,以新生儿肌张力低下和严重虚弱为特征。25-50%的受影响患者在生命的第一年死亡,而幸存下来的患者高度依赖技术(80%需要轮椅、呼吸机和饲管支持)并且寿命缩短。目前,对肌管型肌病患者尚无具体的治疗方法。
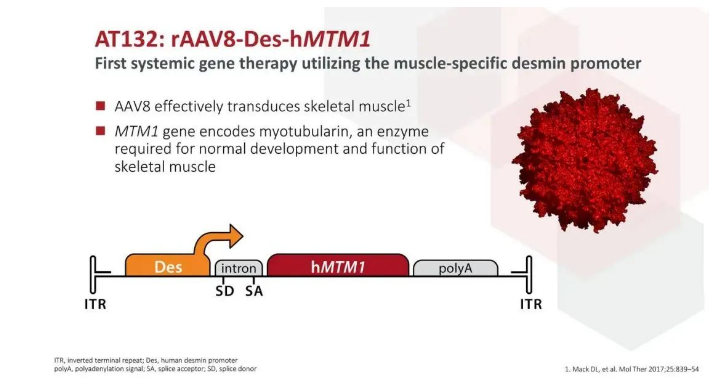
AT132是由腺相关病毒AAV为载体的基因治疗。AAV载体中最常用的是AAV9载体,而AT132采用的AAV8载体,该载体的安全性还有待验证。AT132可将正常的基因拷贝递送至患者体内,从而增加靶组织中肌管蛋白表达的能力,从而治疗XLMTM。
AT132药物基本信息

截图来源:药融云全球药物研发数据库
截至2022年2月28日,AT132的临床试验共有24名男孩患者参与,他们均依赖呼吸机。试验分为两个剂量:低剂量(1.3x1014vg/kg)和高剂量(3.5x1014vg/kg)。其中,7名接受的是1.3×10^14 vg/kg剂量,17名接受的是3.5×10^14 vg/kg剂量。
试验数据显示:治疗24周后,低剂量组的呼吸机平均支持时间(小时算)比对照组减少了约77.7%,有6名患者实现不依赖呼吸机,5名患者能够独立行走;相较于基线而言,高剂量组减少了22.8%,有10名患者实现不依赖呼吸机,有3名患者能够独立行走。
安全性方面:低剂量组中,观察到2例严重不良事件(SAEs);高剂量组中,观察到9例SAEs。4名患者死亡,剩下20名幸存者中有5人患有肝胆炎。
在未治疗组群的14名参与者中(对照组2名,自然史研究组12名),没有人实现不依赖呼吸机,但在48周时,有5名参与者能够独立坐30秒,没有实现其他的运动里程碑。
这些数据表明,AT132对XLMTM还是有治疗意义的。
AT132是安斯泰来以30亿美元现金收购美国基因疗法公司Audentes Therapeutics而获得。AT132的临床试验可谓一波三折。
2020年,高剂量组中3名受试患儿在治疗后出现了淤胆型肝炎并诱发肝衰竭,并先后因继发败血症或胃肠道大出血死亡。为此,美国食品和药物管理局(FDA)暂停了这项临床试验。2021年,低剂量组中出现1例死亡。此试验目前一直处于搁置中。
加州大学洛杉矶分校神经病学和儿科学教授,ASPIRO的首席研究员Perry B. Shieh博士表示:“试验初步数据首次证明AT132有可能为XLMTM患者提供临床改善,包括改善呼吸机依赖性和实现主要运动里程碑。此外,接受治疗参与者中,与肝脏健康有关的重要问题已经确定,并需要继续仔细评估。”
安斯泰来后续将与FDA沟通以尽快解除AT132的临床搁置。
参考资料:
1.公司官网
2.药融云全球药物研发数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论