
不断开拓新产品,体系内研发与外延合作并购,加深护城河,才是创新药企长久之道。
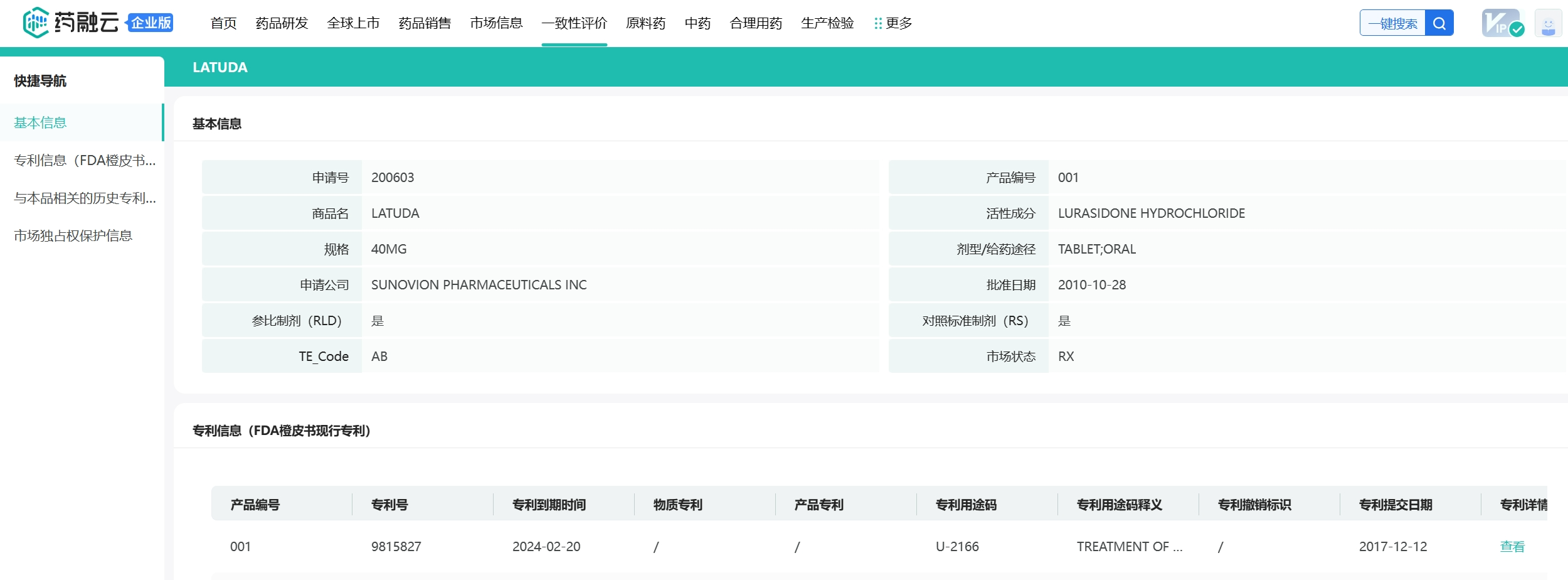
从药融云数据库获悉,日本住友制药的支柱产品抗精神分裂症药品Latuda的在美独家销售权终止(美国化合物专利2024年2月到期),而这势必会造成公司销售额大幅下滑。早在2019年底,住友制药就与英国Roivant Science制药公司达成协议,向Roivant总公司出资30亿美元,获得Roivant一定比例的股份以及收购旗下几家子公司的选择权。此次合作住友制药不仅可以获得子宫肌瘤治疗药Relugolix,以及泌尿系统疾病治疗药Bevegron的全球销售权,还从Roivant公司获得其在制药及健康管理相关领域的平台和技术支持。
2020年底,FDA批准Relugolix用于治疗前列腺癌(商品名Orgovyx),2022年度该产品销售额达到1.82亿美元,成为公司在北美的主要畅销药物之一,而这一未雨绸缪的做法无疑缓解了公司的“专利到期焦虑”。
住友制药是有400年商业历史的住友集团的一员,在2005年由大日本制药株式会社和日本住友制药株式会社合并,主要通过医疗药品、再生医学/细胞疗法和非医疗解决方案来为人类生活做出贡献,重点关注精神病学和神经病学、肿瘤学领域。而合并的两个公司历史可追溯到一百多年前。1897年,21位制药行业的杰出领导者在大阪道商町创立了Osaka Pharmaceuticals,第二年在大阪惠边市设立制药工厂,收购了东京的公私合营公司大日本制药株式会社,并将公司名称变更为大日本制药株式会社。日本住友制药株式会社成立于1984年,由住友化学株式会社(成立于1913年)制药业务的研究、开发和制造部门以及住友化学株式会社药品的独家经销商稻畑产业株式会社的药品销售部门组成。
住友制药自合并后就接连收购了美国的Sepracor、Boston Biomedical、Elevation Pharmaceuticals和Tolero Pharmaceuticals等公司,并在海外成立子公司。20世纪90年代,公司逐步在中国开展事业,2005年底,住友制药(苏州)有限公司在苏州成立,中国也成为住友集团在除日本和北美外的全球第三大重要市场。此前住友制药在中国有近800名员工,2021年的销售额约20亿人民币。
PART1主要产品
住友制药的优先研究领域是精神病学、神经病学和肿瘤学,同时,还致力于通过再生医学/细胞疗法和非医疗解决方案为改善医疗保健和人类生活作出贡献。以下是公司各领域的主要上市产品:
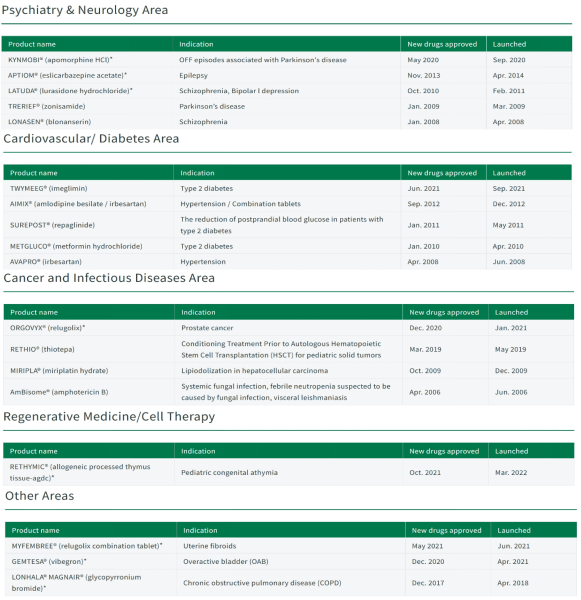
分地区来看,在日本,除了精神病学和神经病学领域,还重点关注糖尿病和罕见疾病领域,上年度畅销产品有TRERIEF(zonisamide,唑尼沙胺)、LATUDA(lurasidone,鲁拉西酮)和TWYMEEG(imeglimin);北美地区的畅销产品有ORGOVYX(relugolix)、MYFEMBREE(relugolix + 雌二醇 + norethindrone acetate)和GEMTESA(vibegron);在中国地区专注于传染病,以及精神病学和神经病学领域,主要畅销产品有MEROPEN(美罗培南)。
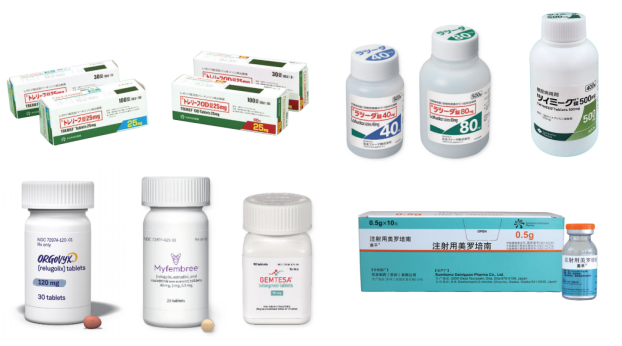
图:各地区畅销药物
PART2研发管线(图片信息截至2023年10月31日)
1.精神病和神经病学
(1)小分子
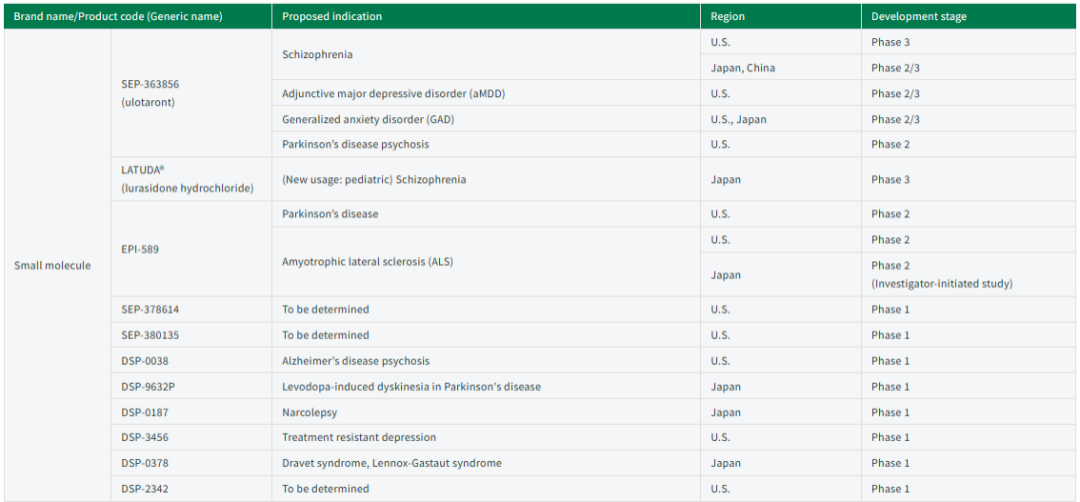
Ulotaront(SEP-363856)是一种 TAAR1(痕量胺相关受体1)激动剂,具有5-羟色胺(血清素)5-HT1A激动剂活性,不与多巴胺D2或5-羟色胺5-HT2A受体结合。前Sunovion公司(2009年收购的美国制药商,现为住友制药子公司)与Psychogenics公司合作,利用其体内表型分析平台SmartCube和相关AI算法发现。目前针对精神分裂症的研究在美国进行到临床试验3期,在日本和中国进行到临床试验2/3期;在美国针对aMDD(辅助性重性抑郁障碍)的研究处于临床试验2/3期;在美国和日本针对GAD(广泛性焦虑障碍)的研究进行到临床试验2/3期;在美国针对帕金森病精神病的研究进行到临床试验2期。
Ulotaront于2019年5月被FDA授予治疗精神分裂症的突破性疗法称号,是第一个也是唯一一个进入精神分裂症患者临床试验3期研究的TAAR1激动剂,也是第一个进入GAD的临床试验2/3期研究的TAAR1激动剂,并作为MDD的辅助治疗。2023年7月,住友制药与大冢制药宣布了临床试验3期的DIAMOND 1和DIAMOND 2研究的顶线结果,在患有精神分裂症的剂型精神病成人患者中,每日一次给药未达到其主要终点,在两项研究中,都观察到了较大的安慰剂效应,这可能掩盖了该分子的治疗效果,总体来说该药物是安全的,耐受性良好。
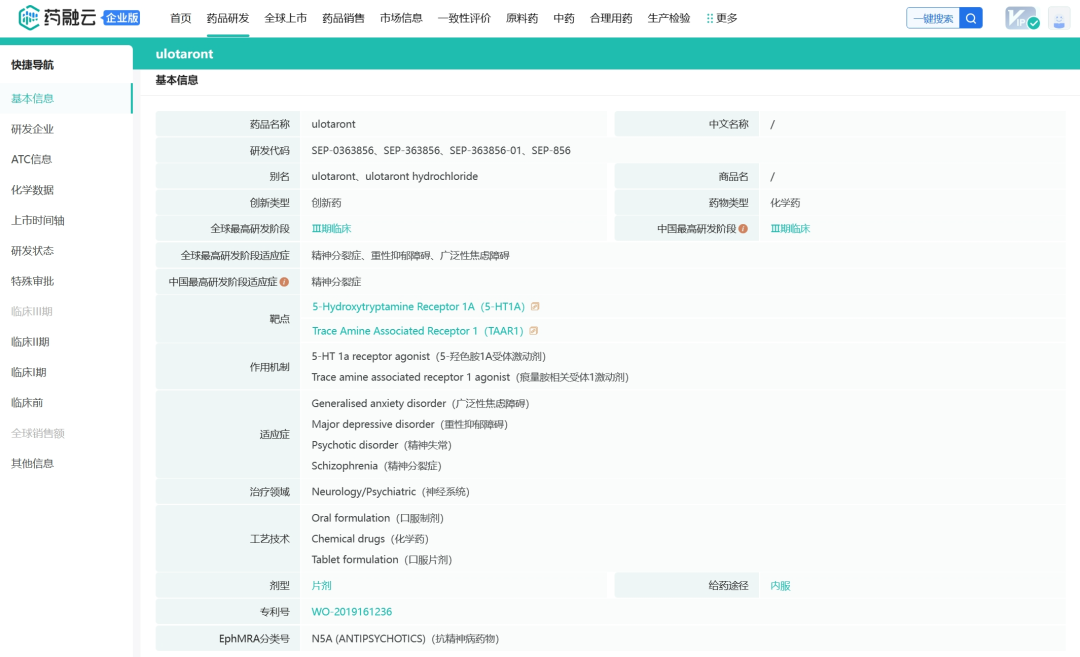
药融云数据库:药物基本信息
EPI-589有望通过消除线粒体功能降低过度产生的氧化应激而显示出功效,它有望被开发用于由氧化还原应激引起的神经退行性适应症。在美国地区针对帕金森病的研究进行到临床试验2期;针对肌萎缩侧索硬化症(ALS)的研究在美国和日本均进行到临床试验2期(在日本的研究由德岛大学主导)。
注:氧化应激(OS) 是指体内氧化与抗氧化作用失衡的一种状态,倾向于氧化,导致中性粒细胞炎性浸润,蛋白酶分泌增加,产生大量氧化中间产物。氧化应激是由自由基在体内产生的一种负面作用,并被认为是导致衰老和疾病的一个重要因素。
Sep-378614和SEP-380135是新型的中枢神经系统活性分子,均由Sunovion公司与Psychogenics公司合作,利用其体内表型分析平台SmartCube和相关AI算法发现。Sep-378614的临床前研究表明,它可能具有快速起效的抗抑郁活性。当前在美国研究进行到临床试验1期。SEP-380135的临床前研究显示了广泛的体内活性,表明对痴呆的许多行为和心理症状有效,包括激越/攻击性、精神运动性多动症和抑郁症,当前针对相关适应症的研究在美国进行到临床试验1期。
DSP-0038是5-羟色胺5-HT2A受体拮抗剂和5-羟色胺5-HT1A受体激动剂。是住友制药利用Exscientia的人工智能技术发现的一种新型化合物。基于5-HT2A受体拮抗剂和5-HT1A受体激动剂的叠加效应,预期DSP-0038表现出更强的抗精神病作用。该化合物在治疗痴呆(BPSD)的行为和心理症状(包括激越、攻击性、焦虑和抑郁)方面也可能具有更广泛的功效。此外,DSP-0038对多巴胺受体D2的亲和力可忽略不计,因此与现有的抗精神病药物相比,它可以显示出更高的安全性和耐受性。目前在美国针对阿尔兹海默症精神病的研究进行到临床试验1期。
DSP-9632P是5-羟色胺5-HT1A受体部分激动剂。可能通过抑制左旋多巴衍生的多巴胺的过度释放,对左旋多巴给药后表达的运动障碍发挥作用。临床前研究表明,DSP-9632P可抑制左旋多巴引起的运动障碍症状。通过稳定的血药浓度,DSP-9632P的透皮贴剂制剂可能成为治疗帕金森病中左旋多巴诱导的运动障碍的有效选择,并且还可能提高患者给药的便利性。在日本针对左旋多巴诱导的帕金森病运动障碍的研究进行到临床试验1期。
DSP-0187是一种食欲素2受体激动剂,有望改善由食欲素缺乏引起的发作性睡病的白天过度嗜睡(EDS)和猝倒,也有望证明对除发作性睡病以外的EDS的疗效。在日本针对发作性睡病的研究进行到临床试验1期。住友制药于2022年4月授予Jazz Pharmaceuticals PLC在除日本、中国和某些其他亚太市场以外的地区的独家开发和商业化权利。
DSP-3456是一种mGluR2/3 NAM(代谢型谷氨酸受体2/3负变构调节剂)。DSP-3456 有望通过增强谷氨酸释放来选择性激活前额叶皮层,同时避免副作用(精神病症状、认知功能障碍),从而表现出类似氯胺酮的抗抑郁作用。在美国针对难治性抑郁症的研究进行到临床试验1期。
DSP-0378是一种γ-氨基丁酸A型受体(GABAA受体)正向变构调节剂,它作用于突触和突触外区域表达的各种GABAA受体亚型,其方式不同于常见的GABAA受体增强剂,例如苯二氮䓬类药物和神经类固醇,预计该药物具有广泛的抗癫痫作用,包括Dravet综合征和Lennox-Gastaut综合征(LGS)等难治性罕见疾病。在日本针对Dravet综合征和Lennox-Gastaut综合征的研究进行到临床试验1期。
DSP-2342是一种5-羟色胺5-HT2A和5-HT7受体拮抗剂。基于5-HT2A和5-HT7受体拮抗剂的累加效应,该药物有望显示出更广泛的抗精神病作用,包括精神病、焦虑和抑郁,此外,还对5-HT2A和 5-HT7受体具有高选择性,有望显示出高水平的安全性和耐受性。DSP-2342是住友制药利用Exscientia的AI技术发现的一种新型化合物,当前在美国研究进行到临床试验1期。
(2)再生医学/细胞疗法
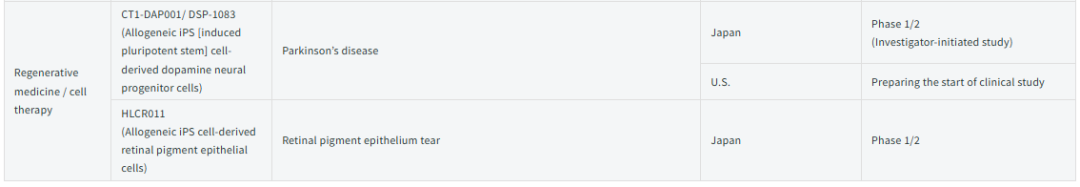
住友制药与合作伙伴合作,开发了针对帕金森病和视网膜色素上皮撕裂的再生医学/细胞疗法,分别是CT1-DAP001/DSP-1083和HLCR011,这两种均是同种异体iPS细胞衍生产品。其中,CT1-DAP001/DSP-1083针对帕金森的研究在日本进行到临床试验1/2期,在美国准备开始临床研究;HLCR011在日本针对视网膜色素上皮撕裂的研究进行到临床试验1/2期。
2.肿瘤学
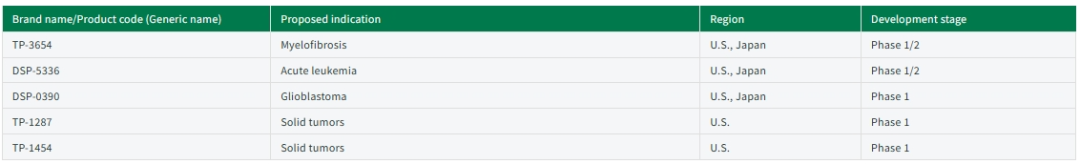
TP-3654通过抑制 PIM(Moloney白血病病毒的前病毒整合位点)激酶来抑制炎症信号通路,PIM激酶经常在各种血液系统恶性肿瘤和实体瘤中过表达,使癌细胞逃避细胞凋亡并促进肿瘤生长。FDA于2022年5月授予TP-3654 孤儿药资格,用于治疗骨髓纤维化。在美国和日本针对骨髓纤维化的研究进行到临床试验1/2期。
DSP-5336是一种小分子抑制剂,可抵抗Menin(一种肿瘤抑制蛋白)和混合谱系白血病(MLL)蛋白的结合,伴有MLL重排或核磷蛋白1(NPM1)突变的急性白血病主要通过menin-MLL相互作用来上调促白血病发生的基因。DSP-5336 在临床前研究中已被证明具有抗癌活性,通过抑制 meninMLL 相互作用来下调基因。FDA于2022年6月授予DSP-5336孤儿药资格,用于治疗急性髓系白血病,目前在美国和日本的研究进行到临床试验1/2期。
DSP-0390是EBP(依莫帕米结合蛋白)抑制剂, EBP是一种参与胆固醇生物合成的内质网膜蛋白,大多数癌细胞的特征是负责其生物合成的各种通路上调,并且对支持细胞增殖的胆固醇需求很高,因此,DSP-0390对EBP的抑制预计会导致胆固醇稳态的破坏并诱导癌细胞死亡。FDA于2022年5月授予DSP-0390孤儿药资格,用于治疗脑癌,目前在美国和日本针对胶质母细胞癌的研究进行到临床试验1/2期。
TP-1287是一种小分子口服药物,可抑制CDK9(细胞周期蛋白依赖性激酶9)。TP-1287在临床前研究中显示出良好的口服生物利用度可以产生一种有效的CDK9抑制剂。FDA分别于2023年2月和3月授予了TP-1287儿科罕见病资格认定和孤儿药认定,用于治疗尤文肉瘤(也称尤因肉瘤)。TP-1454通过酶的四聚化诱导PKM2(丙酮酸激酶M2)的活性,该酶主要以酶活性较低的二聚体状态存在于癌细胞中,PKM2 的四聚化导致癌细胞中有氧糖酵解的减少并恢复免疫抑制微环境,TP-1454有望与免疫检查点抑制剂显示出协同作用。目前TP-1287和TP-1454在美国针对实体瘤的研究均进行到临床试验1期。
3.其他
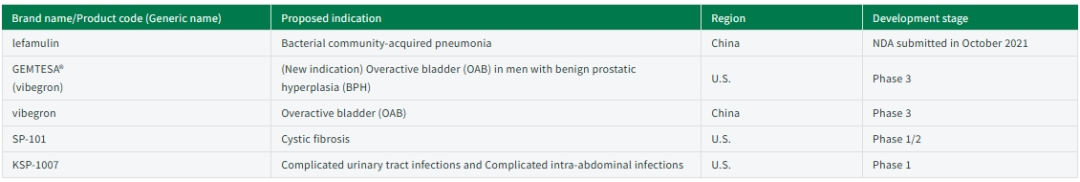
Lefamulin是一种截短侧耳素类抗菌剂,可通过静脉注射或者口服给药,其作用机制为抑制细菌生长所必须的蛋白质的合成。Lefamulin最初由Nabriva Therapeutics开发,在美国,FDA于2019年8月批准了XENLETA(Lefamulin,来法莫林)用于治疗CAP(社区获得性细菌性肺炎)成年患者,由Nabriva Therapeutics在美国地区销售。2018年3月,仑胜医药获得在大中华区(包括中国大陆、香港、澳门、台湾省)开发和商业化lefamulin的权利。2021年5月7日,住友制药与仑胜医药签订资产转让协议,住友制药(苏州)获得仑胜医药持有的包括lefamulin在内的多个在研新药在大中华区的独家研发和销售权。2021年10月,住友制药在中国提交了Lefamulin的新药上市申请,2023年11月14日,国家药品监督管理局(NMPA)批准了XENLETA(Lefamulin,醋酸来法莫林注射剂和片剂)用于治疗成人社区获得性肺炎。
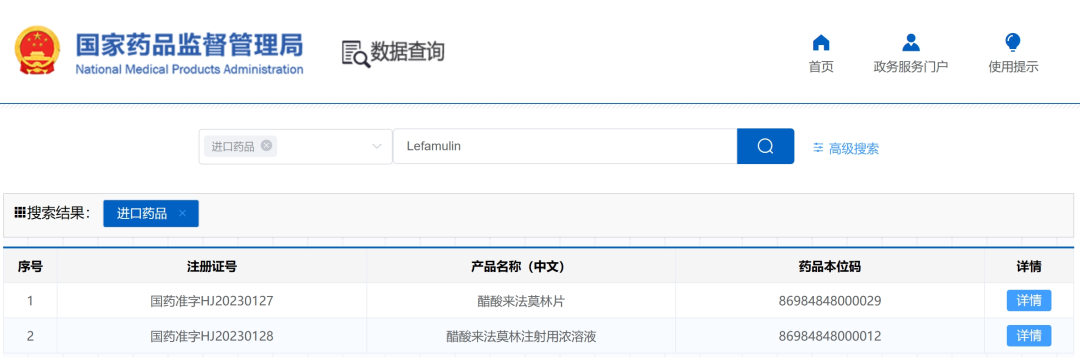
图片来源:国家药品监督管理局
Vibegron是一种口服小分子β3肾上腺素能受体激动剂,选择性作用于膀胱中的β3肾上腺素能受体,使膀胱松弛,增强尿液储存,并改善膀胱过度活动症(OAB)患者的尿急、尿频和急迫性尿失禁症状。2020年12月,Urovant Sciences(2019年12月住友制药从Roivant公司收购)的Gemtesa(vibegron,维贝格龙)在美国获得了膀胱过度活动症的批准。目前在中国针对膀胱过度活动症的研究进行到临床试验3期;在美国针对BPH(良性前列腺增生)男性膀胱过度活动症的研究也进行到临床试验3期。
SP-101是一种新型的腺相关病毒(AAV)载体,可有效地从顶端(管腔)表面转导人气道上皮细胞,它旨在将缩短但功能齐全的CFTR(囊性纤维化跨膜传导调节因子)基因传递给CF(囊性纤维化)患者的气道。基于临床前数据,阿霉素的加入显著改善了SP-101转导和随后CFTR基因的表达,目前正在开发SP-101和阿霉素通过喷雾器给药的联合产品,SP-101有望恢复CFTR功能并改善CF患者肺部的疾病,在美国针对囊性纤维化的研究进行到临床试验1/2期。
KSP-1007可抑制β-内酰胺酶,该酶由可降解碳青霉烯类抗生素的细菌产生。KSP-1007与美罗培南水合物(一种全球通用的碳青霉烯类抗生素,住友制药在国内市场的产品名称为Meropen)联合用药,有望成为治疗耐碳青霉烯类细菌感染的有效选择。FDA于2022年8月授予KSP-1007合格传染病产品(QIDP)资格和快速通道指定,用于复杂性尿路感染、复杂性腹腔内感染、医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎的适应症。目前在美国针对复杂性尿路感染和复杂性腹腔内感染的研究进行到临床试验1期。
自合并后,住友制药一直致力于实现业务全球化,当前在日本、北美、中国和亚洲设有本地总部、销售和开发职能部门,并从事地区特色的销售营销活动。以下是研究开发机构全球分布图:
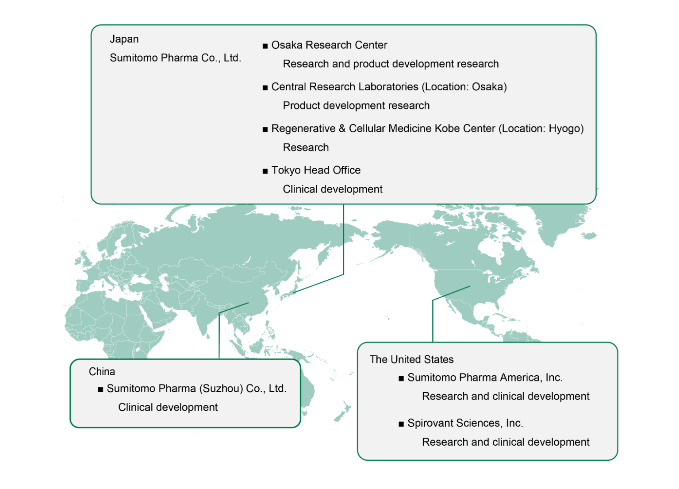
PART3财务状况
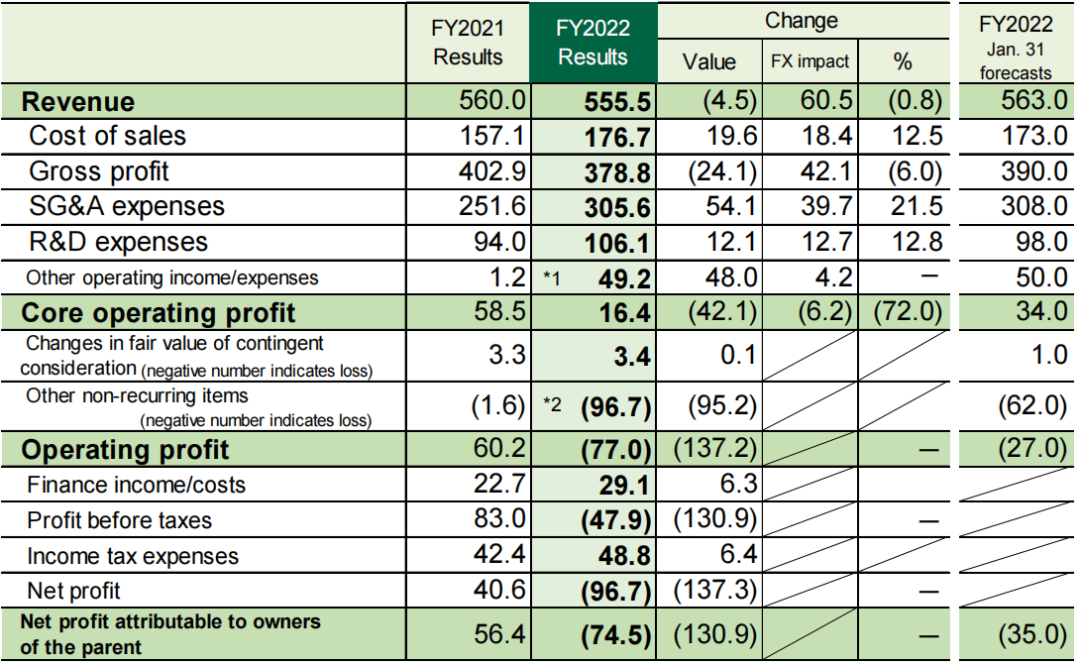
2022财年(2022.04~2023.03)住友制药的收入为5555亿日元(38.5亿美元,均以1.00美元=144.34日元计算),与上年同期相比降低了0.8%。核心营业利润164亿日元(1.14亿美元);营业利润为(亏损)770亿日元(5.34亿美元);税前利润(亏损)479亿日元(3.32亿美元),净利润(亏损)967亿日元(6.70亿美元)。
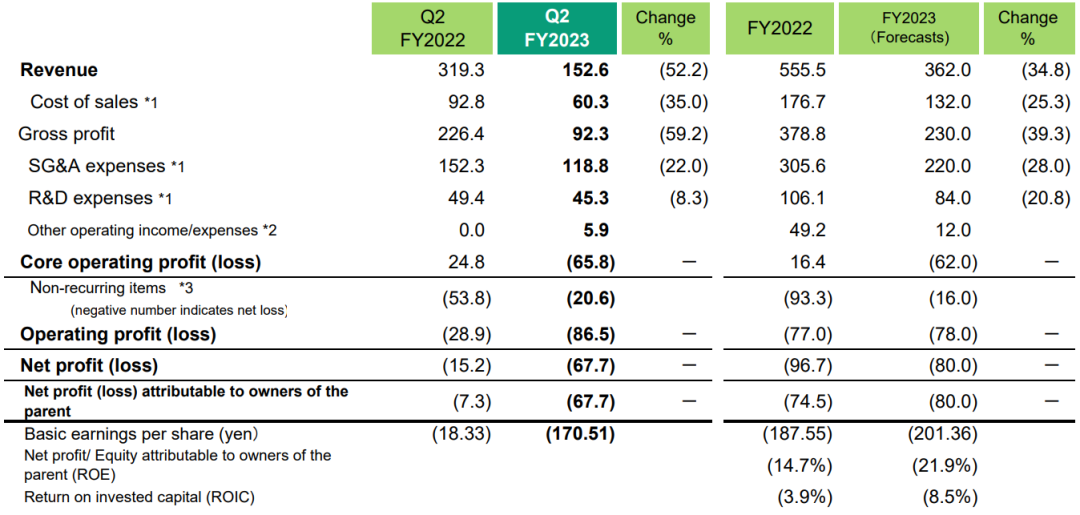
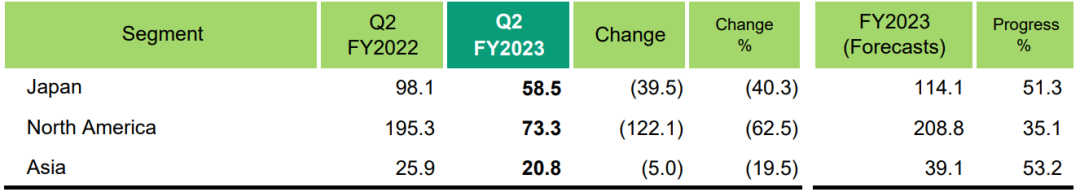
2023前两个季度收入1526亿日元(10.8亿美元),与上年同期相比下降52.2%,收入下降的主要原因是LATUDA(鲁拉西酮)在美国的独家经营权丧失,住友制药食品化学株式会社转让。尽管销售、一般和行政费用比预期减少,但集团公司在北美的合并,以及住友制药动物保健株式会社股份转让产生的其他收入,由于收入下降导致毛利大幅下降,截至2023年9月30日止六个月的核心营业利润为(亏损)658亿日元(4.56亿美元)。尽管前六个月确认的减值亏损主要为专利权,但由于核心经营亏损及北美业务结构改善的开支,营业利润(亏损)为865亿日元(5.99亿美元),较去年同季有所增加。由于日元贬值导致的外汇收益被营业利润的下降所抵消,公司税前利润(亏损)为561亿日元(3.89亿美元)。由于税前亏损,净亏损较去年同期有所增加,净利润(亏损)为677亿日元(4.69亿美元),而截至2022年9月30日的六个月为152亿日元(1.05亿美元)。
分地区来看,日本地区销售额为585亿日元(4.05亿美元),与上年同期相比下降了40.3%;北美地区销售额733亿日元(5.08亿美元),同比下降62.5%;亚洲地区销售额为208亿日元(1.44亿美元),同比下降19.5%。
PART4中期破局经营计划(2023~2027)
2019年,住友制药制定了新的愿景,并励志成为一家能够满足日益多样化的医疗保健需求的公司,公司的目标是到2033年将自己打造成全球化专业企业。短期来看,公司制定了2027年中期经营计划,该计划从2023年开始实施,在中期经营计划的第一年,住友制药预计核心营业亏损为620亿日元(4.30亿美元),因为LATUDA(鲁拉西酮)在美国的独家销售期结束,销售额将几乎归零。
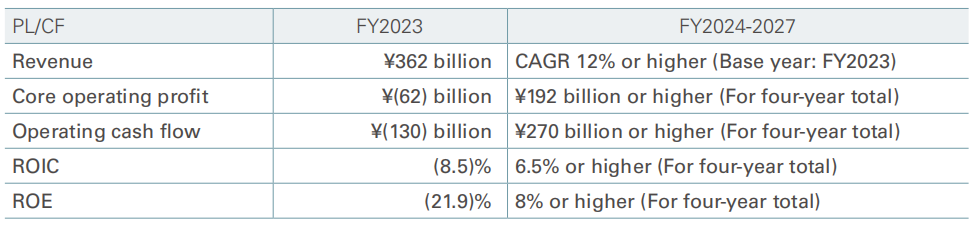
在这种情况下,住友制药将努力建立支持持续增长的收入基础,主要是通过最大限度地提高三个主要产品(ORGOVYX、MYFEMBRE、GEMTESA)的业务,并通过研发改变其业务结构,以业务形式将公司的创新付诸实践。同时,将以美国集团公司合并为契机,重新设计集团运营结构,努力向灵活高效的业务基础转变。在北美,公司的目标是到2024财年实现4600亿日元(31.9亿美元)的收入和400亿日元(2.77亿美元)的核心营业利润。同时还设定了从2023财年开始,到2027财年的收入复合年增长率至少为12%的目标,以及从2024财年到2027财年的累计核心营业利润至少为1920亿日元(13.3亿美元)的目标。以下是公司中期经营计划财政目标:
参考来源:
NMPA/CDE;
药融云数据库;
FDA/EMA/PMDA;
相关公司公开披露(除标注外,正文图片均来自企业官网)等
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论