
2024年2月22日,CDE官网显示,石药集团欧意药业有限公司递交的4类仿制药哌柏西利片上市申请获受理。据药融云数据库显示,此前已有齐鲁制药、南京正大天晴递交哌柏西利片上市申请。
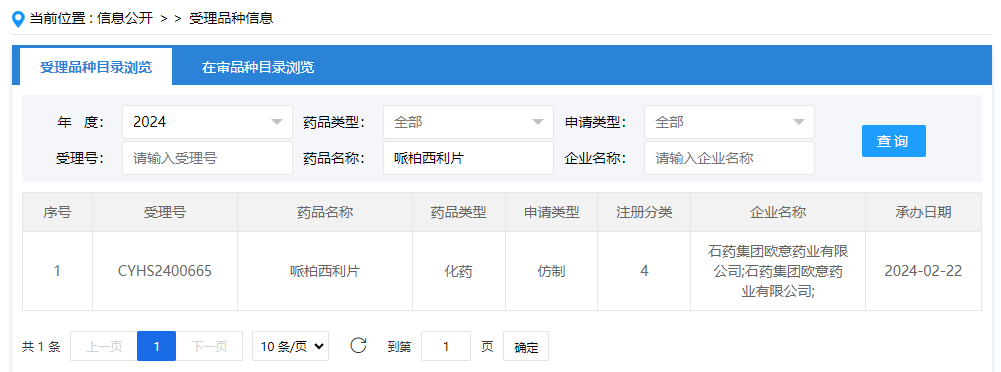 截图来源:CDE官网
截图来源:CDE官网
哌柏西利(palbociclib)在国内有片剂和胶囊剂两种剂型上市。哌柏西利胶囊首仿在2020年 12月18日被齐鲁制药拿下,截至目前胶囊剂在国内已有32条生产批文(在使用中),涉及江苏奥赛康药业、正大天晴药业、重庆药友制药、湖南科伦制药等12家药企。
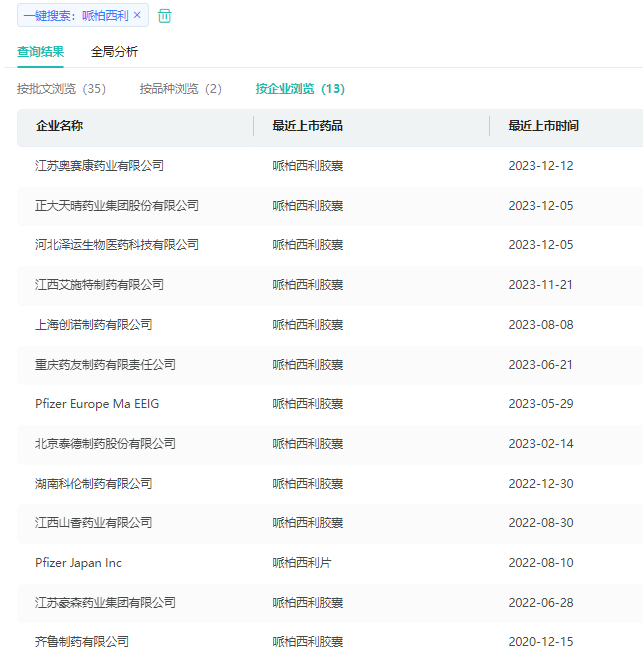
截图来源:药融云中国药品批文数据库
哌柏西利片原研是辉瑞,哌柏西利是全球范围内第一个被批准用于HR+/HER2-型局部晚期或转移性乳腺癌的CDK4/6靶向抑制剂。抑制CDK4/6靶点可以控制细胞周期转化过程,达到抑制肿瘤细胞无限增殖的效果。
近年来,乳腺癌的发病率逐年攀升,已成为全球范围内女性最常见的恶性肿瘤。对女性而言,前五大患病率最高的肿瘤依次是乳腺癌、肺癌、结直肠癌、宫颈癌、皮肤黑色素瘤。其中乳腺癌最多,约占比31%。乳腺癌已成为全球第一大癌,2020年全球新发病例数高达226万例。全球乳腺癌药物市场规模2022年已达315亿美元,据弗若斯特沙利文预测,到2030年将达到699亿美元。
据药融云统计,2022年前三季度国内CDK4/6抑制剂的院内销售额已超3亿元,同比增长393%。该品种是当之无愧的重磅品种,自上市以来,其全球销售额连年增长,至 2019 年其年销售额已达 49.61 亿美元。哌柏西利在2023年全国院内市场销售额近1亿元,同比上涨77%。
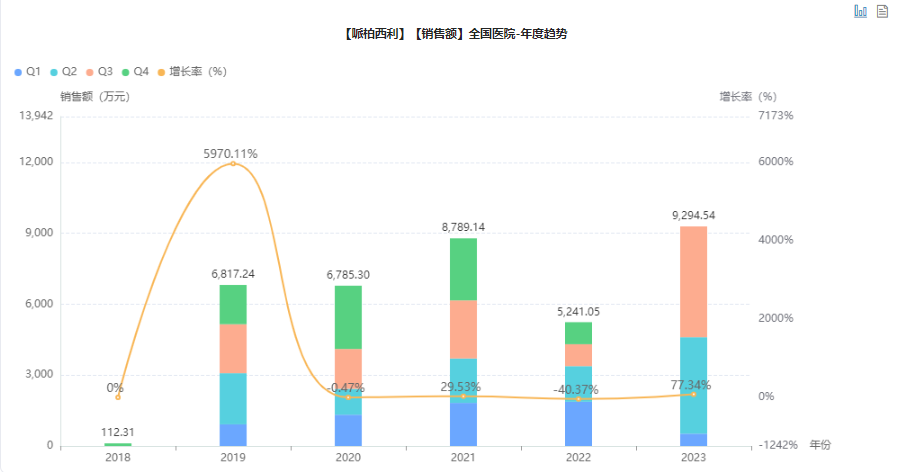
截图来源:药融云全国医院销售数据库
截至目前,全球已有 5 款 CDK4/6 抑制剂(1 类新药)获批上市,包括辉瑞的哌柏西利、礼来的阿贝西利、恒瑞医药的羟乙磺酸达尔西利片、先声药业从 G1 Therapeutics 引进的曲拉西利(Trilaciclib)以及诺华的瑞波西利。此外,嘉和生物从 G1 Therapeutics 引进的来罗西利(lerociclib),已于 2023 年 3 月提交上市申请,用于治疗 HR+/HER2-乳腺癌。
CDE官网显示,2024年石药集团欧意药业截至目前共获得13个受理号(含补充申请),涉及地塞米松磷酸钠注射液 、己酮可可碱缓释片 、SYH2043片 、盐酸伊立替康脂质体注射液、枸橼酸托法替布缓释片等多个品种。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论