
2023年年底,又一家制药巨头(百时美施贵宝)宣布以每股62.50美元的现金收购RayzeBio(RayzeBio是一家成立于2020年的临床阶段的放射性药物治疗公司),总股本价值约为41亿美元。
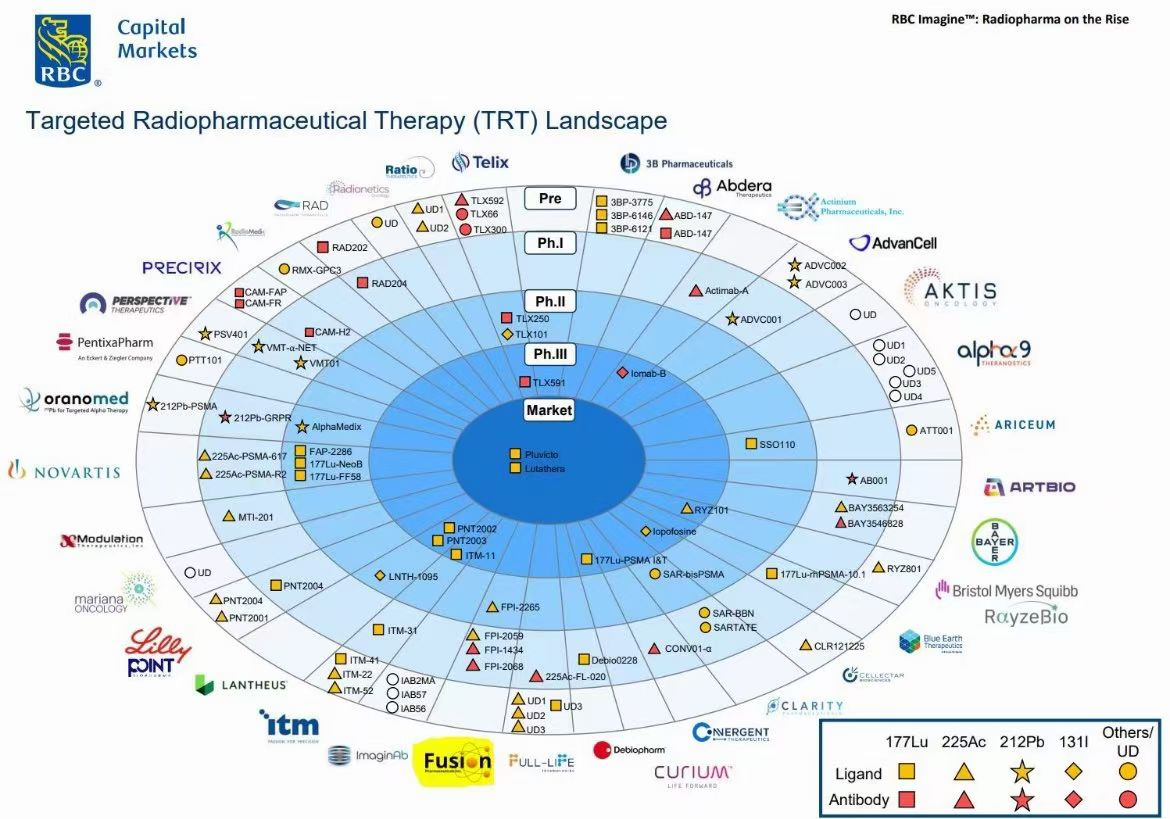
就在前几个月,深耕糖尿病和肥胖代谢领域的礼来宣布收购了放射性疗法公司POINT Biopharma,早在十年前,德国药企拜耳就已经布局核药赛道,并推出了FDA和EMA批准的唯一一个α粒子放射治疗药物,诺华更是推出了多个治疗用RDC(放射性核素偶联药物)(通过收购整合开发),阿斯利康、默沙东和强生等跨国药企也通过股权投资、技术引进多种方式切入该领域。据Technavio发布的《2023-2027年全球放射性药物市场》的最新市场研究报告统计,从2021 年到2026 年,全球放射性药物市场规模预计将增加43.7 亿美元。(相关阅读:新型的首创放射性药物MNPR-101临床前数据优异,股价大涨96%!)
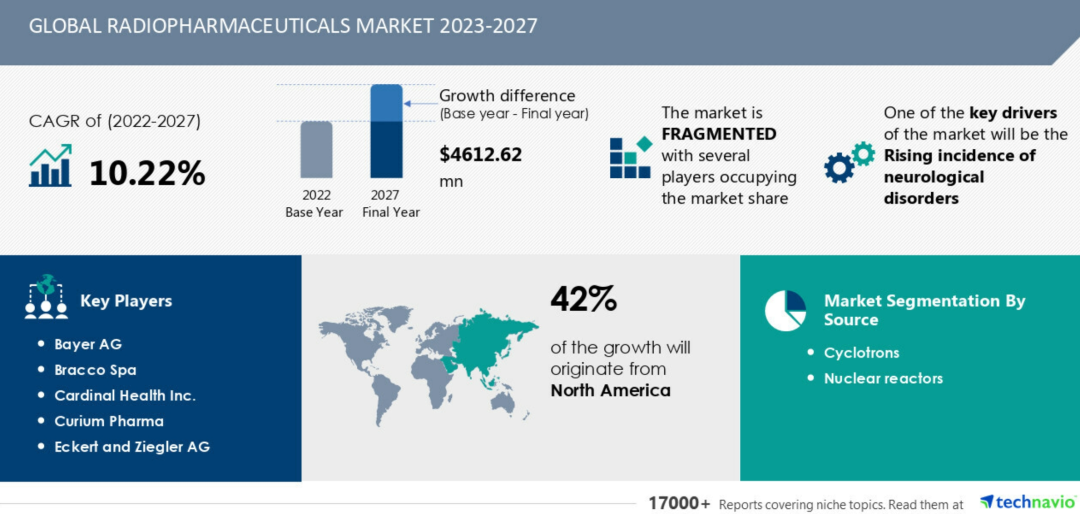
图源Technavio
之前药融圈分享过多篇核药企业长文:深耕60多年的Lantheus以及市值翻几十倍的Telix Pharmaceuticals。今天想和朋友们分享一家被多个制药巨头青睐的加拿大制药公司Fusion pharmaceuticals,让我们一起看看他的吸引力到底在何处。
从药融云数据库获悉,总部位于加拿大(安大略省)的Fusion pharmaceuticals(以下简称Fusion)成立于2014年,是一家临床阶段的生物制药公司,致力于开发下一代放射性药物作为治疗癌症的精密药物。该公司开发了靶向Alpha疗法(Targeted Alpha Therapies,TAT)平台,以及公司专有的Fast-Clear™连接子技术,使其能够将发射α粒子的同位素与抗体和其他靶向分子连接起来,以选择性地将疗法传递给肿瘤。
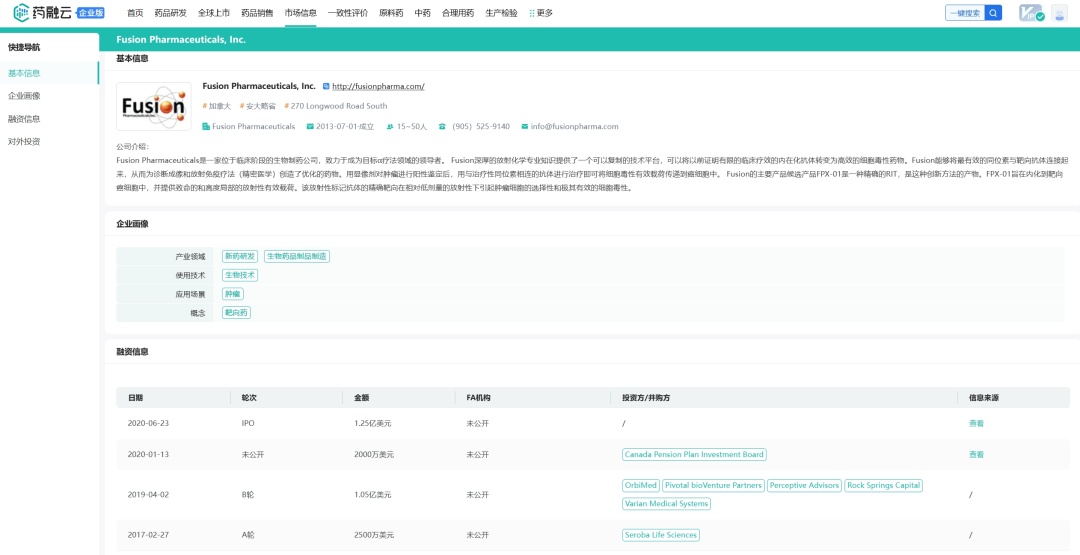
药融云数据www.pharnexcloud.com:融资情况
本文稿件完稿于2024年1月17日,以下内容或非最新。属于完成稿件2个月之后3月19日,阿斯利康宣布收购该公司,价值为24亿美元(约合174亿人民币)(基于生产能力、产品管线前景与协同)。双方最早合作始于2020年。


Fusion由Valliant博士创立,但这并不是Valliant博士第一次与放射性药物打交道,在创立公司之前,Valliant博士曾创立了一个放射性药物研究中心CPDC (the Centre for Probe Development and Commercialization),专注于发现、开发和分发下一代分子成像探针。自成立以来,该公司总融资五轮,2017年融资两轮(除以上统计的A轮融资外,2017年9月A+轮融资2100万美元;强生的JJDC在2017年领投了Fusion),2019年进行了B轮融资,金额达到1.05亿美元,2020年6月通过IPO在纳斯达克上市,此次融资1.25亿美元。同时在2020年11月与阿斯利康合作开发和商业化用于治疗癌症的下一代α发射放射性药物和联合疗法。
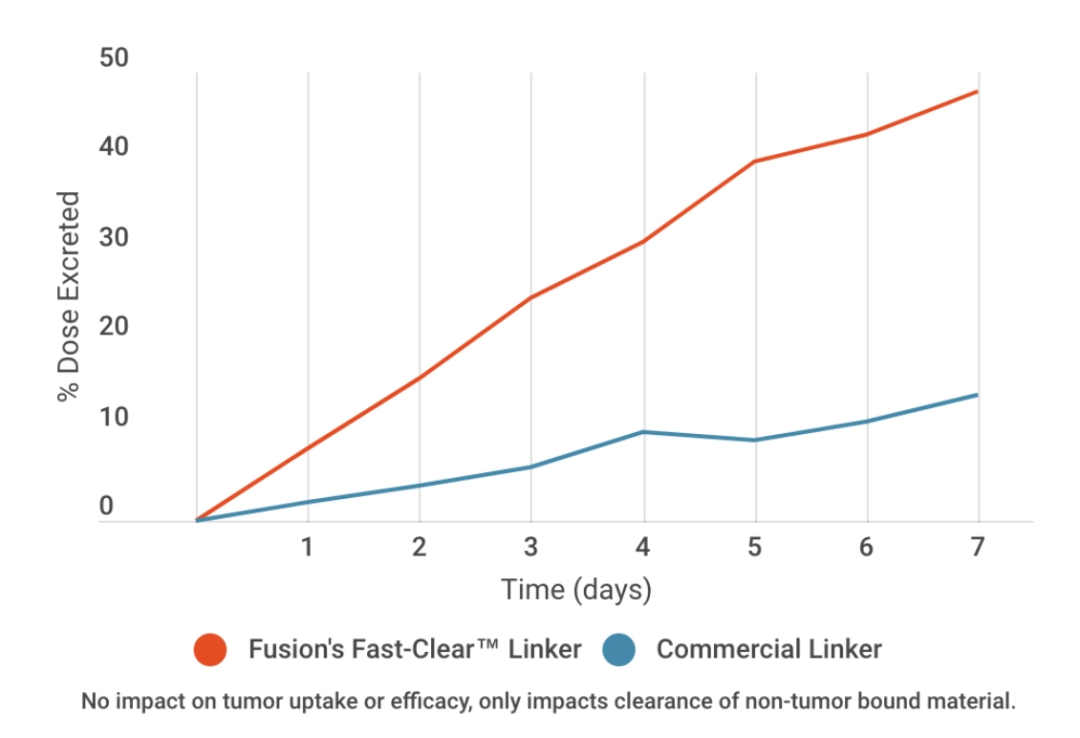
Fusion专有的Fast-Clear连接子技术促进了不与癌细胞特异性结合的医用同位素的快速排泄,与扩大治疗窗口的商业技术相比,Fast-Clear连接子技术(分子和医用同位素之间的“连接器”)旨在以更快的速度清除更多的医用同位素。鉴于Fast-Clear连接子技术的强大功能和多功能性,Fusion正在将该技术应用于一系列分子和分子类别(抗体、小分子等)。
研发管线
除了目前开展到临床试验2期的一个管线以及开展到临床试验1期的两个管线外,Fusion其余管线均处于发现和临床前研究阶段,以下是研发管线的详细进展情况:

FPI-2265
FPI-2265是一种靶向PSMA(前列腺特异性膜抗原)的靶向α疗法(TAT),用于治疗疾病进展的mCRPC(转移性去势抵抗性前列腺癌)患者。2024年1月4日,Fusion宣布已与FDA就其提交的FPI-2265的临床试验2/3期方案达成一致,更新后的开发计划包括临床试验2期剂量优化导入,临床试验2期研究预计将于2024年第二季度启动,并于2024年底完成入组,公司将寻期与FDA举行临床试验2期研究结束会议,根据临床试验2期数据的分析确定临床试验3期给药方案,预计将于2025年开始临床试验3期研究。Fusion还在寻求机会,通过FPI-2265和奥拉帕尼的组合将候选疗法推向更早期的治疗线,预计将在2024年上半年启动联合试验。
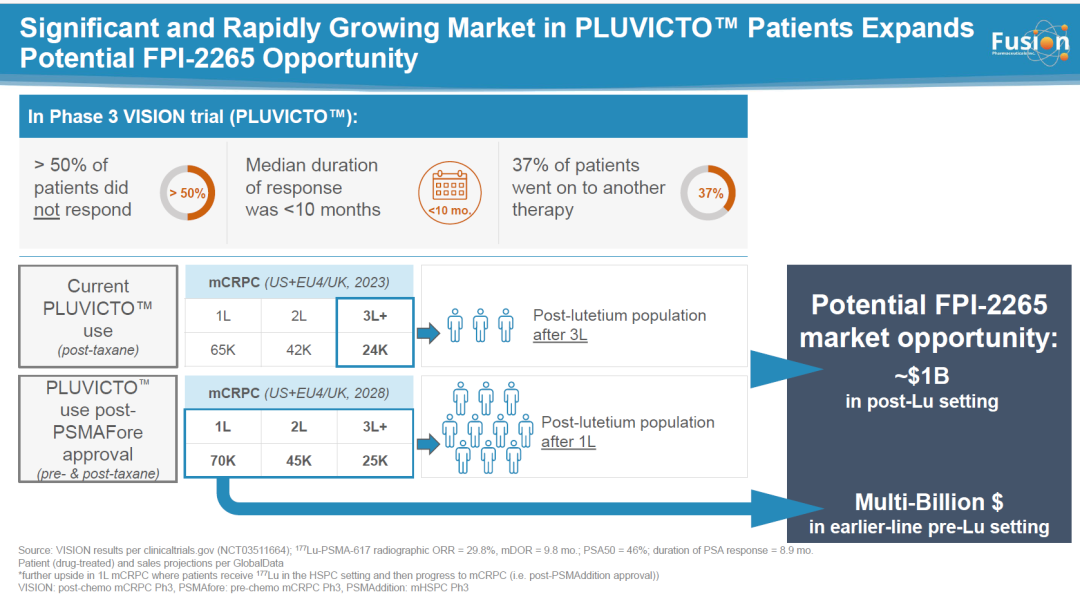
2023年2月,Fusion获得了FPI-2265的临床试验2期研究(TATCIST试验)的IND(新药临床研究审批),TATCIST试验旨在评估该药在患有mCRPC(转移性去势抵抗性前列腺癌)且疾病进展的患者中的疗效,包括对PSMA靶向放射性药物不敏感的患者,以及使用基于镥-177的PSMA放射性药物(如诺华的Pluvicto)进行预处理的患者。根据迄今为止报道的文献和TATCIST数据,已知每8周给药100 kBq/kg是一种安全且有效的剂量方案,为了进一步优化FPI-2265的获益/风险比,Fusion将探索具有更高给药频率的替代方案,同时保持累积剂量和总治疗持续时间相同,要评估的其他方案包括每4周50 kBq/kg的剂量和每6周75 kBq/kg的剂量。主要终点是安全性和PSA(前列腺特异性抗原)水平下降≥50%的患者比例,关键次要终点为ORR(客观缓解率)和rPFS(影像学无进展生存期)。
FPI-1434
FPI-1434是一种抗体偶联放射性药物,旨在靶向表达IGF-1R(IGF-1R是一种在许多肿瘤类型上过表达的受体)癌细胞并递送发射α的医用同位素,利用FastClear接头将靶向IGF-1R的人类单克隆抗体与锕225(一种强大的α发射同位素,具有理想的半衰期和衰变链特性)连接起来。目前正处于临床试验1期,计划完成并进一步评估队列2的结果,召开安全审查委员会(SRC)会议以评估新出现的数据,预计在2024年年中分享有关数据和FPI-1434开发计划的更多细节。
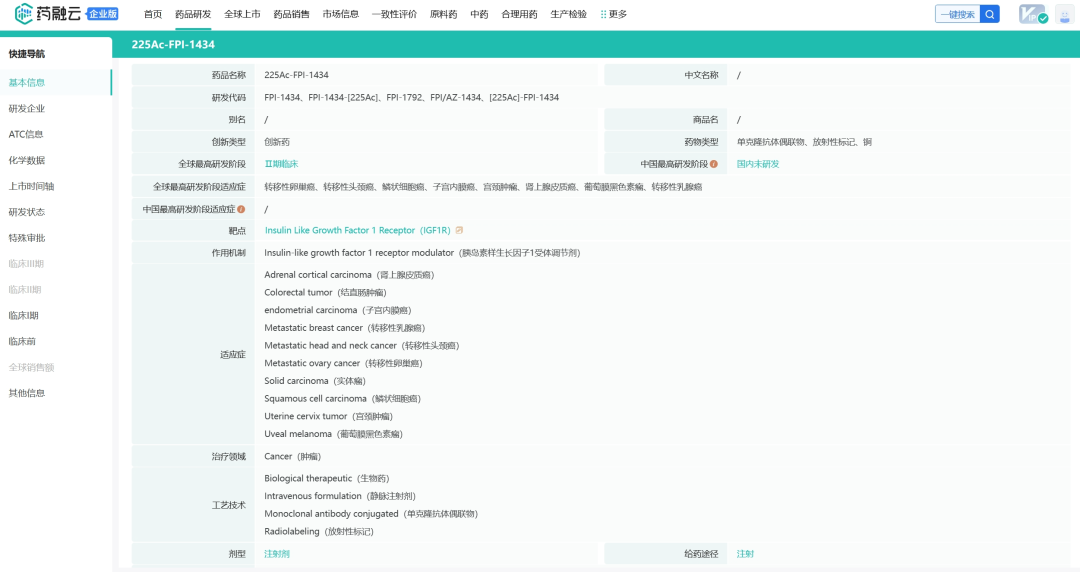
药融云数据库:药物基本信息
2023年6月,Fusion报告了冷/热给药方案队列1中3名患者15 kBq/kg的结果,在队列1中,观察到冷/热给药通常耐受性良好,没有与治疗相关的SAE(严重不良事件)或DLT(剂量限制性毒性)。冷抗体给药前显示出改善肿瘤摄取,同时也降低了在仅热给药组中观察到的血液学毒性。来自冷/热给药组的两名经过大量预处理的患者接受了三个和五个周期的治疗,两人都表现出持久的稳定疾病的最佳反应。
正在进行的FPI-1434的临床试验1期研究中,队列2的早期发现令人鼓舞。迄今为止,在25 kBq/kg剂量队列中未观察到DLT。三分之二的患者完成了DLT期,一名胰腺癌患者因疾病进展而停止治疗,一名接受重度治疗的尤因肉瘤患者在单次25 kBq/kg剂量的FPI-1434后显示出抗肿瘤活性,第二位患者接受了四个周期的治疗,并表现出疾病稳定作为最佳反应。总的来看,FPI-1434耐受性良好,在25 kBq/kg剂量水平下,无DLT和短暂的1级或更少的血小板减少。
基于FPI-1434的作用机制和临床前研究的数据,Fusion还评估了FPI-1434与检查点抑制剂以及DNA损伤修复抑制剂(DDRI)的组合潜力,其中包括聚(ADP-核糖)聚合酶(PARP)抑制剂。第一项计划的研究是评估FPI-1434与默沙东的抗PD-1疗法Keytruda(帕博利珠单抗)联合治疗表达IGF-1R的实体瘤患者。
FPI-2059
FPI-2059是一种靶向神经降压素受体1(NTSR1)的小分子放射性药物,在多种实体瘤中过表达,包括胰腺导管腺癌、结直肠癌、头颈部鳞状细胞癌、胃癌、尤文斯肉瘤和神经内分泌分化前列腺。目前正在开发作为各种实体瘤的靶向α疗法。FPI-2059基于一种以前称为IPN-1087 和3BP-227 的化合物,该化合物之前已在研究者赞助的研究和临床试验1期研究中作为发射β的放射性药物进行研究,Fusion于2021年收购了该资产,并使用锕-225将其转化为发射α的放射性药物。

FPI-2068是一种双特异性IgG的靶向α疗法(TAT),旨在将锕225递送至共表达EGFR和cMET的各种实体瘤。EGFR和cMET是经过验证的癌症靶点,在多种肿瘤类型中共表达,包括头颈部鳞状细胞癌、非小细胞肺癌、结直肠癌和胰腺导管腺癌。当前正在与阿斯利康根据合作协议共同开发。
2023年10月12日,Fusion表示在临床前研究中,FPI-2068在结直肠和肺肿瘤异种移植小鼠模型中显示出抗肿瘤功效,单剂量给药FPI-2068导致肿瘤消退时间延长。此外,FPI-2068引起 DNA损伤反应(DDR) 通路的激活以及细胞凋亡,表明细胞机制无法修复由α辐射诱导的DNA 损伤,这与提出的主要作用机制一致。
财务状况
2022财年,根据与阿斯利康的合作协议收入146万美元,上年同期为144万美元;研发费用为5890万美元;一般和行政费用为3060万美元;年度净亏损约为8760万美元。
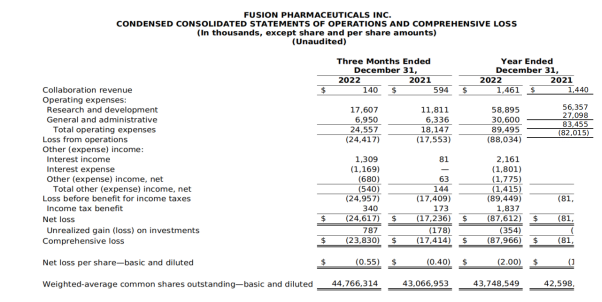
截至2023年9月30日的前三季度合作收入为207万美元;研发费用为4946万美元;一般和行政费用为2357万美元;净亏损6672万美元。第三季度为研发费用1460万美元,而2022年同期为1660万美元。这一下降主要是由于公司停止了FPI-1966项目的临床开发,导致该项目相关活动的减少,以及FPI-1434的临床试验1期的制造相关成本的降低,部分被FPI-2265的临床试验2期项目费用所抵消。一般和行政费用为680万美元,而2022年同期为740万美元,下降的主要原因是公司和专利相关法律费用的减少。报告净亏损1730 万美元,或每股0.25 美元,而2022 年同期净亏损2400 万美元,或每股0.55 美元。
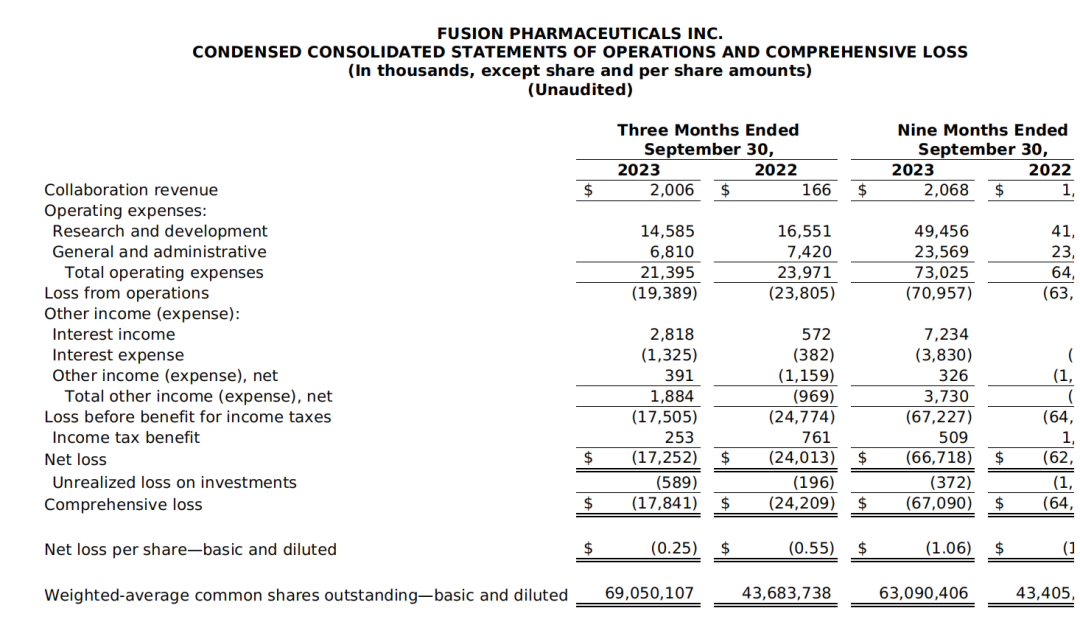
截至2023年9月30日,Fusion的现金、现金等价物和投资约为2.87 亿美元,其中计入公司市场股票发行计划下约6500 万美元的后续销售收益以及公司现有债务融资项下预计提取的1500万美元。Fusion预计,其现金、现金等价物和投资将足以为公司的运营费用和资本支出需求提供资金到2025年第四季度。
参考:
NMPA/CDE;
药融云数据,www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露(除标注外,正文图片均来自企业官网);等等
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论